Диспергационные методы получения коллоидных систем
Диспергированием называют измельчение твердых или жидких тел в инертной среде, при котором резко повышается дисперсность и образуется дисперсная сис-тема, обладающая значительной удельной межфазной поверхностью. Диспергиро-вание – не самопроизвольный процесс. Оно требует затраты энергии на преодо-ление межмолекулярных сил при дроблении вещества. Диспергирование делится на физические и химические виды.
Различают 3 способа физического диспергирования.
Размалывание в коллоидных мельницах. При простом механическом дробле-нии или растирании образуются порошки с сравнительно большими размерами зёрен (т.е. грубодисперсные системы). Для получения коллоидных систем диспергирование проводят в коллоидных мельницах (первая коллоидная мельница сконструирована Плауссоном в 1920 г.).
| Лабораторные коллоидные (шаровые) мельницы (рис.1 А) представляют собой вращающий барабан, заполненный шарами из материалов с определенной твердостью (из стали, чугуна или фарфора). При враще-нии барабана шары перекатываются и своими много-кратными ударами, раскалыванием и растиранием измельчают вещество на все более мелкие частицы. Принцип действия промышленных коллоидных мель-ниц (рис.1 Б) основан на развитии достаточно больших разрывающих (истирающих) усилий в веществе под действием центробежной силы в узком зазоре между вращающим ротором и неподвижным статором. Дроб-ление осуществляют в присутствии жидкой диспер-сионной среды и стабилизатора. | 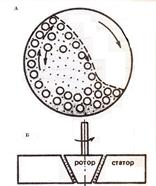 Рис.1. Схемы шаровой и
коллоидной мельниц
Рис.1. Схемы шаровой и
коллоидной мельниц
|
Коллоидные мельницы применяются для диспергирования минеральных красок, смазочных материалов (графит), пищевых веществ, фармацевтических препаратов (сера), сорбентов для хроматографии.
Дробление ультразвуком.Под действием звука большой частоты (15000-20000 Гц/с) происходит попеременное (быстро чередующееся) расширение и сжа-тие вещества, приводящее к разрушению частиц. Этот метод применим для веществ, у которых сравнительно небольшое взаимодействие между молекулами, например, для диспергирования жидкостей. Этим методом получают органозоли, коллоидные растворы серы, графит, гипс, крахмал, желатин, каучук и др. По этому способу получаются эмульсии, используемые при парэнтеральном питании больных (ожогами пищевода, раком желудка).
| Распыление электрической дугой. Для полу-чения золей металлов (серебра, золота, платины) электроды из соответствующего металла поме-щают в растворитель и пропускают ток большой силы. При этом в электрической дуге металл испаряется и его атомы, попав в окружающий чужеродный холодный растворитель, вытесняют-ся из окружения растворителя, конденсируются (объединяются) в более крупные частицы. Этот метод можно рассматривать и как конденсационный метод. | 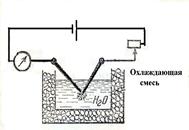 Рис.2. Схема прибора для получения золей металлов электрическим способом
Рис.2. Схема прибора для получения золей металлов электрическим способом
|
Химическое диспергирование (пептизация)
Перевод осадка, образовавшегося при коагуляции, в коллоидный раствор назы-вают химическим диспергированием. Термин был введён Т.Грэмом на основании чисто внешнего сходства процесса пептизации с растворением (перевариванием) белков под действием фермента желудочного сока пепсина.
Пептизация может происходить в результате промывания осадка растворите-лем или под действием специальных веществ – пептизаторов, которые представ-ляют собой сильные электролиты, образующиеся в результате химической реак-ции либо вводимые в раствор. При этом ионы пептизатора адсорбируются на по-верхности частиц рыхлого свежо образованного осадка, придают им определен-ный заряд. Благодаря этого частицы взаимно отталкиваются и наблюдается распад более крупных частиц осадка на мелкие. Таким образом происходит «химическое» раздробление вещества (см. рис. 3). 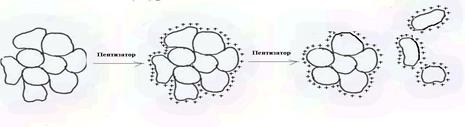
Рис.3. Механизм пептизации
Различают адсорбционную, химическую пептизации, промывание осадка растворителем. В случае адсорбционной пептизации осадок обрабатывают электролитом, содержащим ионы, способные к избирательной адсорбции на поверхности осадка (например, при обработке осадка Fe(OH)3 раствором FeCl3). В случае химической пептизации осадок вступает в химическое взаимодействие с небольшим количеством электролита (кислотой или щелочью), в результате которого образуется стабилизирующий электролит. Например, при частичной обработке осадка гидроксида железа (III) раствором соляной кислоты, протекает реакция Fe(OH)3 + HCl = FeOCl + 2H2O и образуется электролит, который диссоциирует на ионы: FeOCl 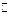 FeO+ + Cl-.
FeO+ + Cl-.
| На поверхности осадка Fe(OH)3, в соответствии с правилом Панета-Фаянса (в результате химичес-кого сродства), адсорбируются ионы FeO+ и при-дают ей положительный заряд. В результате элек-тростатического отталкивания одноименно заря-женных частей поверхности, наблюдается посте-пенное увеличение трещин (см. рис.4), что приво-дит к распаду агрегата осадка на более мелкие час-тицы. Процесс протекает до распада частиц на частицы коллоидных размеров. | 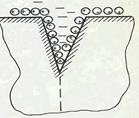 Рис.4 Схема расклинивающего действия адсорбированного слоя ионов пептизатора
Рис.4 Схема расклинивающего действия адсорбированного слоя ионов пептизатора
|
Промывание осадка растворителем осуществляют тогда, когда коллоидная система получена в присутствии значительного избытка одного из реагентов. Устойчивость системы достигается за счёт удаления некоторого избыточного количества электролита.
Дата добавления: 2015-11-12; просмотров: 3345;
