Лабораторная работа № 11.
Контрольная задача: "Определение содержании серной кислоты и растворе."
Цель: - знакомство со способами выражения концентрации растворов;
- приготовление стандартного раствора заданной концентрации;
- осуществление процесса титрования.
Приборы: техно- химические весы, бюретка, колба, пипетки, химический стакан.
Реактивы: контрольный раствор серной кислоты H2SO4, установочное вещество - 0,1н раствор щелочи NaOH, индикатор- фенолфталеин.
Ход работы: Объем контрольного раствора H2SO4 в мерной колбе вместимостью 100мл доводят до метки раствором щелочи NaOH. Пипетку промывают водопроводной, а затем дистиллированной водой и ополаскивают контрольным раствором H2S04. В колбу для титрования пипеткой переносят 10мл раствора серной кислоты H2S04, добавляют 1-2 капли раствора феиофталеина и титруют до слабо- розового окрашивания так же, как при установлении титра щелочи NaOH. Определение повторяют трижды и для расчетов берут среднее значение. Результаты записывают в таблицу.
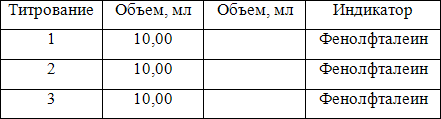
Вычисления содержания серной кислоты проводят двумя способами:
1-й способ: Вычислить нормальную концентрацию раствора по формуле:
N(H2SО4) = V(NaOН)* N(NaOН)\ V(H2SО4);
Вычислить титр раствора по формуле:
T(H2SО4)=N(H2SО4)* Э(H2SО4)\1000;
Вычислить содержание в H2SО4 100мл раствора по формуле:
m(H2SО4) = T(H2SО4)* l00;
2-й способ: Вычислить титр по серной кислоте по формуле:
T(NaOН\H2SО4)= N(NaOН)* (H2SО4)\1000;
Вычислить содержание серной кислоты в 100мл раствора по формуле:
m(H2SО4) = T(NaOН\H2SО4)* V(NaOH)* 10
Контрольные вопросы:
1. В чем сущность метода нейтрализации? Какая химическая реакция лежит в основе этого метода?
2. Что такое стандартный или титрованный раствор?
3. Что такое индикатор?
4. Что такое нормальная концентрация раствора, титр, титр по определяемому веществу?
5. Вычислить титр 0,1096н раствора соляной кислоты НС1.
6. Навеску соды Na2СО3 массой 0,5300г растворили в мерной колбе на 100мл. Определить титр и нормальную концентрацию полученного раствора.
7. На титрование раствора соляной кислоты HCI израсходовано 10мл 0,1н раствора КОН. Какому объему 0,1н раствора кислоты это соответствует?
Дата добавления: 2015-11-10; просмотров: 3274;
