Лекции 7-8-9. Задачи, решаемые кристаллохимией
План лекции
1 Координационное число, координационный полиэдр, число формульных единиц.
2. Плотнейшие шаровые упаковки в кристаллах.
3. Основные типы структур.
4. Основные категории кристаллохимии: морфотропия, полиморфизм, изоморфизм.
Кристаллохимия изучает проблемы связи между строением и химическим составом кристаллов, которые позволяют понять их свойства.
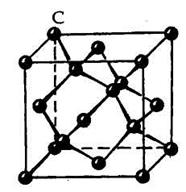
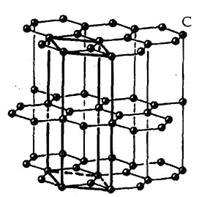
Химический состав минералов — это фундаментальная характеристика, от которой зависят многие их физические свойства. Однако свойства минералов в значительной степени зависят и от геометрического расположения составляющих структуру соединений атомов, ионов или молекул, от природы химических сил — химических связей, реализованных в том или ином кристалле. В качестве примера можно рассмотреть структуры двух модификаций углерода: графита и алмаза (см. рис. 7.1 а, б), различные свойства которых связаны именно с геометрией расположения атомов углерода и соответственно с типом химических связей между ними.
 а
а
|  б
б
|
| Рис. 7.1. Кристаллические структуры алмаза а) и графита б) |
Таким образом, для понимания свойств кристаллов следует в первую очередь принимать во внимание их структуры. Именно поэтому в основу кристаллохимии положены сведения о пространственном расположении атомов в структуре кристаллических тел, т. е. данные структурного анализа кристаллов. Этот аналитический метод базируется на открытом в 1912 г. немецким физиком М. Лауэ явлении — дифракции рентгеновских лучей на кристаллах; благодаря чему стало возможным получать сведения об атомном строении вещества. Именно рентгеноструктурный анализ, оказавшийся наиболее информативным экспериментальным методом изучения строения химических соединений, и стал основой кристаллохимии.
Огромная работа по установлению связи между химическим составом кристаллов и их симметрией проведена русским кристаллографом Е. С. Федоровым и немецким кристаллографом Гротом. Ими была подмечена закономерность, впоследствии названная законом Федорова-Грота, который гласит: кристаллы веществ с простым химическим составом обладают более высокой симметрией по сравнению с кристаллами более сложного состава,т. е. степень симметричности кристалла уменьшается с ростом относительной сложности его состава. Как известно, наиболее высокой симметрией характеризуются кристаллы кубической и гексагональной сингоний. Отсюда можно ожидать, что симметрия большинства веществ простого состава будет относиться к этим сингониям. Действительно, симметрия кристаллов самородных Си , Ag, Pt, Аи, алмаза — кубическая. Структуры же минералов сложного состава, таких как роговая обманка Ca2Na(Mg, Fe)/Al, Fe)[Si6Al2O22] • (ОН)2, мусковит KAl2[Si3AlO10] • (ОН)2, альбит Na[AlSi3G8] и др., более низкосимметричны.
Дата добавления: 2015-08-21; просмотров: 1089;
