ОСНОВНЫЕ ФОРМЫ ПОВРЕЖДЕНИЯ КЛЕТОК
Различают три формы повреждения клеток: 1) ишемическое и гипоксическое повреждение; 2) повреждение, вызванное свободными радикалами, включая активированный кислород; 3) токсическое повреждение.
1. Ишемическое и гипоксическое повреждение. Чаще всего оно обусловлено окклюзией артерий. При этом изначально гипоксия воздействует на аэробное дыхание клетки — окислительное фосфорилирование в митохондриях. В связи с тем что напряжение кислорода в клетке снижается, прекращается окислительное фосфорилирование, а образование АТФ уменьшается или останавливается.
Исчезновение АТФ ведет к быстрому набуханию (отеку) клетки — одному из ранних проявлений ишемического повреждения. Отек клетки обусловлен нарушением регуляции объема клетки плазматической мембраной. Баланс между содержимым клетки и окружающей ее средой обеспечивается энергетически зависимым натриевым насосом, который поддерживает концентрацию калия внутри клетки значительно более высокой, чем внеклеточная. Наблюдается отделение рибосом от мембран гранулярной эндоплазматической сети и диссоциация полисом в моносомы. На поверхности клеток могут образовываться "волдыри", а клетки, имеющие на поверхности микроворсинки, их утрачивают (эпителий проксимальных канальцев почек). В цитоплазме и вне клеток появляются "миелиновые фигуры", образующиеся из цитоплазмы и мембран органелл. Митохондрии набухают, а эндоплазматическая сеть остается расширенной.
Необратимые изменения морфологически ассоциируются с выраженной вакуолизацией митохондрий, повреждением плазматических мембран и набуханием лизосом. Вслед за гибелью клетки ее компоненты прогрессивно разрушаются, и происходит выброс ферментов клетки во внеклеточное пространство. Умершие клетки образуют массы, состоящие из фосфолипидов в виде «миелиновых фигур», которые подвергаются фагоцитозу и разрушаются до жирных кислот.
Проникновение ферментов сквозь поврежденную клеточную мембрану, а затем в сыворотку крови позволяет клинически определять параметры смерти клетки. Например, сердечная мышца содержит трансаминазы, лактатдегидрогеназу и креатинкиназу. Повышение содержания этих ферментов в сыворотке крови является клиническим критерием инфаркта миокарда (смерти кардиомиоцитов).
■ Таким образом, основными признаками необратимости повреждения клетки служат невосстановимые повреждения митохондрий, приводящие к потере АТФ, а также развитие глубоких повреждений плазматических мембран, в основе которых лежит ряд биохимических механизмов.
Во-первых, в некоторых ишемизированных тканях, например печени, необратимое ишемическое повреждение сопровождается заметным уменьшением содержания фосфолипидов в клеточной мембране, которое происходит под действием кальцийзависимых фосфолипаз.
Во-вторых, активация протеаз, обусловленная повышением концентрации кальция в цитозоле, ведет к повреждению цитоскелета, выполняющего роль якоря между плазматической мембраной и внутренним содержимым клетки. В результате во время набухания клетки происходит отслойка клеточной мембраны от цитоскелета, что делает мембрану более податливой к растяжению и разрыву.
В-третьих, при ишемии появляется небольшое количество высокотоксичных свободных радикалов кислорода.
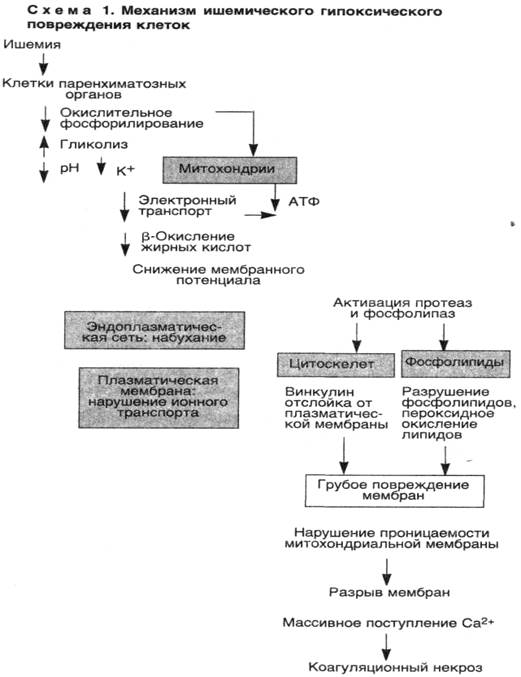
Итак, основными механизмами гибели клетки при гипоксии являются нарушение окислительного фосфорилирования, приводящее к недостаточности АТФ, повреждение мембран клетки, а важнейшим медиатором необратимых биохимических и морфологических изменений является кальций (схема 1).
2. Повреждение клетки, вызванное свободными радикалами кислорода. Чаще всего такое повреждение возникает под воздействием химических веществ, лучистой энергии, кислорода и других газов, а также при старении клеток, разрушении опухолей макрофагами и в некоторых иных случаях.
Свободные радикалы представляют собой молекулы кислорода, имеющие один непарный электрон на внешней орбите. В таком состоянии радикал исключительно активен и нестабилен и вступает в реакции с неорганическими и органическими соединениями — белками, липидами и углеводами.
Для повреждения клетки наибольшее значение имеют три реакции, в которые вступают свободные радикалы.
• Свободнорадикальное пероксидное окисление липидов (СПОЛ) мембран. Свободные радикалы в присутствии кислорода могут вызывать пероксидное окисление липидов плазматической мембраны и органелл. Липидно-радикальные взаимодействия приводят к образованию пероксидов, которые сами по себе являются активными соединениями, инициирующими последующее повреждение других жирных кислот; возникает цепь аутокаталитических реакций, обусловливающая обширное повреждение мембран, органелл и самих клеток.
• Окислительное превращение белков. Свободные радикалы вызывают перекрестное связывание таких лабильных аминокислот, как метионин, гистидин, цистин и лизин, а также фрагментацию полипептидных цепей. Окислительное превращение усиливает разрушение ключевых ферментов посредством нейтральных протеаз, содержащихся в цитозоле.
• Повреждение ДНК. Свободные радикалы вступают в реакцию с тимином, входящим в состав ДНК. Такое повреждение ДНК ведет к гибели клетки или ее злокачественному превращению. Митохондриальная ДНК также повреждается.
Свободные радикалы могут разрушаться спонтанно. Например, супероксидный анион-радикал является нестабильным соединением и спонтанно разрушается с образованием кислорода и пероксида водорода. Однако имеется несколько ферментных и неферментных систем, которые способствуют окончанию или инактивации свободнорадикальных реакций. Эндогенными или экзогенными антиоксидантами являются витамин Е; сульфгидрилсодержащие соединения — цистеин и глютатион; белки сыворотки — альбумин, церулоплазмин и трансферрин. Полагают, что трансферрин действует как антиоксидант, связывая свободное железо, которое, как известно, может играть роль катализатора образования свободных радикалов.
Среди ферментов выделяют супероксиддисмутазу, способную превращать супероксидный анион-радикал в пероксид водорода.
Каталаза, сосредоточенная в пероксисомах, разрушает пероксид водорода до кислорода и воды.
При многих патологических процессах конечный результат действия свободных радикалов зависит от баланса между образованием свободных радикалов и их разрушением.
3. Токсическое повреждение. Примером такого повреждения является действие химических веществ, вызывающих повреждение клетки посредством одного из двух механизмов. Во-первых, часть водорастворимых соединений может действовать непосредственно, связываясь с некоторыми молекулами или органеллами. Например, при попадании в организм хлорида ртути ртуть связывает сульфгидрильные группы клеточной мембраны и других белков, вызывая повышение проницаемости клеточной мембраны и торможение АТФаза-зависимого транспорта. В подобных случаях наиболее выраженные изменения наблюдаются в клетках, которые используют, абсорбируют, выделяют или концентрируют эти химические соединения. При попадании в организм хлорида ртути в наибольшей степени страдают клетки желудочно-кишечного тракта и почек. Цианид непосредственно воздействует на ферменты митохондрий. Многие противоопухолевые химиотерапевтические препараты, в том числе антибиотики, также вызывают повреждение клеток посредством цитотоксического действия.
Во-вторых, некоторые другие химические соединения, особенно жирорастворимые токсины, биологически неактивны ивначале превращаются в токсичные метаболиты, которые затем действуют на клетки-мишени. Хотя эти метаболиты могут вызывать повреждение мембран иклеток путем прямого ковалентного связывания с мембранными белками и липидами, наиболее важный механизм повреждения мембран включает образование реактивных свободных радикалов и последующее СПОЛ.
Дата добавления: 2015-08-14; просмотров: 1150;
