Поддержание кислотно-основного равновесия в полости рта
Поддержание кислотно-основного равновесия в полости рта – очень сложный важный процесс. Полость рта непосредственно контактирует с окружающей средой, является началом пищеварительного тракта, имеет неоднородный рельеф органов полости рта и зоны, труднодоступные для процесса самоочищения.
К факторам, дестабилизирующим постоянство рН ротовой жидкости, относят: прием пищи, употребление лекарственных препаратов, вредные привычки (курение), профессиональные вредные факторы, попадающие из внешней среды или выделяющиеся из организма со слюной, метаболическая активность ротовой микрофлоры, наличие заболеваний зубов и мягких тканей полости рта. Поэтому сдвиги рН в ротовой полости наблюдаются часто.
Изменения КОС в полости рта бывают физиологические и патологические.
Физиологические отклонения обусловлены, как правило, приемом пищи, носят временный характер, быстро компенсируются, не приводят к нарушениям физиологических процессов и не вызывают структурные изменения в тканях полости рта. Соматические заболевания и болезни в полости рта могут вызывать стойкие патологические изменения КОС, приводящие к существенным нарушениям структуры и функции тканей полости рта.
рН ротовой жидкости подвергается суточным колебаниям – минимум утром, а к вечеру рН повышается. Ночью рН ротовой жидкости ниже, чем днем. Наряду с суточными колебаниями отмечены и возрастные изменения рН. С возрастом рН ротовой жидкости снижается. Наблюдается закономерное снижение рН слюны при беременности.
В регуляции постоянства КОС в полости рта принимают участие облигатные и факультативные факторы: КОС полости рта зависит от общего состояния организма, характера питания, условий труда, состояния саливации, жевательной активности, характера и активности ротовой микрофлоры, наличия искусственных протезов, состояние гигиены полости рта и других.
1) Однако главным естественным регулятром кислотно-щелочного равновесия в полости рта является слюна. Слюна обладает выраженными буферными свойствами, которые обеспечиваются тремя буферными системами, входящими в ее состав, - бикарбонатной, белковой и фосфатной. 80% буферной емкости слюны обеспечивается за счет бикарбонатной буферной системы. Следует заметить, что буферные системы ротовой жидкости содержат в 6 раз больше щелочнореагирующих компонентов, чем кислых, благодаря чему буферные свойства слюны более выражены при действии кислых продуктов.
Буферная функция слюны подвержена значительным колебаниям и определяется, прежде всего, ее составом и количеством, которые, в свою очередь, зависят от функциональной активности слюнных желез, скорости и характера слюноотделения (нестимулированная или стимулированная секреция), жевательной активности. Стимулированная слюна секретируется под влиянием раздражения вкусовых рецепторов, жевания. Из вкусовых раздражителей наиболее интенсивным стимулятором является кислый вкус. Вот почему с целью профилактики значительного и длительного снижения рН в полости рта целесообразно добавлять в пищу и напитки небольшое количество слабых пищевых кислот (лимонной, уксусной). Стимулированная слюна отличается от нестимулированной по скорости секреции, составу, в частности, содержанию бикарбонатов. Концентрация бикарбонатов в нестимулированной слюне находится в пределах 1 ммоль/л, а в стимулированной - повышается до 15 ммоль/л. Следовательно, ее буферные свойства, способность к нейтрализации кислых продуктов более выражены.
Стимулирует слюноотделение жевание. Употребление жевательных резинок даже без вкусовых наполнителей оказывает благоприятное влияние на рН полости рта благодаря стимуляции секреции слюны. Вкусовые добавки к ним способствуют более активной стимуляции секреции. Отмечено, что рН слюны повышается с увеличением скорости выделения. Более высокая скорость слюноотделения днем, чем в ночное время, определяет то обстоятельство, что водородный показатель слюны днем выше, чем ночью.
Нарушения слюноотделения и состава слюны, наблюдаемые при многих заболеваниях, сопровождаются устойчивым изменением кислотно-основного состояния и недостаточностью буферных систем в полости рта.
К числу важных факторов саморегуляции КОС в полости рта можно отнести и эмаль зубов. Эмаль зубов является своеобразной буферной системой, участвующей в поддержании должного КОС, а именно, в связывании избытка ионов водорода, оказывающихся на поверхности эмали. Как известно, основным компонентом эмали является гидроксиапатит, кристаллы которого способны к ионному обмену. Во внутреннюю часть кристалла гидроксиапатита могут проникать лишь немногие ионы – это ионы, входящие в состав кристалла, или близкие к ним по строению и свойствам. Ионы водорода относятся к числу тех, которые относительно легко проникают внутрь кристаллов. При резком увеличении содержания кислот в полости рта происходит выход ионов кальция из эмали, а на их место поступают по два водородных иона. Таким образом, эмаль поглощает избыток водородных ионов.
Из дестабилизирующих факторов кислотно-основного состояния в полости рта, в первую очередь, необходимо указать на пищу. Пищевые продукты в зависимости от их характера способны изменять рН полости рта, как в кислую, так и в щелочную сторону. Однако если продукты питания недолго задерживаются в ротовой полости, то эти изменения незначительны и быстро компенсируются.
Наиболее выраженное смещение рН в ротовой полости наблюдается после употребления пищи, содержащей простые углеводы, – сахарозу, глюкозу, фруктозу. Принято даже говорить о специфическом эффекте углеводов в полости рта, так как аналогичных изменений при приеме других пищевых продуктов не наблюдается. Простые углеводы подвергаются быстрой ферментации микрофлорой зубного налета, вызывают резкую активацию гликолиза, в результате чего в полости рта образуются и накапливаются органические кислоты – молочная, пировиноградная и др. Их количество в ротовой жидкости возрастает в 9-16 раз в течение ближайших 20 мин после приема сахара, что приводит к снижению рН слюны. Кроме того, пища, богатая сахарами, стимулирует рост зубного налета (бляшки) за счет того, что она способствует размножению микроорганизмов, особенно кислотообразующих. Последние способны из сахарозы синтезировать внеклеточные полисахариды – декстран, гликан и леван. Благодаря этим запасам полисахаридов в зубном налете (бляшке) возможно еще длительное образование кислот после приема углеводов.
У поверхности эмали концентрация кислот может быть в несколько раз выше, чем в наружном слое зубного налета.
Таким образом, постоянное употребление большого количества углеводов приводит к смещению рН ротовой жидкости в кислую сторону, что, по современным представлениям, способствует развитию кариеса. Однако показано, что кариесогенность углеводов уменьшается при интенсивном жевании – образующиеся при употреблении углеводов кислоты частично нейтрализуются за счет обильного выделения слюны.
Если прием углеводов сопровождается образованием кислых продуктов, то употребление азотсодержащих продуктов (как источник легкоусвояемых субстратов для микроорганизмов полости рта) ведет к накоплению щелочных веществ. В результате метаболических превращений аминокислот, мочевины в ротовой полости образуются аммиак, моно- и диамины, которые способны нейтрализовать кислые продукты, сдвигать рН ротовой жидкости в щелочную сторону. Наиболее важным источником щелочных продуктов в ротовой полости является гидролиз мочевины микробной уреазой с образованием аммиака и аммонийных солей.
Следовательно, в ротовой полости имеют место два противоположно направленных процесса: накопление кислых продуктов в результате ферментации углеводов и накопление щелочных продуктов как следствие утилизации азотсодержащих веществ. Эти два процесса в известной степени и определяют рН ротовой жидкости.
Существенным фактором, влияющим на КОС полости рта, является зубной налет. Зубной налет (бляшка) – это скопление колоний микроорганизмов различных типов, преимущественно кислотообразующих, на поверхности зубов. Помимо микроорганизмов в состав зубного налёта входит небольшое количество слущенного эпителия слизистой оболочки, гликопротеидов слюны, внеклеточных полисахаридов (декстран, леван, гликан). Углеводы легко оседают в зубном налёте и способствуют его дальнейшему образованию.
Наиболее быстро зубной налёт накапливается в межзубных промежутках и проксимальных поверхностях верхних жевательных зубов, то есть в местах, где очищение зубов затруднено. (в пособии стоит, где ЗН)
Микроорганизмы зубного налёта, утилизируя углеводы пищи, вырабатывают большое количество органических кислот. Скорость образования кислот в зубном налёте очень высока и зависит от многих факторов – количества и вида микробных популяций зубного налёта, его субстрата, локализации и диффузионных свойств, буферной емкости слюны и самого зубного налёта (бляшки). Из-за низкой проницаемости зубного налёта, образующиеся кислоты, с одной стороны, не способны диффундировать за пределы налёта, а с другой стороны, они защищены от действия буферных систем. В результате концентрация водородных ионов в зубном налёте резко возрастает; рН на поверхности эмали, покрытой зубной бляшкой, может снижаться до 4,5-5,0. При этом создаются благоприятные условия для очаговой деминерализации эмали и развития кариеса. Помимо зубного налёта выраженное влияние на КОС в полости рта оказывает налёт на языке.
Изменение рН зубного налёта или омывающей его ротовой жидкости, развивающееся после сахарозной нагрузки, получило название кривой Стефана.
В 1940 г. американец Роберт Стефан (R.Staphan) после полоскания полости рта растворами глюкозы и сахарозы наблюдал быстрое снижение рН в зубном налёте (через 2-5 мин) часто до уровня, при котором происходит деминерализация эмали, с последующим медленным возвращением рН к исходному уровню (через 30-60 мин). Изучение кривой Стефана (ее формы, амплитуды, длительности восстановления) приобрело практическую значимость. По скорости снижения рН на кривой Стефана можно судить о массе зубного налёта, его бактериальном составе, активности ферментов, вырабатываемых микробами зубной бляшки, буферной ёмкости зубного налёта и ротовой жидкости, что необходимо для прогнозирования предрасположенности к кариесу, для оценки эффективности проведенного стоматологического лечения. Так, у пациентов с активным течением кариеса или высокой к нему предрасположенности снижение рН на кривой Стефана происходит быстро и до весьма низких цифр. При этом наблюдается медленное восстановление рН до исходного уровня.
Кривая Стефана является высокоинформативным тестом в оценке кариесогенного потенциала жевательных резинок, продуктов питания, в особенности углеводсодержащих (леденцов, шоколадных конфет и др.), напитков, содержащих сахарозу (фанта, пепси-кола и др.), антикариесогенных свойств гигиенических средств.
Ещё одним из факторов, активно влияющих на КОС полости рта, является метаболическая активность микроорганизмов. При патологии полости рта и даже при наличии зубных протезов может изменяться состав ротовой микрофлоры. Кстати, зубные протезы способны существенно менять не только экологию, но и соотношение факторов, регулирующих КОС в полости рта. Выработка кислот микрофлорой в полости рта идёт в основном по анаэробному типу, а основной кислотой, вырабатываемой бактериями, является молочная. При преобладании кислотообразующих микроорганизмов, способных к ферментации углеводов, рН ротовой жидкости отклоняется в кислую сторону. В случае преобладания микробов, продуцирующих уреазу, как это нередко имеет место при болезнях пародонта, создаются условия для сдвига рН в щелочную сторону.
Изменения КОС в полости рта могут происходить в сторону и ацидоза, и алкалоза.
Ротовая жидкость (смешанная слюна) в физиологических условиях является структурированной коллоидной системой и представляет собой перенасыщенный раствор гидроксиапатита, вернее, продуктами его гидролиза – ионами кальция (Са2+) и гидрофосфата (НРО42–).Считается, что эти компоненты входят в состав коллоидных мицелл фосфата кальция, что обеспечивает их устойчивость в перенасыщенном состоянии. Благодаря перенасыщенности слюны этими веществами создается препятствие растворению эмали зубов, облегчается внедрение ионов кальция и фосфатов из слюны в эмаль, то есть, другими словами, осуществляется минерализующая функция слюны.
При сдвиге КОС в кислую сторону снижаются устойчивость мицелл и степень насыщенности эмали гидроксиапатитом. При этом В.К.Леонтьев (1978) выделил два типа нарушений КОС в полости рта. Первый тип – при рН слюны 6,76-6,3. Слюна начинает терять насыщенность гидроксиапатитом. В составе мицелл вместо основного фосфата преобладает кислый – не участвует в минерализации, является основным потенциалобразующим ионом в мицеллах.. Ионы Са не связываются с матрицей эмали, поэтому декальцификация эмали преобладает над минерализацией.
Второй тип – при дальнейшем снижении рН слюны: ниже 6,2-6,0.
•••Эта величина рН считается критической: происходит резкое снижение насыщенности слюны гидроксиапатитом. Слюна из состояния перенасыщения переходит в ненасыщенное, из минерализующей жидкости становится деминерализующей. Процесс минерализации эмали полностью прекращается, возрастает скорость её растворения.
•••При таком подкислении ротовой жидкости повышается активность протеиназ, что также способствует деминерализации зубов.
•••Кислая среда способствует преципитации муцина, и он начинает откладываться на поверхности зубов. Выпадение муцина способствует образованию зубных бляшек. В нейтральной среде слюна равномерно обволакивает зубы, образуя на них особую органическую оболочку.
При сдвиге кислотно-основного состояния в щелочную сторону в ротовой жидкости увеличивается содержание фосфатов, образуются труднорастворимые соединения фосфата кальция Са3(РО4)2, что приводит к нарушению процесса мицеллообразования. Большая перенасыщенность слюны гидроксиапатитом, нарушение процесса мицеллообразования в щелочной среде способствуют образованию кристаллов и зубного камня. (на фоне очень низкого содержания Н2РО4–, ионы К, Na, как электролиты, способствуют снижению заряда мицелл, приближая его к изоэлектрическому состоянию). Существует точка зрения, что защелачивание ротовой жидкости, часто имеющее место при гингивитах и пародонтите, носит защитно-компенсаторный характер и направлено на снижение патогенного действия кислот, образующихся при воспалении. Как бы там ни было, но именно щелочная среда способствует интенсификации процесса налетообразования и отложению зубного камня при этих заболеваниях.
• Наиболее сильным фактором, снижающим рН слюны, является микрофлора. Снижение рН происходит при попадании в полость рта углеводов.
Изучали характер слюноотделения у кондитеров. Было установлено, что содержание остаточных сахаров в смешанной слюне кондитеров в середине рабочего дня превышало исходный уровень в 5-7 раз. Углеводы же являются прекрасной питательной средой для микрофлоры.
ОСОБЕННОСТИ УГЛЕВОДНОГО ОБМЕНА В РОТОВОЙ ПОЛОСТИ
Специфическое влияние углеводов на обмен веществ связано с тем, что они могут вступать в процессы обмена сразу же в полости рта, где условия для усвоения углеводов микрофлорой близки к идеальным: здесь постоянная температура, (~37ºС), влага, близкое к нейтральному значение рН.
Сахар (сахароза) и некоторые другие простые углеводы (глюкоза, фруктоза) оказывают специфическое воздействие на состав слюны и обмен веществ в полости рта. Оно проявляется в том, что после приема простых углеводов в полости рта происходит своеобразный "взрыв" обменных процессов. Метаболический взрыв осуществляется микрофлорой полости рта и зубного налёта. Условия для усвоения углеводов микробами в полости рта идеальные.
Микробы очень активно используют углеводы для своих нужд и запасают их впрок в виде резервных полисахаридов декстранов. Основной механизм утилизации:
1. Происходит значительная активация гликолиза и накопление в полости рта молочной, пировиноградной и других кислот. Их количество в слюне возрастает в 9-16 раз в ближайшие 20 мин после приема сахара, затем быстро уменьшается, возвращаясь к исходному уровню через 60-90 мин.
2. Это приводит к подкислению слюны
3. деминерализующее действие образовавшихся при гликолизе кислотприводит квымыванию кальция и повышению его концентрации в слюне
4. одновременно идёт затрата фосфора на фосфорилирование в энергетических процессах, чтоприводит куменьшению концентрации фосфата.
Механизмы патогенных эффектов углеводов в полости рта
Метаболизм углеводов осуществляется в слюне и некоторых других структурах полости рта. Даже в физиологических условиях в ротовой полости много органических кислот: молочной, пировиноградной, уксусной, различных аминокислот.
Кариесогенные процессы наиболее интенсивно протекают в мягком ЗН. Прием легко усвояемых углеводов – пусковое звено в цепи реакций гликолиза, которые ведут к нарушению гомеостаза полости рта, преобладанию процессов деминерализации эмали.
Метаболизм углеводов завершается образованием органических кислот, повышенная концентрация которых способствует местному сдвигу рН (в зубном налете) и развитию кариеса. У больных кариесом продукция кислот достоверно выше, а нормализация происходит гораздо медленнее.
С другой стороны, синтезируемые микробами резервные полисахариды – декстраны способствуют очень плотному прикреплению микроорганизмов, а заодно и пищевых остатков, и всего зубного налета к поверхности эмали. Все это тоже увеличивает риск образования кариеса.
Исследования показали, что избыток сахаров в пище ведет к накоплению гликогена в твердых тканях зубов. Расщепление гликогена эмали рассматривается как один из начальных моментов развития поверхностного кариозного поражения.
Кроме того, в этих условиях легче происходит образование зубного камня, что впоследствии ведет к развитию заболеваний пародонта.
Кариесогенная роль углеводов зависит не только от потребления большого количества, но также от частоты приема сахара и его количества, остающегося в полости рта, физических свойств сладких продуктов (вязкость, липкость). Чем чаще и длительнее сахар задерживается в полости рта и соприкасается с зубами, тем более выраженное кариесогенное действие он оказывает
Дольше всего задерживаются в полости рта сахаросодержащие пищевые продукты липкой консистенции такие, как шоколад, карамель, сахарный сироп и др.
Длительное время задерживаются углеводы в полости рта при приеме сладостей мягкой консистенции с большей концентрацией сахара.
Недолго сохраняются в полости рта углеводы после приема напитков с концентрацией сахара менее 10%.
• В среднем наиболее высокое содержание глюкозы в смешанной слюне после приема сладостей сохраняется в первые 30 мин.
• Полоскание полости рта чаем, содовым раствором или чистка зубов щеткой позволяют существенно снизить концентрацию глюкозы и ее метаболитов (пирувата, лактата и др.) в смешанной слюне человека после приема сладостей.
• Значительно (практически в 6 раз) ускоряют элиминацию углеводов из полости рта средства гигиены: 1-2% раствор бикарбоната натрия, чистка зубной щеткой.
ИММУНОГЛОБУЛИН А. IgA - это основной класс антител в ротовой полости.
n Повторим: В сыворотке крови содержится в виде мономеров, димеров и тетрамеров, соединенных J-цепью, не связывает комплемент, не проходит через плаценту.
В крови концентрация 2 г/л, 20% от всех Ig.
В слюне – в основном димеры. Т.Е. IgА находится не только в крови, он также секреторный иммуноглобулин. IgА содержится в секретах слизистых (в слюне, слезной жидкости, молозиве, бронхиальном секрете).
РИСунок ниже: Fc рецепторы эпителиальных клеток слизистой и протоков слюнных желез связывают димер IgA, затем к IgА при его прохождении через эпителиальные клетки присоединяется секреторный компонент – особый белок, который синтезируется там же, и называется секреторный комплекс SC. Образуется секреторная форма IgA - sIgA. sIgA выходят на поверхность эпителия и играют решающую роль в местном иммунитете слизистой полости рта.
Трансцитоз IgA через эпителиальные клетки в проток железы
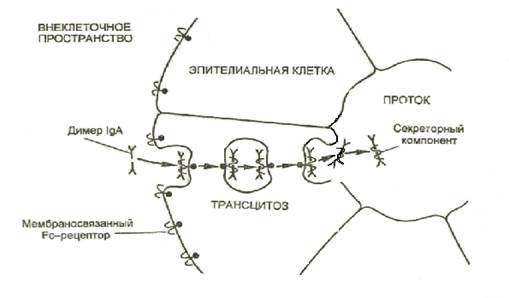
n Т.Е. Биологическая роль этого иммуноглобулина - в основном местная защита слизистых оболочек от инфекции. Иммуноглобулины этого класса связываются с микроорганизмами и препятствуют их присоединению (прилипанию=адгезии) к поверхности эпителиальных клеток, затрудняя размножение.
Кроме синтезируемых местно секреторных IgA в ротовой полости находятся еще сывороточные IgA, проникающие из крови. Секреторные IgA более устойчивы к действию протеолитических ферментов, способны более эффективно нейтрализовать вирусы, бактериальные токсины, ферменты и агглютинировать бактерии по сравнению с сывороточными IgA. Высокая устойчивость sIgA к действию протеолитических ферментов позволяет им проявлять свою биологическую активность в средах с высоким содержанием протеолитических ферментов даже в воспалительных экссудатах.
Иммуноглобулины класса А препятствуют прикреплению широкого спектра микроорганизмов к слизистой оболочке и поверхности зуба, в том числе и кариесогенного стрептококка (Str. mutans), что предотвращает развитие кариеса; выступают в роли опсонинов и активируют фагоцитоз; нейтрализуют вирусы и препятствуют всасыванию антигенов через слизистую оболочку. Чем больше sIg А, тем выше устойчивость к патогенам бактериальной, вирусной и грибковой природы. Нормальный уровень синтеза sIgA – одно из условий достаточной устойчивости детей первых месяцев жизни к инфекциям, поражающим слизистую полости рта. IgA связывает различные антигены (пищевые, микробные) и предотвращает сенсибилизацию организма.
Кроме IgA в ротовой полости содержатся IgM и IgG. Их количество значительно меньше (особенно IgM), чем IgA, но больше, чем при простой диффузии из плазмы крови, что свидетельствует об их местном происхождении. Выявлены следовые количества IgE, который главным образом поступают в полость рта из плазмы крови путем пассивной диффузии подобно IgG.
Дата добавления: 2015-08-14; просмотров: 2811;
