ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС
Если внешние условия, в которых находится термодинамическая система, изменяются, то будет изменяться и состояние системы. Совокупность изменений состояния термодинамической системы при переходе из одного равновесного состояния в другое называют термодинамическим процессом.
Под термодинамическим процессом понимается совокупность последовательных состояний, через которые проходит термодинамическая система при ее взаимодействии с окружающей средой. Другими словаминепрерывное изменение состояния рабочего тела в результате взаимодействия его с окружающей средой называется термодинамическим процессом или сокращенно процессом. Или по другому - изменение состояния термодинамической системы во времени называется термодинамическим процессом.
Различают равновесные (квазистатические) и неравновесные процессы.
Равновесным называют такое состояние системы, при котором во всех точках ее объема все параметры состояния (давление, температура, удельный объем и др.) и физические свойства одинаковы. В термодинамике постулируется, что изолированная система с течением времени всегда приходит в состояние термодинамического равновесия и никогда не может самопроизвольно выйти из нее. Можно сказать так – если процесс происходит бесконечно медленно и при ничтожно малой разности температур окружающей среды и рабочего тела, то можно достигнуть равномерного распределения, как температуры, так и давления по всей массе рабочего тела.
Такой процесс будет также называться равновесным.
Процесс, протекающий при значительной разности температур и давлений окружающей среды и рабочего тела и создающий неравномерное распределение температуры и давлений по всей массе рабочего тела, называется неравновесным.
Система, выведенная из состояния равновесия, и предоставленная при постоянных параметрах окружающей среды самой себе, через некоторое время вновь придет в равновесное состояние, соответствующее этим параметрам. Такое самопроизвольное (без внешнего воздействия) возвращение системы в состояние равновесия называется релаксацией, а промежуток времени, в течение которого система возвращается в состояние равновесия, называется временем релаксации.
Чтобы процесс был равновесным, скорость изменения параметров системы dA/d 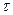 должна удовлетворять соотношению dA/d
должна удовлетворять соотношению dA/d 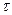 << Срел ~ ΔАрел/τрел, [9]
<< Срел ~ ΔАрел/τрел, [9]
где А - параметр, наиболее быстро изменяющийся в рассматриваемом процессе; срел— скорость изменения этого параметра в релаксационном процессе; 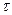 рел — время релаксации.
рел — время релаксации.
Рассмотрим, например, процесс сжатия газа в цилиндре. Если время смещения поршня от одного положения до другого существенно превышает время релаксации, то в процессе перемещения поршня давление и температура успеют выровняться по всему объему цилиндра. Это выравнивание обеспечивается непрерывным столкновением молекул, в результате чего подводимая от поршня к газу энергия достаточно быстро и равномерно распределяется между ними. Если последующие смещения поршня будут происходить аналогичным образом, то состояние системы в каждый момент времени будет практически равновесным. Таким образом, равновесный процесс состоит из непрерывного ряда последовательных состояний равновесия, поэтому в каждой его точке состояние термодинамической системы можно описать, уравнением состояния данного рабочего тела. Именно поэтому классическая термодинамика в своих исследованиях оперирует только равновесными процессами. Поскольку механические возмущения распространяются в газах со скоростью звука, процесс сжатия газа в цилиндре будет равновесным, если скорость перемещения поршня много меньше скорости звука.
Процессы, не удовлетворяющие условию dA/d 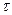 < C релак, протекают с нарушением равновесия, т, е. являются неравновесными.
< C релак, протекают с нарушением равновесия, т, е. являются неравновесными.
Дата добавления: 2015-08-14; просмотров: 1012;
