Применение закона эквивалентов.
Пример 5.Оксид марганца содержит 22,56% кислорода. Найти эквивалентную массу и валентность марганца в этом соединении. Составить формулу оксида.
Решение. Пусть масса оксида марганца равна 100г, тогда масса кислорода будет составлять 22,56 г. На основании закона эквивалентов можно составить следующую пропорцию:
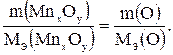 (1.3)
(1.3)
Примем Мэ(Мn) = А г/моль, тогда, согласно формулы (1.2), 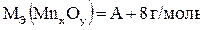 . Исходя из формулы (1.1),
. Исходя из формулы (1.1), 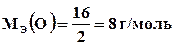 . Подставляя полученные значения в формулу (1.3) имеем:
. Подставляя полученные значения в формулу (1.3) имеем:
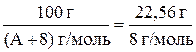 .
.
Решая уравнение относительно А получим: А = 27,5 г/моль.
Валентность марганца (по модулю совпадающую со степенью окисления) определим по формуле, связывающей молярную и эквивалентную массы элемента (1.1):
Мэ(Mn) = fэ (Mn )·М(Mn ) = М(Mn ) : В (Mn ),
откуда
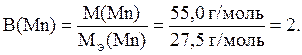
Так как в оксидах кислород двухвалентен, получаем следующую формулу оксида марганца: MnO.
6.Упражнения для самоконтроля направлены на закрепление следующих понятий:
Дата добавления: 2015-08-08; просмотров: 2431;
