Минералы
Под минералом понимают любое природное химическое соединение, образовавшееся при различных химических и физико-химических процессах в земной коре. К минералам относятся также индивидуализированные элементы, обнаруживаемые в земной коре (самородные металлы и металлоиды).
Минералы могут быть газообразные (природный газ), жидкие (нефть, ртуть, вода) и твердые (рудные минералы и др.). Количество природных соединений ограниченно; всего на настоящее время, известно около 4100 различных минералов. В большинстве случаев это твердые кристаллические химические соединения. Каждый год открывают в среднем около 50 новых минералов. В настоящее время многие минералы выращиваются искусственно.
Минералы распределяются в земной коре весьма неравномерно. В образовании горных пород основную роль играют только около 30 так называемых породообразующих минералов, из которых наиболее распространены полевые шпаты — натриевые, калиевые и кальциевые алюмосиликаты, составляющие 60% верхней части земной коры, амфиболы и пироксены — 17%, кварц — 12% и слюды — 3,8%.
Большинство других минералов присутствует в породах в незначительном количестве. Однако именно они имеют огромное значение для различных производств. В тоже время, такие добавочные (акцессорные) минералы оказывают большое влияние на свойства горных пород.
Минералы встречаются в виде одиночных хорошо образованных кристаллов и зерен, рассеянных в породе, поликристаллических плотных и землистых масс, натеков, налетов, корочек и желваков. Некоторые кристаллы, такие, как кварц, полевой шпат и сподумен, могут быть очень больших размеров, однако большинство минералов встречается в виде мелких кристаллов.
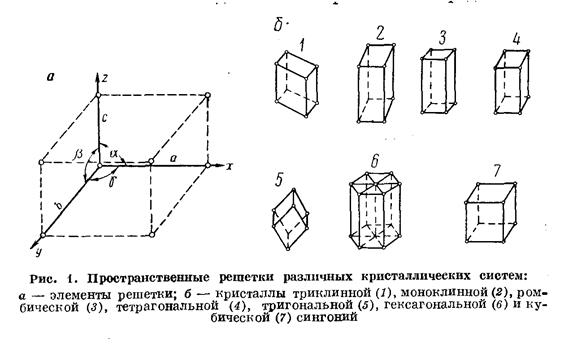
Минералы имеют свою пространственную решетку, соответствующую закону распределения вещества внутри кристалла. Известно семь типов (сингоний) кристаллических решеток, характеризуемых отношениями размеров кристаллических осей a, b, c (наименьших расстояний между узлами решетки в трех направлениях) и углами между ними α, β, γ (рис. 1):
первая сингония — триклинная(a ≠ b ≠ c; α ≠ β ≠ γ ≠ 90°);
вторая сингония — моноклинная (a ≠ b ≠ c; α =γ =90°; β ≠ 90°);
третья сингония — ромбическая (a ≠ b ≠ c; α =γ =β ≠ 90°);
четвертая сингония — тетрагональная (a = b ≠ c; α =γ =β =90°);
пятая сингония — тригональная (a = b = c; α =β =γ ≠ 90°);
шестая сингония — гексагональная (a = b ≠ c; α =β =90° γ =120° );
седьмая сингония - кубическая (a = b= c; α =β =γ =90°);
Физические свойства одиночного кристалла определяются его химическим составом и силами связей между частицами, входящими в пространственную решетку.
Существуют следующие типы связей – ионная (полярная), ковалентная (гомеополярная), металлическая, молекулярная.
Если взаимодействующие атомы имеют различную электроотрицательность, валентные электроны[1] от атома с меньшей электроотрицательностью переходят к атому с большей электроотрицательностью. В результате образуется ионная, или полярная, связь, обусловленная кулоновскими силами взаимодействия. Характерными представителями минералов с ионным типом являются галит КС1 и сильвин КС1.
В случае если соединяющиеся атомы имеют равные или между собой близкие значения электроотрицательности, то связывающие их электроны располагаются симметрично по отношению к ядрам этих атомов. Возникает ковалентная[2], или гомеополярная, связь, которую имеют, например, кварц и алмаз; минералы, обладающие такой связью, характеризуются большой твердостью и высокой температурой плавления.
В узлах решетки металлов находятся лишь положительные ионы[3]. Валентные электроны отделены от своих атомов и легко могут переходить от одного иона к другому; такого типа связи называются металлическими, их имеют, например, самородные золото и медь.
Если решетка кристалла образуется не атомами, а нейтральными молекулами, то связь между ними обуславливается электростатическими силами притяжения, возникающими вследствие поляризации взаимодействующих молекул; такие связи называются молекулярнымии по величине меньше предыдущих.
Свойства поликристаллических агрегатов наряду со свойствами составляющих кристаллов также зависят от сил сцепления между кристаллами. Эти силы обычно слабее внутрикристаллических и близки по величине к молекулярным.
Кристаллы анизотропны; их свойства зависят от направления, в котором производится измерение.
В агрегатах кристаллы обычно не ориентированы, располагаются беспорядочно, поэтому минеральные агрегаты в целом почти изотропны. Они имеют различную макроструктуру, определяющую их свойства. Макроструктура характеризуется размерами, формой кристаллов и их взаимным расположением. Широко распространены зернистые, лучистые, волокнистые, болитовые и другие минеральные агрегаты.
Характерным признаком некоторых минералов является спайность — способность раскалываться по плоским блестящим поверхностям. Явление спайности — следствие наличия в минералах направлений с ослабленным сцеплением частиц. Весьма развита спайность, например, у слюды. Агрегаты, сложенные такими минералами, анизотропны.
По химическому составу минералы принято делить на следующие группы:
самородные элементы (золото, серебро, мышьяк, сера, сурьма, алмаз);
сульфиды(халькозин Сu2S, сфалерит ZnS, киноварь HgS, пирит FеS2);
окислы (куприт Сu2О, корунд А12O3, гематит Fе2O3, кварц SiO2);
силикаты (оливин, тальк, мусковит, биотит, серпентин, каолинит, калиевые полевые шпаты );
соли кислородных кислот — сульфаты, вольфраматы, карбонаты и т. д. (ангидрид СаSO4, барит ВаSO4, шеелит СаWO4, кальцит СаСО3);
галоидные соединения (флюорит СаF2, галитNаС1, сильвин КС1).
Минералы подразделяются по генезису[4] на группы. Различают магматогенные минералы, образовавшиеся как непосредственно из магмы, так и из магматогенных горячих растворов, экзогенные (осадочные) минералы, возникшие вблизи поверхности Земли при участии агентов выветривания, и метаморфические минералы, образовавшиеся на глубине в результате изменения других минералов.
Часто один и тот же минерал может образовываться в различных условиях. Например, слюда может быть магматогенной и метаморфической.
Дата добавления: 2015-08-08; просмотров: 1174;
