Понижение давления насыщенного пара растворителя над раствором. Закон Рауля.
ЛЕКЦИЯ
Коллигативные свойства растворов
Свойства растворов, которые зависят от концентрации и практически не зависят от природы растворенных веществ, называют коллигативными. Общие свойства растворов изучают на примере разбавленных растворов.
Наиболее простые уравнения получены для описания свойств разбавленных растворов неэлектролитов. Характерной особенностью растворов неэлектролитов является отсутствие в них заряженных частиц – ионов.
Понижение давления насыщенного пара растворителя над раствором. Закон Рауля.
Давление насыщенного пара любого чистого вещества при данной температуре постоянно и определяется природой этого вещества. Насыщенный пар находится в равновесии с жидкостью, на примере воды:
H2O(ж) 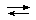 H2O(пар) .
H2O(пар) .
Растворение в воде какого-либо вещества приводит к уменьшению концентрации воды в жидкой фазе, смещению равновесия в сторону конденсации воды и понижению концентрации паров воды. Если растворенное вещество нелетучее, концентрацией паров воды определяется давление насыщенного пара над раствором. Таким образом, давление насыщенного пара над раствором снижается. Соответствующая количественная зависимость подчиняется закону Рауля:
относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного нелетучего вещества.
Математическое выражение закона Рауля:
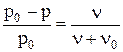 ,
,
где 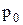 и p ‑ давление насыщенного пара растворителя над
и p ‑ давление насыщенного пара растворителя над
чистым растворителем и раствором;
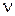 и
и 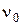 ‑ количество растворенного вещества и растворителя.
‑ количество растворенного вещества и растворителя.
Для растворов электролитов в математическое выражение закона Рауля вводят поправочный множитель 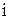 - изотонический коэффициент:
- изотонический коэффициент:
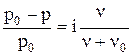 .
.
Изотонический коэффициент равен отношению числа находящихся в растворе частиц (недиссоциированных молекул и ионов) к общему числу молекул растворенного вещества.
Изотонический коэффициент связан со степенью диссоциации соотношением:
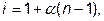
где a - степень диссоциации, доли ед.,
n –число ионов, на которые диссоциирует электролит
(K2SO4 = 2K+ + SO42-, n = 3).
Дата добавления: 2015-08-08; просмотров: 2351;
