Химические свойства металлов. Главным признаком металлов как химических веществ является их способность терять электроны при взаимодействии с другими атомами
Главным признаком металлов как химических веществ является их способность терять электроны при взаимодействии с другими атомами, проявляя восстановительные свойства. В соответствии с восстановительной способностью получен ряд химической активности металлов: от Li до Al – активные, от Al до H+ – средней активности. Металлы, расположенные в ряду активности справа от водорода, называют малоактивными, или благородными.
1. Металлы реагируют с простыми веществами - неметаллами: со фтором – почти все металлы, продукты реакции называют фториды; хлором – почти все, продукты реакции называют хлориды; кислородом – многие металлы, продукты реакции называют оксиды; серой – многие при нагревании, продукты называют сульфидами; водородом, азотом – щелочные и щелочно - земельные металлы, продукты реакции гидриды и нитриды соответственно.
2. С водой взаимодействуют, вытесняя водород из воды, только те металлы, значение электродных потенциалов которых значительно меньше, чем у воды (–0,41 В).
2Li + 2H2O ® 2LiOH + H2
Металлы, расположенные между магнием и свинцом, пассивируют протекание реакции с образованием защитной оксидной пленки.
3. Металлы, стоящие в ряду электродных потенциалов левее водорода, взаимодействуют с хлороводородной кислотой. Окислителем в хлороводородной кислоте является ион водорода H+:
Fe + 2HCl ® FeCl2 + H2
4. Металлы взаимодействуют с серной кислотой. В разбавленной, так же как в хлороводородной кислоте, окислителем является ион водорода:
Ме + Н2SO4 (разб.) ® MeSO4 + H2
В концентрированной серной кислоте в роли окислителя выступает атом серы 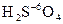 . В этом случае становится возможным окисление некоторых благородных металлов.
. В этом случае становится возможным окисление некоторых благородных металлов.
3Cu + 4H2SO4 ® 3CuSO4 + S¯ + 4H2O
4. Более сильным окислителем, чем серная кислота, является азотная. В разбавленной азотной кислоте окислителем выступает атом азота 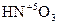 . Продуктами восстановления азота могут являться NH4NO3, N2, N2O, NO. Концентрированная азотная кислота обычно восстанавливается до NO2.
. Продуктами восстановления азота могут являться NH4NO3, N2, N2O, NO. Концентрированная азотная кислота обычно восстанавливается до NO2.
5. Действие растворов щелочей возможно только на «амфотерные» металлы Be, Al, Zn, Sn, Pb. Причем реакция протекает в две стадии: реакция металла с водой с образованием гидроксида и водорода, реакция гидроксида металла со щелочью.
Контрольные вопросы:
1. Дайте определение металлической связи.
2. Перечислите общие свойства металлов, которые могут проявляться одновременно.
3. Какие группы выделяют в ряду активности металлов?
4. Какие металлы проявляют «амфотерные» свойства?
5. В чем отличие действия концентрированной и разбавленной серной кислоты на металлы?
Список рекомендуемой литературы:
1. Глинка Н.Л. Общая химия: учеб. пособие для вузов / Н.Л. Глинка. - М.: КНОРУС, 2009. - С. 545 - 568.
2. Коровин Н.В. Общая химия: учебник для технических направл. и спец. вузов - 7-е изд., испр. - М.: Высшая школа, 2006. - С. 341 - 348.
Ю.Н. Биглова, М.А.Молявко
Дата добавления: 2015-08-08; просмотров: 994;
