Правило Гунда: при данном значении l (т.е. в пределах определенного подуровня) электроны располагаются таким образом, чтобы суммарный спин был максимальным.
Если, например, в трех р-ячейках атома азота необходимо распределить три электрона, то они будут располагаться каждый в отдельной ячейке, т.е. размещаться на трех разных р-орбиталях:

В этом случае суммарный спин равен 3/2, поскольку его проекция равна тl = +1/2 + 1/2 + 1/2 = 3/2. Эти же три электрона не могут быть расположены таким образом:
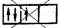
потому что тогда проекция суммарного спина тl = +1/2–1/2+1/2 = 1/2. По этой же причине именно так, как приведено выше, расположены электроны в атомах углерода, азота и кислорода.
Первые 18 электронов заполняют следующие орбитали: 1s22s22p63s23p6. Казалось бы, что девятнадцатый электрон атома калия должен попасть на подуровень 3d, которому соответствуют п = 3 и l = 2. Однако на самом деле валентный электрон атома калия располагается на орбитали 4s. Дальнейшее заполнение оболочек после 18-го элемента происходит не в такой последовательности, как в двух первых периодах. Электроны в атомах располагаются в соответствии с принципом Паули и правилом Гунда, но так, чтобы их энергия была наименьшей.
Принцип наименьшей энергии: в атоме каждый электрон располагается так, чтобы его энергия была минимальной (что отвечает наибольшей связи его с ядром).
Энергия электрона в основном определяется главным квантовым числом п и побочным квантовым числом l, поэтому сначала заполняются те подуровни, для которых сумма значений квантовых чисел п и l является наименьшей. Например, энергия электрона на подуровне 4s меньше, чем на подуровне 3d, так как в первом случае п+ l = 4+0 =4, а во втором п+ l = 3+2 = 5 и т.д.
В.М. Клечковский (1961 г.) сформулировал общее положение, гласящее, что электрон занимает в основном состоянии уровень не с минимальным возможным значением п, а с наименьшим значением суммы п + l.
Дата добавления: 2015-08-08; просмотров: 1280;
