Изопроцессы в термодинамике. Энергия Гельмгольца
1. Изотермический– Т= const
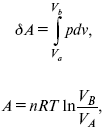
так как
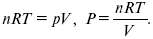
2. Изохорный– V = const
δА = 0,
δА = pdυ = 0,
δQ = dU + pdυ,
δQ = CvdT.
3. Изобарный– P = const
δА = pdυ,
A = pV2 – pV1.
4. Адиабатический– δQ = 0
1) δA = –dU,
A = –CV(T2 – T1), T2 > T1;
2) pdδ= –CvdT,
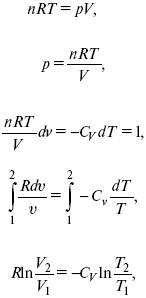
действие, обратное логарифму – потенцирование
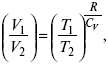
Уравнение первого закона термодинамики в калорических коэффициентах
δQ = ldυ + CVdT,
где l– коэффициент изотермического расширения;
CV – теплоемкость при постоянном объеме.
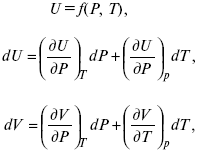
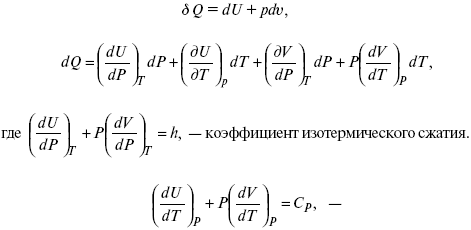
теплоемкость при const давлении,
δQ = hdP + CpdT ,
δQ = χdP + ψdυ.
Связь между функциями CPи CV
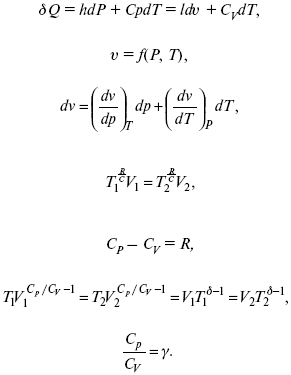
Дата добавления: 2015-08-08; просмотров: 835;
