Терминология. Стволовая кроветворная клетка морфологически сходна с малым лимфоцитом, способна к дифференцировке во все клетки крови (рис
Стволовая кроветворная клетка морфологически сходна с малым лимфоцитом, способна к дифференцировке во все клетки крови (рис. 6-17). Такая клетка была названа CFU-blast (CFU — Colony Forming Unit, колониеобразующая единица). Стволовая кроветворная клетка может выходить в кровоток; постоянно, но редко делится, причём с относительно неизменной частотой (т.е. нечувствительна к запросу). Относительный покой — определяющая характеристика cтволовой кроветворной клетки, тогда как её потомки обладают высокой пролиферативной активностью. Вступление стволовой кроветворной клетки в клеточный цикл регулируется молекулярным «переключателем» — ингибитором циклин-зависимой киназы p21cip1/waf1 (p21). При делении стволовой кроветворной клетки дочерние клетки выбирают симметричное или асимметричное деление, т.е. или остаются стволовыми кроветворными клетками, или дифференцируются в полипотентные потомки с их последующей дифференцировкой в клетки крови, или подвергаются апоптозу. Образующиеся при делении клетки дифференцируются в пролиферирующие полипотентные клетки–предшественницы (колониеобразующие единицы) лимфоцитопоэза (CFU‑Ly) и миелопоэза (CFU-GEMM). В результате деления CFU‑Ly и CFU-GEMM их потомки остаются полипотентными или дифференцируются в один из нескольких типов коммитированных унипотентных клеток (колониеобразующих единиц), также активно пролиферирующих, но дифференцирующихся только в одном направлении.
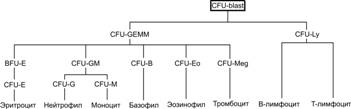
Рис. 6-17. Схема гемопоэза. CFU-blast —стволовая кроветворная клетка; CFU-GEMM — полипотентная клетка–предшественница миелопоэза; CFU‑Ly — полипотентная клетка–предшественница лимфоцитопоэза; CFU‑GM — полипотентная клетка–предшественница гранулоцитов и моноцитов. Унипотентные предшественники: BFU-E и CFU-E — эритроцитов; CFU-Eo — эозинофилов; CFU‑M — моноцитов; CFU‑G — нейтрофилов, CFU‑B — базофилов, CFU‑Meg — тромбоцитов. [17]
Участие остеобластов в формировании ниши стволовой кроветворной клетки. Давно замечено, что новые центры кроветворения возникают в непосредственной близости от кости. Остеобласты в области эндоста влияют на процесс кроветворения. Остеобласт взаимодействует со стволовой кроветворной клеткой и вместе со стромальной клеткой костного мозга участвует в создании ниши стволовой кроветворной клетки (рис. 6-18). Остеобласты продуцируют многочисленные факторы, контролирующие выживание, пролиферацию и созревание стволовой кроветворной клетки.
Цитокины. Остеобласты продуцируют и выделяют цитокины, которые влияют на стволовую кроветворную клетку (рис. 6-19). Среди них колиниестимулирующий фактор гранулоцитов (G-CSF), колониестимулирующий фактор моноцитов (M-CSF), колониестимулирующий фактор гранулоцитов и моноцитов (GM-CSF), ИЛ1, ИЛ6, ИЛ7, лейкоз-ингибирующий фактор (LIF), остеопротегерин, остеопротегерин лиганд (RANKL), стромальный фактор (SDF-1), TNF, VEGF.
Молекулы адгезии остеобластов и стволовых кроветворных клеток: CD34, CD44, CD164, молекула адгезии клеток 1 (ICAM-1) и ICAM-3, связанный с функцией лимфоцитов антигены-1 и -3 (LFA-1, LFA-3), PECAM-1, очень поздние антигены 4 и 5 (VLA-4, VLA-5). В качестве молекул адгезии могут выступать цитокины, связанные с матриксом, такие как интерлейкин 3 (ИЛ3), Flt-лиганд, колониестимулирующий фактор гранулоцитов и моноцитов (GM-CSF), фактор стволовых клеток (SCF), трансформирующий фактор роста 1 (TGF1).

Рис. 6-18. Участие остеобластов в поддержании стволовой кроветворной клетки. Ниша стволовой кроветворной клетки образована несколькими представителями системы стромальных клеток костного мозга, все из которых происходят из общей мезенхимной клетки. Остеобласты и их предшественники в эндосте играют важную роль в создании ниши, участвуя в поддержании, пролиферации и созревании стволовой кроветворной клетки. В этой нише остеобласты взаимодействуют с клетками-партнерами с участием молекул адгезии, цитокинов и факторов роста. Все эти сигналы регулируют функцию остеобластов и могут быть подразделены на механические, системные (например, паратиреоидный гормон) и местные (например, белки BMP, Ang-1). В костном мозге в поддержании ниши стволовой кроветворной клетки участвуют реципрокные взаимодействия между стволовыми клетками, остеобластами и другими клетками стромы костного мозга. [52]
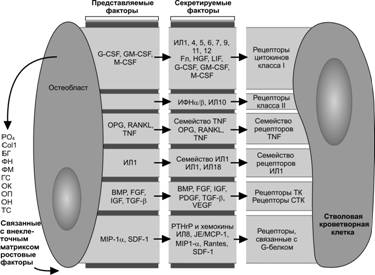
Рис. 6-19. Связанные с поверхностью остеобласта и секретируемые молекулярные факторы, влияющие на стволовую кроветворную клетку. Остеобласт выделяет щелочную фосфатазу, бигликан (БГ), морфогенетические белки кости (BMP), коллаген типа I (ColI), факторы роста фибробластов (FGF), Flt-лиганд (Fл), фибромодулин (ФМ), фибронектин (ФН), фактор роста гепатоцитов (HGF), гепаринсульфат протеогликан (ГС), инсулиноподобные факторы роста (IGF), интерферон (ИФН), JE/белок хемотаксиса моноцитов 1, матриксный белок Gla(MGP), остеокальцин (ОК), онкостатин М, остеопонтин (ОП), тромбоцитарный фактор роста (PDGF), фактор тромбоцитов 4 (PDGF4), рецептор серин/треонинкиназы (СТК), рецептор тирозинкиназы (ТК), тромбоспондин (ТС). [52]
Стволовая кроветворная клетка может выходить из периферического кровотока и заселять разные органы,например, сердце, головной мозг, печень, скелетные мышцы. В зависимости от микроокружения стволовая кроветворная клетка может дифференцироваться в миобласты скелетной и сердечной мышечной ткани, гепатоциты, эндотелиальные клетки сосудов, нейроны, олигодендроциты, астроциты. Стволовая кроветворная экспрессирует характерный комплекс маркёров, которые позволяют выделить её из пуповинной крови и плаценты, костного мозга, периферической крови. Такими маркёрами являются CD34, CD31, CD59, Sca-1, Thy1, Oct-4, Nanog, SOX2, FGF4.
Трансплантация стволовых кроветворных клеток производится при лечении ряда врождённых заболеваний крови (апластическая анемия, -талассемия, серповидноклеточная анемия, лимфопролиферативный синдром, связанный с Х-хромосомой и др.) и гемобластозов (лимфом и лейкемий), при химиотерапии рака для поддержания пула полипотентных кроветворных клеток красного костного мозга.
Получение стволовых клеток
Пуповинная кровь и плацента. Возможно получить несколько миллионов стволовых клеток, что недостаточно для трансплантации взрослому (требуется 7–10 миллионов клеток на 1 кг массы тела), но может быть адекватным для трансплантации детям.
Красный костный мозг. В среднем удаётся выделить одну стволовую кроветворную клетку на каждые 100 000 полученных аспирацией клеток.
Периферическая кровь. Инъекция G-CSF за несколько дней до забора крови стимулирует выход стволовых кроветворных клеток из костного мозга в кровь.
Унипотентные коммитированные клетки способны к дифференцировке в один клеточный тип, пролиферируют и в присутствии факторов роста дифференцируются в клетки–предшественницы. Унипотентные клетки морфологически не отличаются от стволовых клеток. Программирование клетки на определённый путь дифференцировки (коммитирование), по-видимому, происходит случайным образом.
Клетки–предшественницы — клетки одной линии, различающиеся морфологически и образующиеся последовательно в каждой линии, начинающейся с коммитированной унипотентной клетки и завершающейся формированием зрелой клетки крови.
Дата добавления: 2015-07-07; просмотров: 1565;
