Определение и классификация коррозионных процессов
КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
Определение и классификация коррозионных процессов
Коррозия — это разрушение металла в результате его физико-химического взаимодействия с окружающей средой. При этом металлы окисляются и образуются продукты, состав которых зависит от условий коррозии.
Коррозия самопроизвольный процесс и соответственно протекает с уменьшением энергии Гиббса системы. Химическая энергия реакции коррозионного разрушения металлов выделяется в виде теплоты и рассеивается в окружающем пространстве. Коррозия приводит к большим потерям в результате разрушения трубопроводов, цистерн, металлических частей машин, корпусов судов, морских сооружений и т. п. Безвозвратные потери металлов от коррозии составляют до15% от ежегодного их выпуска. Замена прокорродировавшего котла или конденсатора на большой теплоэлектростанции может нанести энергосистеме существенный ущерб. Кроме того, к убыткам от коррозии можно отнести также стоимость потерянного продукта, например, масла, газа, воды из системы с прокорродированными трубами или антифриза через прокорродировавший радиатор. Выброс природного Газа и других пожаро- и взрывоопасных веществ через отверстия, образованные вследствие коррозии, может привести к пожарам и даже к мощным взрывам с огромными и материальными потерями и даже с человеческими жертвами, как, например, в случае Башкирской трагедии.
В целом потери народного хозяйства от коррозии исчисляются миллиардами рублей ежегодно. Цель борьбы с коррозией — это сохранение ресурсов металлов, мировые запасы которых ограничены. Изучение коррозии и разработка методов защиты металлов от нее представляют теоретический интерес и имеют большое народнохозяйственное значение.
По механизму протекания коррозионного процесса, зависящему ; от характера внешней среды, с которой взаимодействует металл, различают химическую и электрохимическую коррозию.
Химическая коррозия характерна для сред, не проводящих электрический ток. При химической коррозии происходит прямое гетерогенное взаимодействие металла с окислителем окружающей среды. По условиям протекания коррозионного процесса различают: а) газовую коррозию - в газах и парах без конденсации влаги на поверхности металла, обычно при высоких температурах. Примером газовой коррозии может служить окисление металла кислородом воздуха при высоких температурах; б) коррозию в неэлектролитах — агрессивных органических жидкостях, таких, как сернистая нефть и др.
Электрохимическая коррозия характерна для сред, имеющих ионную проводимость. При электрохимической коррозии процесс взаимодействия металла с окислителем включает анодное Растворение металла и катодное восстановление окислителя. Электрохимическая коррозия может протекать: а) в электролитах — входных растворах солей, кислот, щелочей, в морской воде; б) в атмосфере любого влажного газа; в) в почве.
Особым видом электрохимической коррозии следует считать коррозию за счет внешнего электрического тока. В качестве пример0й подобного вида разрушений можно привести коррозию трубопроводов с токопроводящими жидкостями, нерастворимых анодов в электрохимических ваннах, подземных металлических сооружений.
Хотя механизм протекания коррозионного процесса в разных условиях различен, по характеру разрушения поверхности металла коррозию можно разделить на равномерную и местную (рисунок 15.1).
Равномерная, иди общая, коррозия распределяется более или менее равномерно по всей поверхности металла, в то время как местная коррозия сосредоточена на отдельных участках и проявляется в виде точек, язв или пятен. Местная коррозия, как правило, более опасна чем равномерная коррозия, так как процесс проникает на большую глубину. Особыми видами коррозии являются межкристаллическая коррозия (коррозия по границам зерен), избирательная коррозия (растворение одного из компонентов сплава) и коррозионное растрескивание (коррозия при одновременном воздействии химических реагентов и высоких механических напряжений). Данные виды коррозии особенно опасны, так как могут привести к быстрому разрушению машины, аппарата или конструкции.
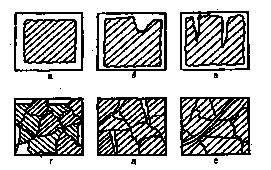
а – равномерное, б – местное, в – точечное, г – избирательное,
д – межкристаллическое, е - транскристаллическое
Рисунок 15.1 – Виды коррозионных разрушений
Скорость коррозии выражают несколькими способами. Наиболее часто пользуются массовым и глубинным показателями коррозии. Первый из них дает потерю массы (в граммах или килограммах) за единицу времени (секунду? час, сутки, год), отнесенную к единице площади (квадратный метр) испытуемого образца. Глубинный показатель коррозии выражается уменьшением толщины металла в единицу времени. Скорость электрохимической коррозии можно также выразить величиной тока, приходящегося на единицу площади металла.
Итак, самопроизвольное разрушение металла (коррозия) приносит большие убытки. Коррозия протекает по различным механизмам и вызывает разные виды разрушений.
Дата добавления: 2015-08-08; просмотров: 3032;
