II. Титрование по методу нейтрализации.
| т.э |
| b |
| c |
| a |

|
|
a) NaOH + HCl = NaCl + H2O; H+ + OH- = H2O
Отрезок a-b: подвижные ионы Н+ заменяются на менее подвижные ионы Na+, электропроводность падает.
Отрезок b-c: избыток HСl ведет к резкому возрастанию электропроводности.
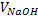
|
| т.э |
| b |
| c |
| a |
|
б) CH3COOH + NaOH = CH3COONa + H2O
Отрезок a-b: малоподвижные ионы СН3СОО- заменяются на более подвижные ионы ОН-, электропроводность растет.
Отрезок b-c: избыток NaOH ведет к более резкому возрастанию электропроводности.
Так как соль подвергается гидролизу, то на практике получается почти прямая линия.
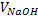
|
| V2 т.э |
| V1 т.э |
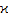
|
в) Титрование смеси кислот НСl и CH3COOH – NaOH
Первой оттитровывается сильная кислота (HCl) – V1.
Второй слабая (CH3COOH) – (V2 – V1).
Преимущества кондуктометрического титрования:
Ø Можно титровать мутные и окрашенные растворы
Ø Более точно устанавливается точка эквивалентности
Ø Можно анализировать смесь веществ
Ø Относительная ошибка определений (0,1-2)%
Дата добавления: 2015-08-04; просмотров: 1382;
