Контроль качества драже.
Контролируют качество по внешнему виду на основании осмотра 20 драже. Испытание распадаемости проводят ежегодно согласно фармакопейной статье «Таблетки» (приложение 3). Время распадания не должно превышать 30 мин.
Растворение. Определение распадаемости таблеток не дает информации о высвобождении лекарственных веществ из распавшейся лекарственной формы и не позволяет сделать заключение об их доступности.
Более надежным контролирующим методом является «тест-растворение». При этом анализируется количество лекарственного вещества (в интервалах времени), диффундирующего из целых или распавшихся таблеток в растворяющую жидкость (вода, 0,1 н раствор кислоты хлористоводородной, 0,1 н раствор натрия гидроксида, буферные растворы, искусственные пищеварительные соки и др.)
Покрытие таблеток оболочками
Покрытие таблеток оболочками имеет многостороннее значение и следующие цели:
1) защита таблеток от экстремальных факторов внешней среды (ударов, истирания и др.);
2) защита от воздействий окружающей среды (свет, влага, кислород и углекислота воздуха);
3) маскировка неприятного вкуса и запаха, содержащихся в таблетках лекарственных веществ;
4) защита от окрашивающей способности лекарственных веществ, содержащихся в таблетках (например, таблетки активированного угля);5) защита содержащихся в таблетках лекарственных веществ от кислой реакции желудочного сока;
6) защита слизистой рта, пищевода и желудка от раздражающего действия лекарственных веществ;
7) локализация терапевтического действия лекарственных веществ в определенном отделе желудочно-кишечного тракта;
8) предотвращение нарушений процессов пищеварения в желудке, возможных при нейтрализации желудочного сока лекарственными веществами основного характера;
9) пролонгирование терапевтического действия лекарственных веществ в таблетках;
10) преодоление несовместимости различных веществ, находящихся в одной таблетке, путем введения их в состав оболочки и ядра;
11) улучшение товарного вида таблеток и удобства их применения.
При покрытии таблеток оболочками применяют различные вспомогательные вещества, условно подразделяющиеся на следующие группы: адгезивы, обеспечивающие прилипание
материалов покрытия к ядру и друг к другу (сахарный сироп, ПВП, КМЦ, МЦ, АФЦ, ОПМЦ, ЭЦ, ПЭГ и др.): структурные вещества, создающие каркасы (сахар, магния оксид, кальция оксид, тальк, магния карбонат основной); пластификаторы, которые придают покрытиям свойства пластичности (растительные масла, МЦ, ПВП, КМЦ, твины и др.); гидрофобизаторы, придающие покрытиям свойства влагостойкости (аэросил, шеллак, полиакриловые смолы, зеин ); красители, служащие для улучшения внешнего вида или для обозначения терапевтической группы веществ: (тропеолин 00, тартразин, кислотный красный 2С, индигокармин и др.); корригенты, придающие покрытию приятный вкус (сахар, лимонная кислота, какао, ванилин и др.).
Применяется более 50 наименований пленкообразователей.
Таблеточные покрытия в зависимости от их состава и способа нанесения разделяют на следующие группы:
1. Прессованные (или сухие) покрытия.
2. Пленочные покрытия.
3. Дражированные покрытия (нанесение сахарной оболочки). Прессованные покрытия
Нанесение оболочек прессованием («сухие» покрытия) осуществляют с помощью таблеточных машин типа «Драйкота» английской фирмы «Манести» или отечественной РТМ-24 Д. Машина представляет собой сдвоенный агрегат, состоящий из двух роторов
На первом роторе обычным способом прессуются таблетки- ядра двояковыпуклой формы, передающиеся с помощью специально транспортирующего устройства на второй ротор, где наносится покрытие. Схема нанесения покрытия прессованием такова. Сначала происходит заполнение гнезда матрицы порцией гранулята, необходимого для образования нижней части (половины) покрытия, затем на гранулят по специальным направлениям с первого ротора подается таблетка-ядро, на которую наносится покрытие. После фиксации таблетки точно по центру гнезда матрицы нижний пуансон несколько опускается, после чего отпускаетсяверхний пуансон, слегка впрессовывающий таблетку-ядро в находящуюся под ней порцию гранулята, или создает над таблеткой пространство для заполнения второй порции гранулята. После подачи этой порции происходит окончательное формирование покрытия путем прессования (одновременно верхним и нижним пуансоном). На заключительной стадии осуществляется выталкивание таблетки, покрытой оболочкой.
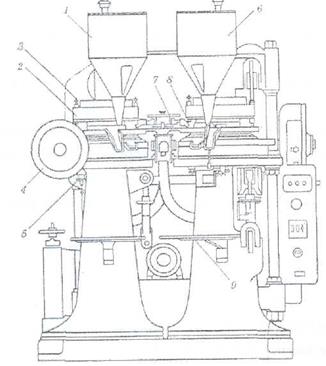
Рис.. Таблеточная машина «Драйкота»:
/ — бункер с гранулятом; 2 — ротор; 3 — пуансон; 4 — ролик; 5 — регулировочный винт; 6 — бункер с массой для оболочки; 7,8 — передатчики; 9 — емкость для готовых таблеток
Производительность машины 10 500 таблеток в час.
К недостаткам этого метода следует отнести: значительный расход материала для покрытия, увеличение массы и размера таблеток, неравномерность оболочки по толщине, трудность переработки брака, нарушение центровки ядра, значительная пористость покрытий, приводящая к увеличению объема в результате набухания таблеток-ядер при поглощении ими влаги из воздуха, проникающего сквозь поры оболочки. При этом происходит образование трещин в прессованной оболочке или даже ее отслаивание.
Главным преимуществом данного метода покрытия является исключение использования в технологии растворителей. Поэтому прессованные покрытия рациональны для таблеток гигроскопичных и чувствительных к воздействию влаги веществ (антибиотики).
С целью пролонгации эффекта действующего вещества его вводят в состав как ядра, так и покрытия. Покрытие быстро распадается в желудке (начальная доза), а ядро (таблетка) распадается постепенно, поддерживая определенную постоянную концентрацию вещества в организме. Этот метод позволяет преодолеть несовместимость находящихся в одной таблетке различных веществ, вводя их в состав оболочки и ядра.
Пленочные покрытия ^ Пленочным покрытием называется тонкая (порядка 0,05-— 0,2 мм) оболочка, образующаяна таблетке после высыхания нанесенного на ее поверхность раствора пленкообразующего вещества. Они имеют следующие преимущества:
1. Возможность избирательной растворимости таблеток в желудке или кишечнике.
2. Регулирование скорости адсорбции лекарственных веществ.
3. Возможность совмещения в одной лекарственной форме несовместимых лекарственных веществ.
4. Сохранение физических, химических и механических свойств ядер таблеток при нанесении пленочных покрытий.
5. Сохранение первоначальных геометрических параметров таблеток, их формы, маркировки, фирменных обозначений.
6. Уменьшение массы объема пленочного покрытия по сравнению с дражировочным.
7. Возможность автоматизации процесса покрытия, интенсификации производства и сокращение производственных площадей.
В зависимости от растворимости пленочные покрытия разделяют на следующие группы:
а) водорастворимые;
б) растворимые в желудочном соке;
в) кишечно-растворимые;
г) нерастворимые.
Водорастворимые покрытия и покрытия, растворимые в желудке. Водорастворимые покрытия улучшают внешний вид таблеток, корригируют их вкус и запах, защищают от механических повреждений. Покрытия, растворимые в желудке, предохраняют таблетки от воздействия влаги воздуха; они разрушаются в организме в течение 10—30 мин.
Для получения водорастворимых покрытий полиэтиленоксид и поливинилпирролидон наносят на таблетки в виде 20—30% растворов в 50—90% этиловом или изопропиловом спиртах, метилцеллюлозу и натриевую соль карбоксиметилцеллюлозы — в виде 4 — 7% водных растворов.
Покрытия, растворимые в желудочном соке, представляют бензиламино- и диэтиламинобензилцеллюлозой, п-аминобензоатом, сахарозой, глюкозой, фруктозой, маннитом, винилпиридином, зеином и желатином.
Кишечно-растворимые покрытия. Кишечно-растворимые покрытия защищают лекарственное вещество, содержащееся в таблетке, от действия кислой реакции желудочного сока, предохраняет слизистую желудка от раздражающего действия некоторых лекарств, локализируют лекарственное вещество в кишечнике, пролонгируя в определенной степени его действие. Кишечно-растворимые покрытия обладают также более выраженным, чем у перечисленных выше групп покрытий влагозащитным эффектом.
Процесс растворения энтеросолюбильных оболочек в организме обусловлен воздействием на них комплекса ферментов и различных солюбилизирующих веществ, содержащихся в кишечном соке.
Для получения кишечно-растворимых покрытий в качестве пленкообразователей используются высокомолекулярные соединения со свойствами полиэлектролитов с большимчислом карбоксилвных групп. Они диссоциируют в нейтральной или щелочной среде с образованием нерастворимых солей. Применяются природные вещества: шеллак, карнаубский воск, казеин, кератин, парафин, церезин, спермацет, цетиловый спирт, а также синтетические продукты,стеариновая кислота в сочетании с жирами и желчными кислотами, бутилстеарат, фталаты декстрина, моносукцинаты ацетил-, метилфталилцеллюлозы.
Чаще всего для получения кишечно-растворимых покрытий используют ацетил фтали л целлюлозу, как вещество, наиболее устойчивое квоздействию желудочного сока. Перечисленные пленкообразователи наносят на таблетки в виде растворов в этиловом, изопропиловом спирте, ацетоне или в смесях указанных растворителей. Для получения окрашенных оболочек п растворы добавляют пигменты и красители.
Кишечно-растворимые покрытия выдерживают (2—4 ч и более) воздействия желудочного сока, что позволяет таким таблеткам в неизмененном виде пройти через желудок; в кишечном же соке они распадаются в течение 1 ч, обеспечивая высвобождение лекарственного вещества в кишечнике.
Нерастворимые покрытия. Основное назначение покрытий данного типа — защита таблетки от механического повреждения и от воздействия атмосферной влаги, устранение неприятного запаха и вкуса лекарственного вещества, пролонгирование его действия. К покрытиям относят этилцеллюлозу, монолаурат полиэтиленсорбита, поверхностно-активные вещества и др. Механизм высвобождения лекарственного вещества из таблеток с нерастворимыми оболочками заключается в следующем. После поступления таблетки в желудочно-кишечный тракт пищеварительные соки проникают в нее сквозь микропоры оболочки и вызывают или растворение содержимого таблетки, или ее набухание. В первом случае растворенные вещества диффундируют через пленку в обратном направлении — в сторону желудочно-кишечного тракта под влиянием разности концентраций, во втором — происходит разрыв оболочки за счет увеличения объема таблетки, после чего лекарственное вещество высвобождается обычным образом.
Способы нанесения пленочных покрытий
Существуют 3 способа нанесения пленочных покрытий на таблетки:
1. Погружение в раствор пленкообразующего вещества.
2. Наслаивание в дражировочном котле.
3. Получение покрытия во взвешенном слое.
Первый способ основан на погружении таблеток поочередно, то одной, то другой стороной в покрывающий раствор. Таблетки фиксируются с помощью вакуума на металлическом перфорированном листе специальной машины, производительность которой составляет 5—8 тыс. покрытых оболочками таблеток в час. Машины подобного типа выпускаются фирмой «Артур Колтон». Этот способ достаточно сложен и пригоден лишь для нанесения на таблетки вязких, но не слишком клейких растворов. В настоящее время в связи с недостаточно высокой производительностью он применяется редко.
Наиболее широко применяется способ нанесения пленочных покрытий в дражировочном котле. Для нанесения покрытия двояковыпуклые таблетки помещают в дражировочныйкотел, в период работы он вращается со скоростью 20—25 об/мин. Перед началом процесса покрытия с поверхности таблеток сильной воздушной струей удаляется пыль. Покрывающий раствор вводят в котел путем периодического разбрызгивания с помощью установленных у отверстия котла форсунок. Для сушки оболочек таблетки обдувают в котле воздушной струей.
Для нанесения .покрытия в псевдоожиженном слое используется установка, конструкция которой почти не отличается от установки типа СГ, применяемой для получения гранулята. Форсунки для разбрызгивания покрывающего раствора устанавливаются в нижней или верхней части рабочей камеры аппарата. Определенное количество таблеток помещают в рабочую камеру, включают вентилятор (компрессор), и под действием образующегося воздушного потока масса таблеток переводится в псевдоожиженное состояние, после чего с определенной скоростью в камеру подается покрывающий раствор. Скорость поступления раствора определяется его вязкостью, скорость движения воздуха в аппарате — размером камеры и количеством находящихся в ней таблеток. Продолжительность процесса нанесения покрытия зависит от необходимой толщины оболочки и колеблется от 15 до 45 мин. После прекращения пульверизации раствора скорость движения воздуха слегка увеличивают, при этом образование пленочной оболочки происходит наиболее эффективно, процесс сушки покрытия значительно сокращается по сравнению с остальными способами.
Пленочное покрытие незначительно увеличивает массу таблеток. Благодаря применению летучих органических растворителей, исключается длительная стадия сушки оболочек. Продолжительность процесса нанесения пленочного покрытия составляет 2—4 ч.
Пленочные покрытия можно наносить не только на таблетки, но и на гранулы или на частицы порошкообразного материала.
Основным недостатком нанесения пленочных покрытий в промышленных масштабах является значительное увеличение концентрации паров, зачастую ядовитых и огнеопасных органических растворителей в помещениях цехов, что требует принятия соответствующих мер противопожарной безопасности, установке мощной приточно-вытяжнои вентиляции и безопасности работников.
В производстве для нанесения пленочных покрытий на основе органических растворителей применяют установки УПТ-25 и УЗЦ-25.
Установка замкнутого цикла УЗЦ-25 способна улавливать пары растворителей, регенерировать их и снова пускать в производство. На этой установке производят таблетки ПАСК — Na (натриевая соль парааминосалициловой кислоты) с пленочным кишечно-растворимым покрытием.
Дражированные покрытия. Дражированное (от франц. dragee — нанесение сахарной оболочки) Основное назначение оболочек — защита таблеток от внешних воздействий, маскировка неприятного вкуса и запаха лекарственного вещества, улучшение внешнего вида таблеток. Иногда в состав оболочек добавляют вещества, защищающие таблетку от воздействия желудочного сока.
Создание дражированных оболочек осуществляется в дражировочных котлах1 илиобдукторах трех форм: шарообразной, эллипсоидной и грушевидной. Наиболее распространенная — эллипсоидная форма. Ее преимущества — в возможности большей загрузки таблетками и создании большего давления на них. Кроме того, в котлах такого типа создаются оптимальные вращательные движения дражир о ванных таблеток, ускоряющие и улучшающие условия нанесения оболочки.
Форма котла, степень его загрузки, скорость вращения, наклон котла к горизонтали, а также площадь поверхности дражированных таблеток значительно влияют на качество покрытия. Оптимальная скорость котла — 18—20 об/мин, угол наклона котла к горизонтали — 30—45°, оптимальная загрузка — 25—30% от объема котла.
Дражированная таблетка состоит из таблетки-ядра, содержащей лекарственное вещество, и покрытия, содержащего комплекс вспомогательных веществ.
Таблетка-ядро должна быть механически прочная. Это обусловлено действием на таблетку при дражировании четырех факторов:
— суммарная масса таблеток, зависящая от величины загрузки котла (с увеличением загрузки и скорости вращения котла возрастает возможность разрушения таблеток);
— свободное падение таблеток с верхней точки вращающегося котла на нижнюю (эта сила прямо пропорциональна массе таблеток и высоте, с которой они падают);
— кинетическая энергия вращающихся таблеток в котле (таблетка не просто произвольно падает, а создается вращательный момент, сила которого зависит от массы таблетки и скорости вращения котла);
— расклинивающий эффект жидкостей, применяемых при дражировании.
Таблетки, подлежащие дражированию, не должны иметь плоскую форму, чтобы избегнуть их слипания. Для дражирования рекомендуются два типа таблеток:
— со средним овалом поверхности, глубина кривизны составляет около 15% диаметра, высота по центру —- 25—30% диаметра (г - 0,75d);
— со стандартной кривизной поверхности (малый овал), глубина кривизны составляет 10% диаметра, высота по центру — не менее 25% диаметра таблетки (г - l,Id).
До 1975 г. на отечественных химико-фармацевтических заводах существовала технология покрытия таблеток методом сахарно-мучного дражирования. Стадии технологического процесса дражирования таблеток:
1. Обволакивание, или грунтовка.
2. Наслаивание, или накатка.
3. Сглаживание, или полировка.
4. Глянцовка.
Обволакивание, или грунтовка, состоит в том, что движущиеся таблетки в дражировочном котле увлажняют сахарным сиропом 64—70% концентрации и обсыпаются пшеничной мукой или же смесью ее с магния карбонатом основным. После обсыпки таблетки вращаются 25:—30 мин, после чего их сушат теплым воздухом (40—50 °С) в течение 30-—40 мин. Операции увлажнения таблеток, обсыпки, свободного вращения и сушки повторяют 2— 3 раза. Стадия обволакивания, в случае необходимости, применяется для изоляции таблетки-ядра от проникновения влаги, особенно в первые моменты увлажнения таблеток.
За стадией обволакивания следует стадия наслаивания, или накатки. Во всем технологическом цикле дражирования — это самая важная стадия, так как именно здесь происходит, в основном, образование всей оболочки.
На этой стадии одни заводы применяют сахарно-мучное тесто для наслаивания, другие — таблетки увлажняли сахарным сиропом и обсыпали магния карбонатом основным или же смесью его с пшеничной мукой в равных количествах. После одноразовой подачи сахарно-мучного теста таблеткам дают свободное вращение, перемешивая их в котле в течение 30-— 40 мин. Затем таблетки сушат теплым воздухом 20—30 мин. Операции подачи теста, свободного вращения, сушки таблеток повторяют многократно, до получения определенной массы таблеток.
За стадией наслаивания следует стадия сглаживания, или полировки, которую осуществляют с помощью сахарного сиропа с добавлением небольших количеств желатина (до 1%) и красителей. На этой стадии происходит удаление неровностей, шероховатостей.
Последней стадией процесса дражирования является стадия глянцевания, т. е. придания таблеткам блеска, товарного вида. Ее осуществляют двумя способами.
Применяя первый способ, готовят глянцовочную мастику следующего состава, %;
— воска пчелиного — 45;
— масла вазелинового— 45;
— талька — 10.
Глянцовочную мастику в количестве 0,05—0.06% руками наносят на вращающиеся теплые таблетки и дают свободное вращение таблеткам 30—40 мин. Затем таблетки обсыпают небольшим количеством талька для ускорения получения глянца.
Применяя второй способ, отполированные таблетки выгружают из котла и помещают в специальный котел, стенки которого покрыты воском. Включают вращение котла на 1,5—2 ч и таким образом получают глянец.
Сахар но-мучное дражирование имеет ряд существенных недостатков.
Исследования показали, что в процессе хранения в результате окислительных процессов и энзиматического расщепления белковых веществ в муке образуются свободные органические кислоты с выделением газообразных веществ, что ведет к прогорканию. Мука, входящая в состав покрытия, ухудшает его физико-механические свойства и часто ведет к растрескиванию покрытия.
Сахарно-мучное тесто, применяемое при дражировании, по своей консистенции негомогенно, и покрытие, получаемое на его основе, не имеет ровной однородной поверхности. Мучное тесто затрудняет возможность механизировать и автоматизировать процесс. Кроме того, сахарно-мучное дражирование характеризуется трудоемкостью и длительностью.
В связи с изложенным выше проф. П. Д. Пашневым (Харьков) разработан новый способ покрытия таблеток — суспензионный метод дражирования.
| Состав суспензии, %Сахар | 58,00 |
| Вода | 24,85 |
| Поливинилпирролидон | 0,75 |
| Аэросил | 1,00 |
| Магния карбонат зовной | 13,40 |
| Титана двуокись | 2,00 |
Сочетание сахара и воды представляет собой 70% сахарный сироп, являющийся носителем суспензии.
Поливинилпирролидон (ПВП) является высокомолекулярным соединением винилпирролидона. В растворе молекулы ПВП, присоединяясь друг к другу, образуют пространственную сетку. Молекулы сахара, растворенные в воде, оказываются заключенными в ячейки сетки.
В процессе сушки обрабатываемых таблеток вода, находящаяся в отдельных ячейках сетки, удаляется. Оставшийся в ячейках сетки сахар, кристаллизуясь, не имеет возможности соединяться в агломераты. Образуются мелкодисперсные кристаллы, обладающие меньшей хрупкостью и большей пластичностью.
Аэросил (аморфная двуокись кремния), применяемый в суспензии, является ее стабилизатором. Механизм стабилизации заключается в том, что на поверхности частичек аэросила имеются силаноловые группы, образующие с водой гель при помощи водородных мостиков. Образовавшийся гель препятствует седиментации взвешенных частиц. Магния карбонат основной — наполнитель. Титана диоксид — краситель (пигмент).
Стадии суспензионного метода дражирования таблеток.
1. Нанесение на таблетки покрытия из неокрашенной суспензии.
2. Нанесение на таблетки покрытия из окрашенной суспензии или окрашенного сиропа.
3. Глянцевание таблеток.
Суспензионное дражирование таблеток осуществляют как на обычных дражировочных котлах, так и на автоматических линиях фирм «Штенберг» (Германия) и «Пеллегрини» (Италия).
Технологический режим дражирования заключается в следующем,
В дражировочный котел загружают таблетки-ядра в количестве 25—30% от объема котла, предварительно обкатанных и обеспыленных. Включают привод котла и на вращающиеся таблетки подают 2—2,5% суспензии методом полива или же разбрызгивания с помощью форсунки. Таблеткам дают «раскататься» 4—5 мин. Угол наклона котла к горизонтали составляет 45°, скорость вращения — 20—25 об/мин. После чего таблетки сушат теплым воздухом 40—45 °С в течение 3—4 мин.
Операции подачи суспензии, обкатки и сушки повторяют многократно, до получения определенной массы таблеток.
О режиме нанесения окрашенного покрытия на основе окрашенной суспензии или окрашенного сиропа и глянцевании таблеток говорилось выше.Суспензионный метод покрытия таблеток оболочками позволил автоматизировать процесс, уменьшить трудозатраты, повысить производительность труда в 3—5 раз. Новая технология улучшила качество покрытых оболочками таблеток:
а) снизилась их средняя масса;
б) улучшен товарный вид:
в) повысилась стабильность покрытых оболочками таблеток — срок годности препаратов увеличился с 1 года до 4 лет;
г) исключен пищевой продукт — мука, приводившая к растрескиванию покрытия. Rp.: Acidi ascorbinici 0,2
Pyridoxini Hydrochloridi 0,05
Acidi nicotinici 0,02
Misce fiat pulv. D.t.d. N 20 S. По 1 пор; З раза в день.
Расчеты: Потери
Кислоты аскорбиновой 0,2*20=4,0 12мг*3-36 мг
Пиридоксина гидрохлорида 0,05*20=1,0 нет данных
Кислоты никотиновой 0,02*20=0.4 прописана в в соотношении 1/10 по отнош к
М общ= 5,4 N41=0,27 аскорб.к-те, поэтому расчеты не делаем.
Технология. В ступку № 4 помещаем 4,0 кислоты аскорбиновой, измельчаем, затирая
поры ступки. Так как соотношение 1:20 не превышено, в ступку вносим 0,4 кислоты
никотиновой, растираем, перемешиваем. Вносим 1,0 пиридоксина гидрохлорида,
растираем, перемешиваем. Смешивание и измельчение продолжаем до тех пор, пока на
расстоянии 25 см невооруженным глазом не будут видны отдельные частицы при
надавливании пестиком на смесь ингредиентов.
Дозирование. С помощью ручных весов и капсулоторки развешивают общую массу
порошка на дозы массой по 0,27 г числом 20, помещая на вощеные капсулы.
Стадия 4-— упаковка. Завертывают каждую дозу порошка в вощеную капсулу, капсулы
складывают по 3 и помещают в картонную коробку.
ппк
Acidi ascorbinici 0,2 Acidi nicotinici 0,02 Pyridoxini Hydrochloridi 0,05 Мобщ=5,4М1=0,27
Обязательные виды контроля: Органолептический, письменный, при отпуске. Этикетки: «Внутреннее» или «Порошок» «Беречь от детей», «Хранить в сухом месте» Сроки и усл. хр. 10 сут в сухом, защищ. от света месте при Тне выше 25С.
Требования, предъявляемые к порошкамВ Государственной фармакопее содержатся требования, предъявляемые к порошкам: сыпучесть, однородность, допустимые нормы отклонения в массе отдельных доз. цвет, вкус, запах, упаковка и оформление, соответствующие входящим в состав ингредиентам. Порошки должны быть однородными при рассмотрении невооруженным глазом, иметь размер частиц не более 0,16 мм (при отсутствии других указаний в частных статьях). Порошки, применяемые для лечения ран, поврежденной кожи и слизистых оболочек, а также порошки для новорожденных и детей до 1 года, должны быть стерильными и готовиться в асептических условиях.
Величина их частиц должна составлять 0,1 мм. В настоящее время фармацевтическая промышленность выпускает лекарственные вещества с размером кристаллов 70—1000 мкм. В связи с этим многие вещества требуют дополнительного измельчения в процессе изготовления порошков.
Контроль качества.
Его осуществляют на всех этапах деятельности специалиста.
Фармацевтическая экспертиза прописи рецепта (проверка совместимости, доз, норм единовременного отпуска и т.д.).
Контроль качества на стадиях изготовления (проверка однородности, сыпучести). В соответствии с ГФ измельченные порошки должны быть однородными, иметь размер частиц не более 0 16 мм. Если нет других указаний в соответствующих документах, однородность порошковой смеси проверяют визуально. Порошок собирают в центр ступки, надавливают пестиком, рассматривают невооруженным глазом на расстоянии 25 см при этом не должно быть отдельных частиц, блесток или вкраплений.
Контроль качества изготовленного препарата (ППК, органолептический контроль, отклонение в массе порошков, оформление, упаковка). Органолептически проверяют соответствия цвета, запаха смеси цвету и запаху входящих ингредиентов, заполнение капсул и др.
Контроль при отпуске. Проверяют соответствие упаковки, оформления, свойствам веществ препарата, правильность выписывания сигнатуры, соответствие номеров и фамилии больного на рецепте, этикетке, квитанции, сигнатуре, наличие номера препарата на упаковке.
В процессе изготовления сложных порошков в аптеках часто пользуются лекарственными полуфабрикатами — специальными внутриаптечными заготовками, представляющими собой смесь наиболее употребительных лекарственных веществ, подобранных в соотношениях, характерных для большинства рецептов.
Как1 и при производстве других лекарственных форм, использование таких препаратов существенно сокращает время, затрачиваемое на изготовление порошков, что способствует их более быстрому отпуску.
Состав полуфабрикатов утверждается контрольно-аналитическими учреждениями, имеющими на то полномочия.Лекарственные вещества в полуфабрикатах не должны реагировать одно с другим, полуфабрикаты должны иметь большие сроки хранения. Применение полуфабрикатов ускоряет процесс изготовления порошков, так как за один раз взвешивают смесь из 2 — 3 и более ингредиентов. Если рецептурная пропись полностью соответствует имеющемуся в аптеке составу полуфабриката, отвешивают необходимую на все дозы массу полуфабриката и затем ее дозируют.
Если пропись не соответствует составу полуфабриката в полной мере, добавляют недостающие ингредиенты с учетом соотношения ингредиентов в прописи и их физико-химических свойств.
После изготовления порошковой смеси фармацевт по памяти заполняет лицевую сторону ППК и передает помощнику фармацевта (фасовщику) для дозирования, фасовки, упаковки, оформления.
Необходимо помнить, что в виде полуфабрикатов приготавливают лишь такие лекарственные смеси, которые наиболее часто повторяются в рецептуре аптек и представляют собой (рациональные прописи с точки зрения их совместимости) сочетания лекарственных веществ, не изменяющиеся при хранении.
Наиболее распространенными являются следующие полуфабрикаты:
1) Glucosum 0,25 + Acidum ascorhinicum 0,05;
2) Zinci oxydum + Talcum + Bolus alba aa 0,05;
3) Dimedrolum 0,03 (0,05) + Saccharum 0,25;
4) Acidum acetylsalicylicum + Phenacetinumaa 0,01.
Приготовление полуфабрикатов, так же как и порошков, с их использованием производят по общим правилам технологии сложных порошков.
Все лекарственные формы для новорожденных и детей до 1 года, независимо от способа применения, должны изготовляться в аптеках в асептических условиях. Известно, что даже микроорганизмы низкой вирулентности могут вызвать серьезные заболевания, особенно у ослабленных новорожденных.
Лекарственные препараты для новорожденных должны быть стерильными, а препараты для детей до 1 года по микробиологической чистоте — соответствовать нормативу «Не более 50 бактерий и грибов суммарно в 1 г или 1 мл препарата при отсутствии Enterobacteriaceae, P. aeruginosa, S. aureus».
Порошки для внутреннего применения.. При этом в нарушение НД около 25 % порошков в аптеках изготавливают, измельчая таблетки (например, тавегил, энтеросептол, панангин, пентоксил и др.), что недопустимо из-за наличия наполнителей, стабилизаторов, красителей идругих добавок. .
Еще одной проблемой является необходимость изготовления порошков с использованием тритураций, учитывая малые дозировки выписанных лекарственных веществ (даже не сильнодействующих). Использование тритураций приводит к повышению микробной контаминации препарата из-за содержания глюкозы, являющихся хорошей средой для развития микроорганизмов.Порошки для внутреннего применения не являются оптимальной лекарственной формой (особенно для новорожденных), так как они, по сути, полуфабрикаты, которые при приеме растворяют или суспендируют. Часто добавляют корригенты домашнего изготовления (соки, сиропы, варенье и т.п.), что может привести к изменению фармакологического эффекта.
Наиболее часто встречающиеся порошки разрешено ввести во внутриаптечную заготовку Технология изготовления порошков для новорожденных и детей в возрасте до 1 года не отличается от общей технологии лекарственной формы «Порошки».
Таблица Прописи порошков для новорожденных и порошков для детей
| Состав | Срок хранения |
| Порошки для новорожденных | |
| Димедрол 0,001 или 0,002 Сахар (глюкоза) 0,2 | 90 сут*1 |
| фенобарбитал 0,002 или 0,005 Сахар (глюкоза) 0,2 | 90 сут*1 |
| Эуфиллин 0,003 Сахар 0,2 | 20 сут*1 |
| Порошки для детей | |
| Дибазол 0,003 (0,005—0,008) Сахар 0,2 | 90 сут*3 |
| Димедрол 0,005 Сахар (глюкоза) 0,1 | 90 сут*3 |
| Димедрол 0,005 Кальций глкжонат 0,25 Сахар (глюкоза) од | 1 год*3 |
| Кальций глюконат 0,05 Сахар (глюкоза) 0,2 | 1 год*3 |
| Кальций глюконат Сахар (глюкоза) поровну | 1 год*4 |
* Хранить в защищенном от света месте. *2 Запрещается замена на глюкозу. "Хранить в сухом и защищенном от света месте. *4 Хранить в сухом месте.
Вопрос 3. Fructus Rosae — плоды шиповника (Rosae fructus — шиповника плод)
В медицине используются представители:
секц. Rugosae Chrshan.: шиповник морщинистый (Rosa rugosa Thunb.);
секц. Cinnamomeae DC: шиповник майский (ш. коричный) — Rosa majaiis Herrm. (R. cinnamomea L), ш. иглистый (R. acicularis Lindl.), ш. даурский (Я. davurica Pall.), ш. Беггера (Я. beggeriana Schrenk), ш. Федченко (Я. fed-tschenkoana Regel), ш. кокандский (Я. kokanica (Regel) Regel ex Juz.);
секц. Caninae DC: ш. собачий (Я. canina L), ш. щитконосный (Я. corym-bifera Borkh.), ш. мелкоцветковый (Я. micrantha Borrer ex Smith), ш. песколюбивый (Я. psammophila Chrshan.),ш. войлочный (Я. tomentosa Smith), ш. зангезурский (Я. zangezura P. Ja-rosc.) и некоторые другие виды.
Химический состав. Плоды шиповника содержат кислоту аскорбиновую (от 0,2-1 % у низковитаминных видов и до 4-5 % у высоковитаминных), каротиноиды (в-каротин и др.) до 10мг%, токоферолы (витамин Е), флавоноиды (флавонолы — рутин, кемпферол; катехины;лейкоантоцианиди-ны; антоцианы), гидролизуемые и конденсированные дубильные вещества, органические кислоты — лимонная и яблочная (2-4 %), жирное масло, пектиновые вещества (до 14%), сахара (до 24 %), около 0.9 % свободных аминокислот (в основном аспарагиновой).
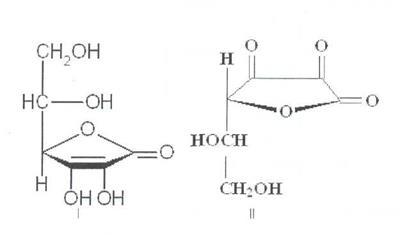
Заготовка, первичная обработка и сушка. Заготавливают зрелые плоды до заморозков, когда они приобретают оранжево-красную окраску, пока они твердые, так как мягкие плоды при сборе легко раздавливаются, при сушке в них уменьшается содержание витаминов. Оно снижается и после заморозков. Собирают плоды вручную в корзины или ведра, очищают от примеси листьев и поврежденных плодов. Сушат в сушилках при температуре 80-90 °С на металлических сетках, слоем 2-3 см, периодически перемешивая. После сушки отделяют чашелистики и удаляют изменившие окраску, подгоревшие плоды.
Стандартизация. Качество плодов шиповника регламентировано ГФХ1 и ВФС 42-185-72.
Числовые показатели. Цельное сырье. Кислоты аскорбиновой не менее 0,2 %; влаги не более 15 %; золы общей не более 3 %; примеси веточек, чашелистиков и плодоножек не более 2 %; почерневших, пригоревших, поврежденных вредителями и болезнями плодов не более 1 %; недозрелых плодов (от зеленой до желтой окраски) не более 5 %; измельченных плодов, в том числе орешков, проходящих сквозь сито с отверстиями диаметром 3 мм, не более 3 %; органической примеси не более 0,5 %, минеральной — не более 0,5 %.
Порошок. Кроме требований, предъявляемых к цельному сырью по содержанию кислоты аскорбиновой, общей золы и влажности, порошок должен соответствовать также следующим: частиц, не проходящих сквозь сито с отверстиями 2 мм, не более 15 %.
Для сырья, используемого для изготовления «Холосаса», «Каротолина» и сиропов. Органических кислот не менее 2,6 %: золы общей не более 4 %; почерневших, пригоревших,
поврежденных вредителями и болезнями плодов не более 3 % (остальные показатели такие же. как указано выше).
Количественное определение кислоты аскорбиновой проводят титриметрически (раствором 2,6-дихлор-фенилиндофенолятанатрия). Количественное определение суммы органических кислот проводят алкалиметрически. ( методика аналогичная, как для др. видов сырья:взятие навески, извлечение, очистка извлечения фильтрованием, методомТСХ, взятие аликвоты, колич опред с о ответствую щи методом).
Хранение. В хорошо проветриваемых помещениях. Срок годности 2 года.
Использование. Для приготовления настоев, сиропов, микстуры Траскова, витаминных и поливитаминных сборов, применяемых при гипо- и авитаминозе С и различных заболеваниях, сопровождающихся повышенной потребностью в кислоте аскорбиновой. Для получения богатых каротиноидами препаратов «Масло шиповника» и «Каротолин», применяемых как ран о заживляющие средства, а кроме того, для получения препарата «Холосас», содержащего органические кислоты, используемого как желчегонное средство.
Входит в состав ряда БАДов. Имеется также НД на «Плоды шиповника свежие» (ТУ 64-4-26-86).
Вопрос 4. Рецепт выписан верно. НЕО не регламентированы для инградиентов. Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности.
Билет 22. Вопрос 1. Chloramphenicol — хлорамфеникол (Левомицетин) ■
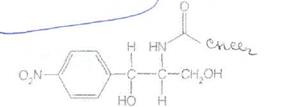
D-(-)-mpeo-\ -п-нитрофенил-2-дихлорацетиламинопропандиол-1,3
Белый или белый со слабым желтовато-зеленоватым оттенком кристаллический порошок без запаха. Т. пл. 149-153°С. Удельное вращение от +18 до +21° (5%-ныйраствор в этаноле)
Хлорамфеникол мало растворим в воде, эфире, хлороформе, растворим в этилацетате. В этаноле хлорамфеникол легко растворим. Подлинность хлорамфеникола подтверждают по УФ-спектру0,002%-ного водного раствора, который в области 220-400 нм имеет максимум поглощения при 278 нм и минимум при 237 нм. ФС рекомендует устанавливать величину удельного показателя поглощения при длине волны 278 нм (от 290 до 305).
Определение подлинности. Левомицетин.Реакция гидролиза в щелочной среде лежит в зснове испытания подлинности хлорамфеникола и его производных. При нагревании в гечение 1-2 мин с 15%-ным раствором гидроксида натрия хлорамфеникол и хлорамфениколастеарат приобретают желтое окрашивание, переходящее в красно-оранжевое. Одновременно ощущается запах аммиака. Фильтрат после подкисления азотной кислотой дает характерную реакцию на хлориды. Это позволяет подтвердить наличие в молекуле хлорамфеникола нитрофенильного радикала, аминогруппы и ковалентно связанного атома хлора, поскольку при щелочном гидролизе образуется «основание» хлорамфеникола, переходящее в аци-форму, выделяется аммиак и натриевая соль глиоксиловой кислоты:
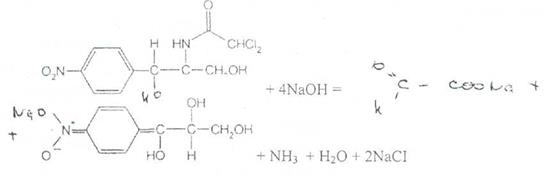
NaCI + AgNO3 -> AgCI + NaNO3
AgCI + 2NH3 • H2O -> [Ag(NH3)2]CI + 2H2O
Известны многочисленные способы идентификации и количественного определения, основанные на предварительном гидрировании (цинковой пылью в кислой среде)
нитрофуппы в молекуле хлорамфеникола до аминогруппы. Одновременно отщепляются
о атомы хлора: «

Образовавшийся 1 -п-аминофенил-2-ацетиламинопропандиол-1,3 диазотируют и превращают в азокраситель, сочетая с d-нафтолом. а-нафтиламином или другим амином или фенолом. Например, в результате азосочетания с d-нафтолом образуется азокраситель красного цвета: 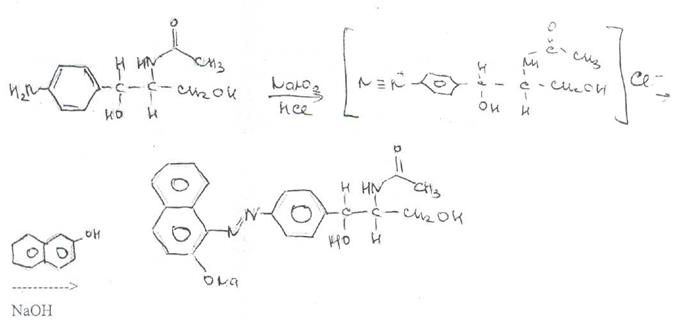
Хлорамфеникол, подобно эфедрину, за счет наличия в молекуле спиртового гидроксила и ""' вторичной алифатической аминогруппы может образовывать окрашенные комплексные соединения с солями тяжелых металлов. С раствором сульфата меди образуется синий осадок, который растворяется в н-бутаноле, окрашивая его слой в фиолетовый цвет.
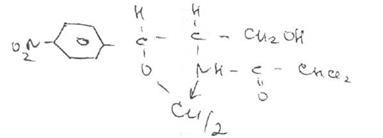
Для идентификации лекарственных веществ, содержащих в молекуле нитрогруппу, используют также испытание, основанное на последовательном гидрировании (цинком в хлороводородной кислоте) до ароматического амина с последующей его конденсацией с диметиламинобензальдегидом до образования окрашенной соли основания Шиффа. Хлорамфеникол в этих условиях приобретает ярко-оранжевое окрашивание.
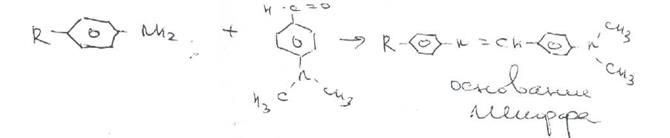
Наличие исходных и промежуточных продуктов синтеза в хлорамфениколе устанавливают методом ТСХ на пластинках Силуфол УФ-254 в системе хлороформ-метанол-вода (90:10:1). На хроматограмме допускается наличие на более трёх посторонних пятен, каждое из которых не должно превышать пятно свидетеля по величине и интенсивности (не более 0,5% каждой примеси).Количественное определение хлорамфеникола по ФС выполняют нитритометрическим методом после предварительного гидрирования в кислой среде цинковой пылью:
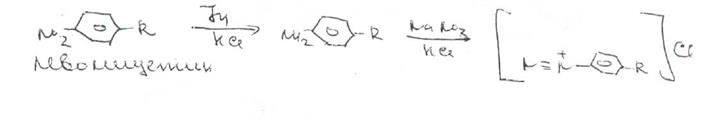
Содержание хлорамфеникола определяют иобратным бромид-броматометрическим методом. Однако этому, как и в случае нитритометрии, должна предшествовать стадия гидрирования нитрогруппы в аминогруппу с помощью цинковой пыли и хлороводородной кислоты при нагревании на кипящей водяной бане. Остаток цинка удаляют фильтрованием и к фильтрату добавляют избыток 0,1 М раствора бромата калия в присутствии бромидов. Количество непрореагировавшего тнтранта устанавливают с помощью иодида калия*'Л Выделившийся иод оттитровывают 0.1 М раствором тиосульфата натрия.
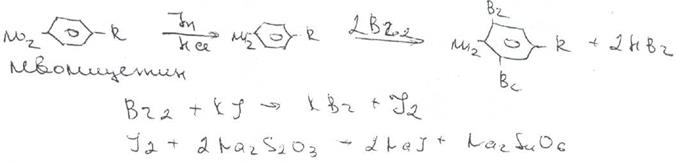
Хлорамфеникол хранят по списку Б. в хорошо укупоренной таре в склянках оранжевого стекла— в сухом защищенном от света месте при комнатной температуре.
Хлорамфеникол — антибиотик широкого спектра действия. Его применяют для лечения брюшного *тифа, паратифов, дизентерии, бруцеллеза, коклюша, пневмонии, различных инфекционных заболеваний. Он легко всасывается из желудочно-кишечного трак-^J сохраняя при этом свою активность. Это позволяет использовать хлорамфеникол для назначения внутрь обычно в дозах 0,5 г 3-4 раза в сутки.
Вопрос 2. Пролонгаторы.
Вспомогательные вещества, увеличивающие время нахождения лекарственных средств в организме, называются пролонгаторами. У лекарственных средств пролонгированного действия увеличена продолжительность действия.
При быстром выведении лекарственных веществ из организма или быстром разрушении в нем а/б, витаминов, гормонов и др. возникает необходимость частого введения лекарственных веществ, что приводит кизменению концентрации их в организме и обусловливает нежелательные побочные явления (аллергические реакции, раздражение и т.п.). Необходимо создание лекарственных препаратов, однократный прием которых, сохраняя бы в организме в течение длительного времени терапевтически активнуюконцентрацию лекарственного вещества, в том числе поступление лекарственного вещества с заданной скоростью.
Пролонгирующим компонентам, помимо требований, предъявляемых к вспомогательным веществам, следует отнести и поддержание оптимального уровня лекарственного вещества в организме, отсутствие резких колебаний его концентрации. Максимум концентрации лекарственного вещества в крови прямо пропорционально введенной дозе, скорости всасывания и обратно пропорционально скорости выделения вещества из организма.
Существуют различные технологические методы пролонгирования ЛП: повышение вязкости дисперсионной среды (заключение лекарственного вещества в гель); заключение лекарственного вещества в пленочные оболочки; суспендирование растворимых лекарственных веществ; создание глазных лекарственных пленок вместо растворов и др.
Наиболее предпочтительным является заключение лекарственного вещества в гель или использование в качестве дисперсионной среды неводных растворителей (ПЭО - 400, масла и др.). В качестве геля для пролонгированных ЛП чаще используют растворы ВМС различной концентрации, что позволяет регулировать время пролонгирования. К таким веществам относятся МЦ, КМЦ и натрий КМЦ (1%), ПВП, коллаген и др. ВМС. (пример - глазные капли в виде 10% раствора сульфацил - натрия, пролонгированные 1% МЦ).
При изготовлении таблеток пролонгированного действия лекарственное вещество вводят как в ядро, так и в состав покрытия. При этом покрытие получают из гранул легко распадающихся в желудке, а ядро готовят на основе гранулята, не распадающегося в желудочном соке. Такое прессованное покрытие после приема таблетки быстро разрушается и освобождает лекарственное вещество (доза называется начальной), а затем медленно распадается таблетка (ядро), поддерживая постоянную концентрацию вещества в организме.
Прессованные покрытия
Нанесение оболочек прессованием («сухие» покрытия) осуществляют с помощью таблеточных машин типа «Драйкота» английской фирмы «Манести» или отечественной РТМ-24 Д. Машина представляет собой сдвоенный агрегат, состоящий из двух роторов
На первом роторе обычным способом прессуются таблетки- ядра двояковыпуклой формы, передающиеся с помощью специально транспортирующего устройства на второй ротор, где наносится покрытие. Схема нанесения покрытия прессованием такова. Сначала происходит заполнение гнезда матрицы порцией гранулята, необходимого для образования нижней части (половины) покрытия, затем на гранулят по специальным направлениям с первого ротора подается таблетка-ядро, на которую наносится покрытие. После фиксации таблетки точно по центру гнезда матрицы нижний пуансон несколько опускается, после чего отпускается верхний пуансон, слегка впрессовывающий таблетку-ядро в находящуюся под ней порцию гранулята, или создает над таблеткой пространство для заполнения второй порции гранулята. После подачи этой порции происходит окончательное формирование покрытия путем прессования (одновременно верхним и нижним пуансоном). На заключительной стадии осуществляется выталкивание таблетки, покрытой оболочкой. 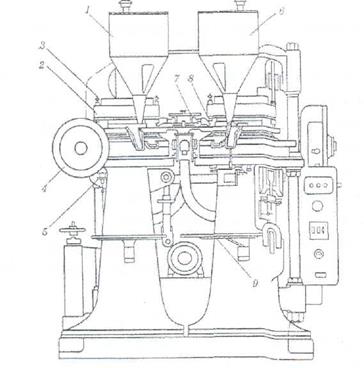
гис.iаилетоиная машина <удраикота»:
/ — бункер с гранулятом; 2 ■— ротор: 3 — пуансон; 4 — ролик; 5 — регулировочный винт; 6 — бункер с массой для оболочки; 7,8 — передатчики; 9 — емкость для готовых таблеток
Производительность машины 10 500 таблеток в час.
К недостаткам этого метода следует отнести: значительный расход материала для покрытия, увеличение массы и размера таблеток, неравномерность оболочки по толщине, трудность переработки брака, Нарушение центровки ядра, значительная пористость покрытий, приводящая к увеличению объема в результате набухания таблеток-ядер при поглощении ими влаги из воздуха, проникающего сквозь поры оболочки. При этом происходит образование трещин в прессованной оболочке или даже ее отслаивание.
Главным преимуществом данного метода покрытия является исключение использования в технологии растворителей. Поэтому прессованные покрытия рациональны для таблеток гигроскопичных и чувствительныхк воздействию влаги веществ (антибиотики).
С целью пролонгации эффекта действующего вещества его вводят в состав как ядра, так и покрытия. Покрытие быстро распадается в желудке (начальная доза), а ядро (таблетка) распадается постепенно, поддерживая определенную постоянную концентрацию вещества в организме. Этот метод позволяет преодолеть несовместимость находящихся в одной таблетке различных веществ, вводя йх в состав оболочки и ядра, у ( МНОГОСЛОЙНЫЕ ТАБЛЕТКИ
Многослойные таблетки позволяют сочетать вещества несовместимые по физико-химическим свойствам, пролонгировать действие лекарственных веществ, регулировать последовательность их всасывания в определенные промежутки времени.
Изготовление многослойных таблеток, каждый слой которых содержит заданные лекарственные вещества, требует прежде всего точной послойной дозировки в отдельности, поэтому конструкцией машин для изготовления слоистых таблеток поедусмотоена точнаядозировка каждого слоя. Для изготовления слоистых таблеток применяют таблеточные машины с многократной засыпкой гранулята. Лекарственные вещества, предназначенные для различных слоев, подаются в питатель машины из отдельного бункера. Обычно каждый гранулят имеет определенную окраску в целях лучшего визуального контроля, граница каждого слоя таблетки должна быть четко выражена, а боковая поверхность — блестящей, для этого требуется спрессовать каждый слой в отдельности. Различными зарубежными фирмами выпускаются модели РТМ для получения слоистых таблеток. Фирма « В. Фетте» (ФРГ) выпускает машину РТМ типа P11/S для получения трехслойных таблеток. Под-прессовка каждого слоя в отдельности обеспечивается введением на верхнем копире машины двух механизмов предварительного прессования, а третий слой, следовательно и таблетка в целом, окончательно формируется роликами давления.
КАРКАСНЫЕ ТАБЛЕТКИ
Для получения каркасных таблеток используют вспомогательные вещества, образующие непрерывную сетчатую структуру (матрицу), в которую включено (инкорпорировано) лекарственное вещество. Такая таблетка не распадается в желудочно-кишечном тракте. В зависимости от природы матрицы она может набухать и медленно растворяться или сохранять свою геометрическую форму в течение всего пребывания в организме и выводиться неизмененной в виде пористой массы, в которой поры заполнены жидкостью.
Каркасные таблетки относятся к пролонгированным препаратам поддерживающего действия. Лекарственное вещество из них высвобождается путем вымывания. При этом скорость его высвобождения не зависит ни от содержания ферментов в окружающей среде, ни от величины ее рН и остается достаточно постоянной по мере прохождения таблетки герез желудочно-кишечный тракт. Скорость высвобождения лекарственного вещества определяют такие факторы, как природа вспомогательных и растворимость лекарственных веществ, соотношение лекарственного и образующего матрицу веществ, пористость таблетки и способ ее получения. Вспомогательные вещества, используемые для образования матриц, подразделяют на гидрофильные, гидрофобные, инертные и неорганические.
Для получения гидрофильных матриц применяют набухающие полимеры (гидроколлоиды): гидроксипропил целлюлозу, гидроксипропилметилцеллюлозу, гидроксиэтил метил целлюлозу, 2-оксиэтилметакрилат, метилметакрилат, винилпирролидон и др.
Гидрофобные (липидные) матрьщы получают из натуральных восков (например, карнаубского воска) или из синтетических моно-. ди- и триглицеридов — эфиров кислот миристиновой, пальмитиновой и стеариновой, гидрированных растительных масел, высших жирных спиртов и др.
Инертные матрицы образованы нерастворимыми полимерами, такими как этилцеллюлоза. полиэтилен, полиметилметакрилат, сополимеры метилметакрилата и алкилакрилатов и др. Для создания каналов в слое полимера, нерастворимого в воде, в состав композиции добавляют водорастворимые вещества (ПЭГ, ПВП, лактоза, пектин и др.). Вымываясь из каркаса таблетки, они создают условия для постепенного выделениямолекул лекарственного вещества. Широко применяется также смесь полимера, чаще всего этилцеллюлозы с мелкодисперсным неорганическим веществом (тальк, бентонит, кизельгур и др.)- Порошок неорганических веществ разрыхляет полимерный слой и также создает внутри таблетки каналы, в которых осуществляется диффузия жидкости и соответственно молекул лекарственного вещества.
Для получения неорганических матриц используют нетоксичные нерастворимые вещества: кальций фосфат двухзамещенный, кальция сульфат, бария сульфат, аэросил и др.
Каркасные таблетки получают прямым прессованием смеси лекарственных и вспомогательных веществ, прессованием микрогранул или микрокапсул лекарственных веществ, а также таблетированием гранулята, приготовленного с использованием полимера.
Перспективным методом в технологии каркасных таблеток является получение твердых дисперсных систем (ТДС) лекарственных веществ в полимерах. Рекомендовано использование твердой дисперсии лекарственных веществ (фенобарбитал, никотинамид, кислота никотиновая и др.) в полиэтилене, полиметакрилате и др. с введением в композиции ПВП, ПЭГ. Лекарственные вещества смешивают в смесителе с порошками полимера и других добавок. Из смеси прессуют таблетки. Время высвобождения лекарственного вещества из такого полимерного каркаса составляет около 8 ч.
Твердую дисперсию лекарственного вещества в полимере (ЭЦ и смеси ЭЦ с оксипропилметилцеллюлозой) получают растворением лекарственного вещества в органическом растворителе вместе с полимером и последующего гранулирования смеси по мере испарения растворителя. Получают также гранулы из смеси лекарственных веществ с солью жирных кислот (магния стеарат. алюминия пальмиат и др.) и водорастворимого полимера (ПВП, оксипропилцеллюло-зы и др.). Гранулы смешивают с порошком ЭЦ и прессуют в таблетки. Для приготовления антигистаминной композиции пролонгированного действия на основе мебедрола (в-диметиламиноэтилового эфира орто-метилбензгидрола гидрохлорида) рекомендованы ЭЦ, кальция стеарат и кальция сульфат. При изменении их содержания в таблетке время высвобождения лекарственного вещества можно варьировать от 8 до 20 ч.
При построении каркаса из гидрофильных полимеров рекомендован следующий способ: порошок полимера впитывает лекарственное вещество, растворенное в изотоническом солевом растворе, высушивается и используется для приготовления таблеток.
Замедление диффузии молекул лекарственного вещества достигается путем включения его в сетку полимер-полимерного комплекса, который образуется за счет взаимодействия между функциональными группами двух макромолекул. Для этой цели рекомендовано использование ПВП и сшитой кислоты полиакриловой («Carbopol»). На их основе предложено готовить таблетки продленного действия с применением многих лекарственных веществ. Однако эти таблетки характеризуются быстрым высвобождением лекарственного вещества в начальный период времени с постепенным более медленным его выделением в последующие часы. С целью достижения более равномерного выделения лекарственного вещества предложено покрывать таблетку пленкой из ЭЦ.Приготовление мазей с антибиотиками. Мази с антибиотиками готовят по правилам технологии мазей в асептических условиях. При отсутствии указания врача в качестве основы используют: Вазелин 60,0 г Ланолин безводный 40,0 г
Компоненты сплавляют, фильтруют в расплавленном состоянии и стерилизуют при 150° С в течение 1 ч..
Из-за быстрой инактивации антибиотиков, введенных в мазь в виде водного раствора, их растирают со стерильным вазелиновым маслом или стерильной основой, т. е. вводят по типу суспензий.
Мази (unguenta) представляют собой мягкую лекарственную форму, которая предназначена для наружного применения (для нанесения на кожу, раны и слизистые оболочки) и состоит из основы и равномерно распределенных в ней лекарственных веществ. Кроме того, в мази могут быть введены консерванты, поверхности о-активные вещества (ПАВ), стабилизаторы и другие вспомогательные ингредиенты, разрешенные к медицинскому применению. При комнатной температуре мази, как правило, сохраняют свою форму, при повышении температуры окружающей среды превращаются густые жидкости. По дисперсологической классификации мази относятся к свободным всесторонне дисперсным бесформенным системам с упруговязкоплатичной дисперсионной средой. К мазям предъявляют следующие требования:
1) мази должны иметь мягкую консистенцию для удобства их нанесения и образования на обрабатываемой поверхности ровной сплошной пленки;
2) лекарственные вещества в мазях должны быть максимально измельчены и равномерно распределены по всей массе для достижения необходимого терапевтического эффекта иточности дозирования лекарственного вещества;
3) мази не должны содержать грубых включений;
4) при хранении и применении состав мазей изменяться не должен.
Дата добавления: 2015-08-04; просмотров: 3924;
