Российской Федерации об охране здоровья граждан и в порядке, определенном настоящей Инструкцией.
Рецепт выписан правильно. Адонизид - список Б. Хранят изолированно от др. в герметичной таре, наполненной доверху, в темном и прохладном месте.
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности, а для ЛС, взаимодействующих с пищей, времени их употребления относительно приема пищи (до. во время, после еды).
Микстура хранится в аптеке при Т не выше 25С в течение 10 сут.
Лекарственное растительное сырье храпят в сухом, хорошо вентилируемом помещении в хорошо закрытой таре.
Вторая часть квитанции с указанием номера лекарства, вида ЛФ, фамилии больного, даты и времени изготовления лекарства, его стоимости выдается на руки заказчику.
Третья часть квитанции содержит два одинаковых номера: первый с указанием «приготовил», «проверил», «отпустил» наклеивается на рецепт, второй — на упаковку отпускаемого лекарства. По этим номерам изготовленные лекарства располагаются на вертушках на рабочем месте провизора по отпуску лекарств. Отпуск изготовленного аптекой лекарства производится по квитанции, номер которой должен совпадать с номером, наклеенным на упаковку лекарства и на оборотную сторону рецепта. .
Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Растворы хранятся в теч. 10 дней в защищ. от света месте при Т не выше 35С. мазь хранится в теч 10 дней в прох. защищ. от света месте.
ч. Билет №1_3^опрос 1. ^Производное барбитуровой кислоты Barbitalum-natrium —барбитал-натрий (веронал)
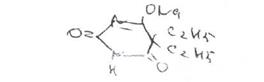
Ь,э-диэтилбарбитуровая кислота
Белый кристаллический порошок без запаха. Т. пл. 189-192°С, гигроскопичен, ле растворим в воде и этаноле, практически нерастворимы в эфире. Водные раствс натриевых солей барбитуратов имеют щелочную реакцию (рН 9,0 — 11.0).
Подлинность барбитуратов можно установить по ИК-спектрам. ИК-спектры, снятые по прессования в таблетках с бромидом калия в области 4000-400 см-1, должны иметь пол] :овпадение полос поглощения с прилагаемым к ФС рисунком спектра или со спектр сравнения.
УФ-спектры барбитуратов в области 220-280 нм имеют максимумы и миниму поглощения, используемые для идентификации. Раствор барбитала-натримя в этаноле по> цобавления буферного раствора с рН 10 имеет максимум поглощения при 240 нм и mhhhv — при 224 нм.
Для испытания барбитуратов и их натриевых солей используют химические реакц основанные на соде- и комплексообразовании с солями тяжелых металлов, сплавлении щелочами, окислении, нейтрализации натриевых солей, обнаружении ионов нат] Кислотные свойства
Вследствие лактам-лактимной таутомерии барбитураты являются слабыми кислота или солями слабых кислот. При образовании солевой формы отрицательный за] делокализуется с образванием амбидентного иона, так как образующаяся система более годна энергетически:
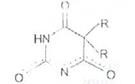
ьароитураьы, ооладая свойствами lNH-кислот, вступают в реакции комплексоооразоват с солями тяжелых металлов (Со2+, Cu2+, Ag2+).
Все барбитураты и их натриевые соли образуют с ионом кобальта комплексы! соединения, окрашенные в сине-фиолетовый цвет (в присутствии хлорида кальция). 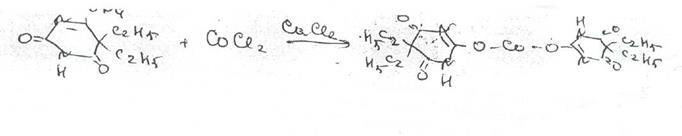
Цветная реакция с раствором сульфата меди (II) Наблюдается синее окрашивание и осадок красно-сиреневого цвета
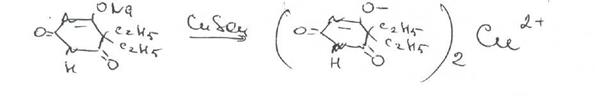
Для идентификации барбитуратов могут быть использованы реакции образования моно- и дизамещенных комплексов с солями меди (II) в присутствии пиридина. Комплексы имеют
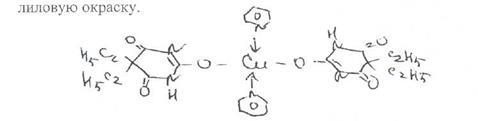
При взаимодействии с ионами серебра происходит образование однозамещенных (растворимых в воде) и двузамещенных (нерастворимых в воде) солей серебра. В присутствии карбоната натрия барбитураты образуют вначале натриевую соль, затем олнозамешенную серебряную:
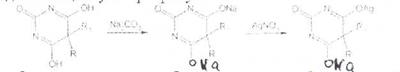
Однозамещенная серебряная соль при добавлении избытка нитрата серебра превращается в нерастворимую двузамещенную серебряную соль:

Ьароитураты могут оыть обнаружены с помощью общих цветных реакции на производные пиримидина, основанных на их окислении. При взаимодействии с концентрированной серной кислотой и 1-2 каплями раствора дихромата калия появляется стойкое зеленое окрашивание. Если вместо дихромата калия взять раствор ванадата аммония, то после нагревания на водяной бане раствор приобретает травянисто-зеленое окрашивание, переходящее в голубое. Присплавлении барбитурата с резорцином и концентрированной серной кислотой, последующем охлаждении и подщелачивании раствором гидроксида натрия возникает зеленая флуоресценция.
Р-ция конденсации с альдегидами. При использовании ванилина в присутствии концентрированной серной кислоты после кипячения появляется вишневое окрашивание, переходящее в сине-фиолетовое: 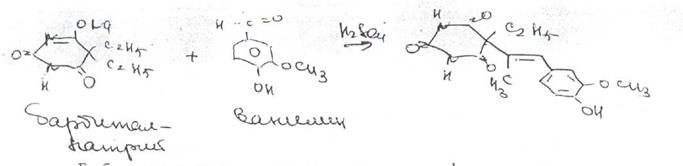
ъароитураты и их натриевые соли можно идентифицировать сплавлением с едкими щелочами, так как они при этом разрушаются с выделением аммиака:
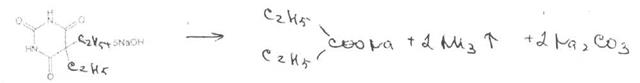
При последующем подкислении хлороводородной кислотой выделяется диоксид углерода и ощущается запах соответствующей жирной кислоты:
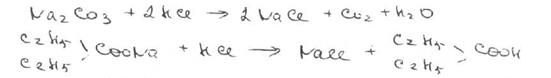
Для натриевых солей барбитуратов выполняют испытание, основанное на нейтрализации разведенной хлороводородной кислотой:
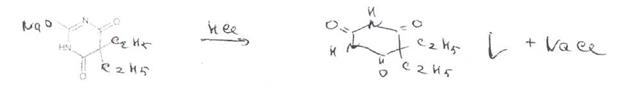
Выпавший осадок барбитурата отфильтровывают, промывают водой, сушат и определяют температуру плавления.
Обнаруживают ион натрия (по окраске пламени).
При испытании чистоты натриевых солей барбитуровой кислоты устанавливают предельное содержание примеси свободной щелочи, метилового спирта .Так как при синтезе барбитала натрия используется метилат натрия. Определяют свободную щелочь методом кислотно-основного титрования (ацидиметрически), растворитель-этанол.
Методы колич. опред.
1. Меркуриметрич. опред. Реакцию взаимодействия производных барбитуровой кислоты с ионом ртути (II), в результате которой образуются нерастворимые в воде соединения, используют для меркуриметрического определения, сочетая его с комплексонометрией. Натриевые соли барбитуратов растворяют в воде, добавляют 10%-ный раствор ацетата натрия и избыток 0,1 М раствора нитрата ртути (II). Осадок барбитурата ртути (II) отфильтровывают, а в фильтрате комплексонометрическим методом (титрант 0,05 М раствор трилона Б, индикатор ксиленоловый оранжевый) в присутствии гексаметилентетранина оттитровывают избыток нитрата ртути (II).
В основе меркуриметрического определения лежит реакция между барбитуратом и нитратом ртути (II):

При комплексонометрическом титровании избытка нитрата ртути (II) раствором трилона Б образуется комплексное соединение ртути:2. Метод ацидиметрии. Метод основан на процессе гидролиза и нейтрализации образовавшегося гидроксида натрия.
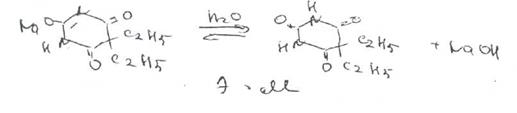
NaOH +HCI — > NaCI + Н2О
Параллельно выполняют контрольный опыт, чтобы учесть возможную примесь свободной щелочи.
Из найденного колва(%) барбитала-натрия вычитают содер. (%) свободной щелочи, умноженное на коэф. 5,15, если эта примесь имеется,
3. Метод аргентометрии.
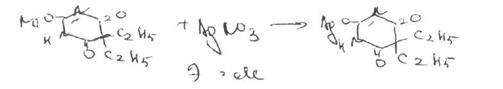
4. Метод гравиметрии,Барбитураты и их натриевые соли можно также количественно определить гравиметрическим методом, осаждая или извлекая кислотные формы барбитуратов. Натриевые соли предварительно переводят в кислотные формы. В качестве эксграгентов используют эфир или хлороформ который затем отгоняют, остаток сушат и взвешивают. Хлороформные извлечения выпаривают досуха (на водяной бане) и остаток растворяют в диметилформамиде. Затем титруют, используя в качестве титранта 0,1 М раствор метилата лития (индикатор тимоловый синий).
5. СФМ в УФ-области. Для количественной оценки барбитуратов и их натриевых солей используют спектрофотометрическое определение в области 239-240 нм. Растворителями при этом служат боратный буферный раствор с рН 10 (барбитал) В указанных условиях барбитал имеет максимум поглощения при 240 нм (550). В скобках указана величина удельного показателя поглощения, по которой рассчитывают содержание барбитурата.
6. ФЭКМ. Известны многочисленные методики фотометрического определения барбитуратов в лекарственных формах, основанные на рассмотренных выше цветных реакциях.
Барбитураты и их натриевые соли хранят по списку Б в хорошо укупоренной таре. Производные барбитуровой кислоты применяют как успокаивающие и снотворные средства. Вопрос 2. Rp.: Infusi herbae Adonidis vernalis 200 ml
Barbitali-natrii 1,0
Natrii bromidi 6,0
Tincturae Convallarii10 ml
Misce. D. S. По 1 столовой ложке 3 раза в день.
Проверка доз:
Траву адониса брали в соответ. с требованиями ГФХ1 Фенобарбитал список Б ВРД0,2 ■ РД0,07 ВСД 0,5 СД0,21
Кол-во приемов: 210:15=14 РД61,0:14=0,07 Дозы не завышены.Концентрация водного извлечения в прописи рецепта не указана. В соответствии с указанием ГФ настой травы горицвета весеннего (сырье хранится по списку Б) изготавливают в соотношении 1 :30. Следовательно, для изготовления 200 мл настоя необходимо взять 6,6 г (200/30) стандартного сырья (биологическая активность 1,0 г травы 50 — 66 ЛЕД или 6,3 — 8 КЕД). В аптеку поступило сырье с биологической активностью 70 ЛЕД.
Массу сырья с более высокой биологической активностью рассчитывают по формуле
Х=АБ/В:
Х= 6,6* 66/70 = 6,22 г.
Расчет объема экстрагента (воды очищенной) с использованием коэффициента водопоглощения . При расчете объема экстрагента следует учитывать, что лекарственное растительное сырье поглощает некоторый объем экстрагента, который удерживается в сырье и после его отжима. Этот объем характеризуется величиной коэффициента водопоглощения сырья (Кв). Общий объем извлечения по прописи рецепта равен 200 мл.
К травы горицвета весеннего 2,8 мл/г, 6,22 г сырья удержат после отжима сырья 17,14 мл воды очищенной (6,22* 2,8) = 17,14 мл.
Объем экстрагента: 200 + 17,14=217,14 мл
Количество сухих веществ менее 4%(3.5%)
После изготовления микстуры оформляют лицевую сторону ПК.
Herbae Adonidis vernalis (70 LED/g). 6,22
Aquae purificatae...........................217,14ml
Barbitali-natrii 1,0
Natrii bromidi .6,0
Tincturae Convallarii 10 ml
V= 210 ml Подписи:
Расчеты для изготовления водного извлечения с использованием экстрактов-концентратов. В аптеке имеется жидкий экстр акт-концентрат горицвета весеннего (1 :2) станд артизо в анный.
При изготовлении водных извлечений из жидких экстрактов-концентратов вместо выписанной по рецепту массы ЛРС берут двойное (по объему) количество концентрата, которое разбавляют соответствующим объемом воды очищенной.
Жидкого экстракта-концентрата следует взять 13,2 мл (6,6 • 2).
При изготовлении микстур с использованием экстрактов-концентратов можно использовать концентрированные растворы других лекарственных веществ. В аптеке имеется концентрированный 20%-ный (1:5) раствор натрия бромида. Его следует взять 6*5=30 мл.
Объем воды очищенной составит 156,8 мл (200 -— 13,2 -— 30).
После изготовления микстуры оформляют лицевую сторону паспорта письменного контроля.
Дата добавления: 2015-08-04; просмотров: 1159;
