Принципиальный состав СРТТ и назначение компонентов
СРТТ − это многокомпонентная композиция, каждый компонент которой выполняет конкретную и важную роль независимо от его содержания в рецептуре.
2.7.1.1 Окислители
Роль окислителя в СРТТ многофункциональна, но прежде всего он является поставщиком активного (свободного) окисляющего агента (O2, F2). Кроме того, окислитель оказывает огромное влияние на плотность и объем газообразных продуктов горения топлива, так как вводится в состав до 70,0–72,0 % и определяет токсичность продуктов горения.
Роль окислителя могут выполнять соли азотной кислоты (нитраты), соли хлорной кислоты (перхлораты) и нитросоединения органических веществ. При их разложении выделяется определенное количество активного окисляющего агента [57].
В таблице 5 представлены реакции разложения некоторых окислителей и содержание в них свободного кислорода в отсутствии горючих компонентов.
Таблица 5 − Реакции разложения окислителей
| Химическая формула окислителя | Реакция разложения | Количество кислорода в 1 кг на 1 кг вещества | Растворимость в воде в граммах на 100 г раствора | |
| при 20 °С | при 100 °С | |||
| KClO3 | 2KClO3 = 2KCl + 3O2 | 0,39 | ||
| NaClO3 | 2NaClO3 = 2NaCl + 3O2 | 0,45 | ||
| KClO4 | KClO4 = KCl + 2O2 | 0,46 | 1,7 | |
| NaClO4 | NaClO4 = NaCl + 2O2 | 0,52 | ||
| NH4ClO4 | 2NH4ClO4 = 4H2O + Cl2 + +2O2 + N2 | 0,34 | - | |
| KNO3 | KNO3 = K2O + N2 + 2,5O2 | 0,40 | ||
| NaNO3 | 2NaNO3 = Na2O + N2 + +2,5O2 | 0,47 | ||
| NH4NO3 | NH4NO3 = 2H2O + N2 + +0,5O2 | 0,2 |
Требования, предъявляемые к окислителям:
1. Максимальное содержание свободного (активного) окисляющего агента (O2, F2) − не менее 30 % и легкое выделение его при горении топлива.
2. Минимальная теплота образования. Чем она меньше, тем выше значение единичного импульса топлива
J = 9,3264 D 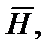
где D 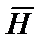 = Qобр. прод. горения - Qобр. исх. компонентов.
= Qобр. прод. горения - Qобр. исх. компонентов.
3. Стабильность свойств при температуре переработки, хранении и эксплуатации изделий. Окислитель не должен разлагаться и изменять своего агрегатного состояния.
4. Окислитель должен иметь: хорошую адгезию к связующему-горючему; минимальную чувствительность к механическим воздействиям; максимальную плотность; широкую сырьевую базу и низкую стоимость.
5. Он должен совмещаться без химического взаимодействия и выделения газообразных продуктов в процессе смешения топливной массы при хранении и эксплуатации изделий.
В таблице 6 приведены некоторые свойства солей и нитросоединений органических веществ, которые могут выполнять роль окислителя СРТТ.
Исходя из перечисленных требований, предъявляемых к окислителям, и анализа физико-химических свойств, представленных в таблице 6, можно сделать следующие рекомендации:
1. С точки зрения содержания активного окисляющего агента наиболее выигрышно смотрятся перхлораты нитрония, нитрозила, лития и нитрат лития, но ни один из них не нашел применения в СРТТ, так как сильно гигроскопичны, а перхлораты нитрония и нитрозила нестойки.
2. Поскольку рабочим телом в ракетном двигателе являются газообразные продукты горения топлива, то наиболее выгодно по объему газообразных продуктов, образующихся при разложении, применение нитрата аммония (0,980 м3/кг). Но он гигроскопичен и имеет низкое содержание свободного кислорода (20 %). Нитрат аммония нашел при-менение в качестве окислителя в составах для пороховых аккумуляторов давления. Заряды невелики по размерам и их можно хранить в герметично закрывающейся таре или полиэтиленовых пакетах.
3. Важным показателем для компонентов СРТТ является плотность, так как она определяет показатель весового качества ракетного двигателя. Максимальную плотность имеют соли бария, но при их разложении выделяется небольшой объем газообразных продуктов. Они широко применяются для изготовления пиротехнических изделий, так как сами и их оксиды придают пламени интенсивную зеленую окраску.
По комплексу характеристик в качестве окислителя СРТТ нашел широкое применение перхлорат аммония, хотя и выделяет при разложении небольшое количество свободного кислорода (34 %).
Таблица 6 − Физико-химические свойства солей и нитросоединений органических веществ
| Наименование окислителя | Химическая формула | Молекулярная масса | Плотность, г/см3 | Температура плавления, °С | Объем газов, выделяемых при разложении 1 кг вещества, м3 | Количество свободного кислорода, % | Физическая стабильность и химическая стойкость | |
| Нитрат лития | LiNO3 | 69,0 | 2,38 | 0,568 | 58,0 | Очень гигроскопичен | ||
| Нитрат натрия | NaNO3 | 85,0 | 2,20 | 0,439 | 47,1 | Гигроскопичен | ||
| Нитрат калия | KNO3 | 101,0 | 2,11 | 0,386 | 39,6 | малогигроскопичен | ||
| Нитрат аммония | NH4NO3 | 80,0 | 1,72 | 0,980 | 20,0 | Гигроскопичен | ||
| Нитрат бария | Ba(NO3)2 | 261,0 | 3,20 | 0,138 | 30,6 | малогигроскопичен | ||
| Перхлорат нитрония | NO2ClO4 | 145,5 | 2,25 | 180 р | 0,616 | 66,2 | Очень гигроскопичен, малостоек | |
| Перхлорат нитрозила | NOClO4 | 129,5 | 2,17 | 50 р | 0,605 | 61,8 | сильно гигроско-пичен, нестоек | |
| Гидразин диперхлорат | N2H4(ClO4)2 | 232,0 | 2,02 | 0,774 | 35,8 | Сильно гигроскопичен, высокая чувствительность к механ. возд. несовместим с комп. СРТТ | ||
| Перхлорат лития | LiClO4 | 106,4 | 2,43 | 0,422 | 60,2 | гигроскопичен | ||
| Перхлорат натрия | NaClO4 | 122,5 | 2,02 | 0,365 | 52,3 | гигроскопичен | ||
| Перхлорат калия | KClO4 | 139,0 | 2,52 | 0,322 | 46,2 | негигроскопичен | ||
| Перхлорат аммония | NH4ClO4 | 117,5 | 1,95 | 150 р | 0,790 | 34,0 | малогигроскопичен | |
| Перхлорат бария | Ba(ClO4)2 | 336,4 | 2,34 | 0,270 | 38,0 | малогигроскопичен | ||
| Гексонитроэтан | C2(NO2)6 | 304,0 | 1,86 | 55 р | 0,516 | 53,3 | нелетуч, нестоек, склонен к тепловому самовоспла-менению | |
| Октоген | C4H8N8O8 | - | 1,92 | 278,5–280,0 | - | - | - | |
| Гексоген | C3H6N6O6 | - | 1,82 | 204,5–205,0 | - | - | - | |
| Примечание − р − начало реакции разложения | ||||||||
Перхлорат калия нашел применение в плазмообразующих составах. Остальные компоненты, представленные в таблице 6, применения в составах СРТТ не нашли, так как гигроскопичны. В последнее время в составах СРТТ широко применяются гексоген, октоген, а также
АДНА [52, 68, 72–73].
Свойства ПХА и способы его производства [61-62].ПХА – белое кристаллическое вещество. Плотность 1,88–1,95 г/см3. Температура начала разложения 150 °С (при длительном воздействии).
Он существует в двух кристаллических модификациях: ромбической и кубической. Обычная кристаллическая форма − ромбическая, при температуре 240 °С переходит в кубическую, при этом увеличивается объем кристаллов и поглощается тепло. Ромбическая модификация представляет собой кристаллический порошок белого цвета с плотностью 1,95 г/см3.
ПХА склонен к электризации, причем его элекризуемость возрастает с увеличением дисперсности. Так, фракция с размером частиц 200-300 мкм электризуется до потенциала 1,0–2,6 кВт, а фракция с размером частиц до 100 мкм – до 6,0–11,0 кВт. Увеличение его влажности с 0,04–0,07 % до 5,0–6,0 % снижает сравнительную электризуемость с 8,0–11,0 кВт до 0,4–1,7 кВт.
ПХА способен увлажняться. Его гигроскопическая точка при
20 °С составляет 96,0 %. При относительной влажности воздуха 75,0 % влажность ПХА за 4–6 ч достигает равновесного состояния 1,5 %.
В связи с изменением гигроскопичности ПХА при изменении условий хранения может слеживаться. Слеживаемость и плохая сыпучесть затрудняют его переработку (фракционирование, дозирование, транспортировку). Он налипает на рабочие органы дозатора, что влияет на точность дозирования. Образование агломератов может быть причиной непромесов в топливной массе. Для снижения слеживаемости используют антислеживающие добавки.
ПХА растворим в воде, спиртах, а также в глицерине, ацетоне. Не растворим в бензине, толуоле, дибутилфталате, нитрометане, этиловом эфире, этиленгликоле и в абсолютном большинстве горюче-связующих веществ.
Химическая активность ПХА определяется тем, что это соль очень сильной кислоты и слабого основания. Вследствие этого водные растворы проявляют кислую реакцию, под действием концентрированных соляной и азотной кислот происходит полное разложение ПХА.
Щелочи легко вступают с ПХА в обменную реакцию. Вследствие чего нельзя использовать в контакте с ним материалы и вещества с основными свойствами. В сухом состоянии ПХА не взаимодействует с металлами, во влажном оказывает корродирующее действие. Это является следствием образования хлорной кислоты
NH4ClO4 + H2O = HClO4 + NH4OH,
которая корродирует металл. Поэтому все оборудование, предназначенное для переработки ПХА, должно быть изготовлено из нержавеющей стали.
ПХА − термически стойкое соединение, только при длительном нагревании при температуре 150 °С можно добиться его разложения.
С повышением температуры и в присутствии примесей скорость распада растет.
Скорость и глубина разложения ПХА существенно изменяются в присутствии катализаторов. Например, добавка 1 % ферроцена повышает скорость распада ПХА в 2 раза, а добавка 1 % фтористого лития замедляет низкотемпературную стадию его распада.
Взрывчатые характеристики.ПХА способен детонировать от капсюля-детонатора № 8, если диаметр заряда превышает 60 мм и его плотность близка к единице. Увлажнение ПХА резко понижает его восприимчивость к детонации. Скорость детонации ПХА при изменении диаметра заряда от 60 до 90 мм возрастает с 2340 до 2780 м/с.
С увеличением степени дисперсности ПХА скорость детонации растет.
ПХА молочувствителен к тепловому импульсу. Свободно насыпанный на поверхность в количестве до 100 кг не воспламеняется от мощного луча огня.
Чувствительность ПХА к механическим воздействиям зависит от его дисперсности, влажности, присутствия примесей и условий испытаний.
Токсичность.ПХА относится к весьма токсичным веществам. Соединения хлорной кислоты блокируют поступление йодидов из крови в щитовидную железу. При воздействии ПХА на организм развивается острая или хроническая интоксикация, наблюдается расстройство кровообращения и дистрофическое изменение мышц сердца, почек, печени. Снижается деятельность вегетативной нервной системы.
ПХА влияет на кальциевый обмен − приводит к разрушению костной ткани эмали. Допустимая концентрация ПХА в воде водоемов
3 мг/л. Максимальная концентрация в смеси производственных и хозяйственно-фекальных вод не должна превышать 150 мг/л. Предельно допустимая концентрация (ПДК) в воздухе 0,001 г/м3.
Производство ПХА.Промышленностью освоено два способа получения ПХА:
1) нейтрализацией хлорной кислоты газообразным аммиаком;
2) обменной реакцией между перхлоратом натрия, аммиаком и соляной кислотой.
Основным сырьем для получения ПХА по методу нейтрализации являются: соляная кислота, газообразный аммиак и дистиллированная вода.
Технологический процесс состоит из трех стадий:
1. Получение технической (48–50%-ной) хлорной кислоты электролизом водного раствора соляной кислоты.
2. Очистка хлорной кислоты от соляной электрохимическим методом.
3. Получение ПХА взаимодействием хлорной кислоты с аммиаком.
Обменный метод получения ПХА применяется на большинстве действующих заводов. Основное сырье: хлорид натрия, аммиак, соляная кислота.
Технологический процесс получения ПХА состоит из следующих стадий:
1. Электрохимическое окисление хлорида натрия до хлората натрия.
2. Электрохимическое окисление хлората натрия до перхлората натрия.
3. Обменная равновесная реакция в растворе между перхлоратом натрия, аммиаком и соляной кислотой.
Получают ПХА трех марок: К, С, М (крупный, средний, мелкий), отличающихся между собой гранулометрическим составом.
В производстве СРТТ используется перхлорат аммония с округлой формой частиц с целью снижения вязкости топливных масс и повышения уровня физико-механических характеристик топлива [61-62].
2.7.1.2 Связующие-горючие
Связующее-горючее в составе СРТТ выполняет следующие функ-ции:
- обеспечивает определенный уровень реологических характеристик топливной массы в сочетании с окислителем и энергетической добавкой;
- связывает в единое целое компоненты топлива, придавая заряду необходимый уровень физико-механических характеристик;
- является дополнительным источником тепловой энергии и газообразных продуктов горения топлива.
Количество горюче-связующего вещества в составе СРТТ определяется прежде всего содержанием активного окисляющего агента. Чем больше активного кислорода в окислителе, тем больше можно взять связующего-горючего для обеспечения стехиометрического соотношения компонентов. Если связующее-горючее в своем составе содержит активные группы −NO2, −ONO2, −F2 и др., то его количество для получения стехиометрического соотношения может достичь
30 % масс. и есть возможность получить топливную массу с низкой вязкостью. Чтобы обеспечить однородность состава топлива, устойчивость ее структуры и высокие физико-механические характеристики топлива, количество связующего должно быть не менее 10 % масс. Кроме того, количество связующего-горючего оказывает большое вли-яние на реологические свойства топливной массы и определяет способность ее переработки. Так, при содержании связующего-горючего в рецептуре в количестве 10 % масс., топливная масса может перерабатываться глухим прессованием, при содержании 10–15 % масс. − приходным прессованием, 10–20 % масс. − литьем под небольшим давлением, 15–20 % свободным литьем.
Связующее-горючее может представлять собой смесь горючего со связующим (металл+смола) или соединением, обладающим одновременно свойствами горючего и связующего (битумы, каучуки). Низкомолекулярные горюче-связующие как компоненты СРТТ малопригодны. Практический интерес в качестве связующих-горючих СРТТ представляют высокомолекулярные соединения [63–64, 75–76].
Требования, предъявляемые к связующим-горючим:
1.Связующее-горючее должно быть вязкой жидкостью или твердым полимером, способным образовывать с низкомолекулярным веществом термодинамически устойчивые системы, способные к восприятию большого количества наполнителя (окислитель, специальные до-бавки). Низкая вязкость связующего-горючего может привести к расслаиванию топливной массы и не позволит выполнить требования по уровню физико-механических характеристик.
2. Связующее-горючее должно иметь:
- хорошие смачивающую способность и адгезию к наполнителю;
- низкую температуру стеклования;
- высокое отношение водорода к углероду;
- отсутствие в составе элементов, дающих агрессивные продукты горения;
- малую теплоту образования, а продукты окисления - большую теплоту образования;
- оптимальную плотность;
- высокую физическую и химическую стабильность с целью обеспечения требуемого гарантийного срока хранения изделия;
- широкую сырьевую и промышленную базу, что гарантирует низкую стоимость.
3. Связующее-горючее должно обладать требуемой «живучестью» (жизнеспособностью) при переработке топливной массы и способностью отверждаться при температуре 40–60 °С без существенного выделения тепла и с минимальной усадкой.
4. В отвержденном состоянии оно должно иметь высокие физико-механические характеристики и обладать упруго-эластичностью для обеспечения сохранения сплошности изделия, сопротивляемости сжатию и растяжению.
5. В целях безопасной переработки должно обладать низкой чувствительностью к механическим воздействиям.
Основные представители связующих-горючих.Одним из первых каучуков, нашедших применение в качестве связующего-горючего СРТТ, был полисульфидный каучук − тиокол. Он является продуктом взаимодействия дихлордиэтиленформаля с тетрасульфидами щелочных металлов. Отличительный признак тиокола − наличие меркаптановых групп −SH.
В производстве СРТТ нашли применение тиоколы марок НВТ-1 и Т-2.
Дата добавления: 2015-08-01; просмотров: 3802;
