ОПУХОЛЕВЫЙ ПРОЦЕСС КАК БИОЛОГИЧЕСКОЕ ЯВЛЕНИЕ
Опухолевый процесс - это процесс, сопровождающийся прибавлением клеточной массы. Для новообразований характерен автономный тип роста. В норме количество клеток регулируется посредством точной балансировки двух противоположных процессов - клеточного деления и клеточной элиминации. При онкологическом заболевании прибавление клеточной массы опережает клеточную гибель либо за счет активации процессов пролиферации, либо вследствие угнетения процессов апоптоза, а чаще всего - при сочетанном нарушении этих процессов. Существенно, что дисбаланс регуляции количества клеток вызван неспособностью трансформированного клона реагировать на внешние сигналы; таким образом, объем клеточной массы перестает зависеть от потребностей организма, что и подразумевается под понятием «автономность».
На протяжении всего XX века ученые пытались сформулировать, какие конкретные признаки отличают опухолевые клетки и ткани от их нормальных предшественников. Прогресс в данной области, представляющей основу для разработки направлений противоопухолевой терапии, затруднялся биологическим разнообразием проявления новообразований. Тем не менее к настоящему времени удалось выделить и классифицировать несколько четких, подкрепленных молекулярногенетическими данными тенденций. Наиболее ясное обобщение этих признаков представлено в работе основоположников молекулярной онкологии D. Hanahan и R. Weinberg, появившейся на страницах журнала Cell (? 1 за 2000 г.). По мнению авторов, все или почти все опухоли характеризуются несколькими неотъемлемыми чертами.
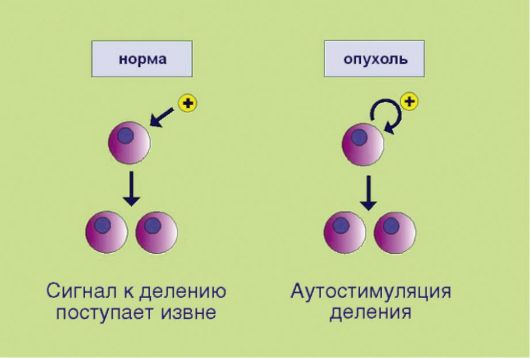 Рис. 5.1.Аутостимуляция пролиферативного сигнала
Рис. 5.1.Аутостимуляция пролиферативного сигнала
1. Самодостаточность в отношении сигналов пролиферации, связанная e аутопродукцией факторов роста, соответствующих рецепторов или других компонентов сигнального промитотического каскада(рис. 5.1). Существенно, что нормальная клетка никогда не делится сама по себе; для запуска пролиферативной программы необходим сигнал извне, доставляемый эндокринной системой (гормоны), паракринными механизмами (тканевые факторы роста), или через синаптические окончания нейронов (нейротрофика). Таким образом, увеличение количества клеток в норме происходит лишь в том случае, если многоклеточный организм-хозяин продуцирует сигналы к наращиванию клеточной массы. Трансформированная клетка продуцирует подобные сигналы сама для себя, вне зависимости от потребностей организма, что и приводит к безостановочному делению опухолевого клона.
2. Потеря чувствительности к сигналам, сдерживающим процесс пролиферации, обусловленная инактивацией супрессорных (антимитотических) белков (рис. 5.2). Клоны, обладающие аномальной способностью к аутостимуляции пролиферативного каскада, могут возникать в организме достаточно часто, что связано с постоянным мутационным процессом в клетках организма. Однако все многоклеточные представители живой природы выработали в процессе эволюции несколько уровней защитных систем, препятствующих несанкционированному накоплению клеток. В случае появления клеток со способностью к аутокринной стимуляции деления организмхозяин продуцирует сдерживающие сигналы, доставляемые к клеткам
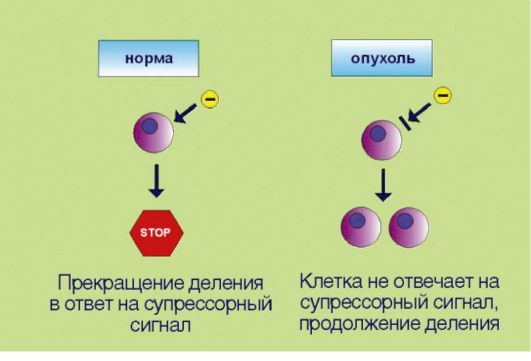 Рис. 5.2.Потеря чувствительности к сигналам, прекращающим клеточное деление
Рис. 5.2.Потеря чувствительности к сигналам, прекращающим клеточное деление
в виде гуморальных факторов и направленные на прекращение пролиферации. Трансформированные клетки в отличие от нормальных утратили способность к восприятию таких сигналов. Подобная нечувствительность к супрессорным воздействиям может происходить в результате утраты соответствующих мембранных рецепторов или других компонентов сигнальных каскадов, участвующих в проведении экстрацеллюлярного сигнала к клеточному ядру.
3. Замедление процессов программируемой клеточной гибели, опосредованное дисбалансом биохимической регуляции процессов апоптоза (рис. 5.3). В повседневной жизни слово «смерть» всегда подразумевает негативный эмоциональный оттенок. Напротив, в условиях функционирования многоклеточных живых систем физиологическое значение гибели клеток в значительной мере зависит от контекста этого события. Принято выделять 2 основные разновидности клеточной смерти: непрограммируемая и программируемая. Непрограммируемая гибель клеток (некроз) происходит в результате выраженных неблагоприятных воздействий (гипоксия, ожог и т.д.). Подобное событие может негативно отражаться на структуре и функции органа и сопровождаться формированием рубцовой ткани. Программируемая клеточная гибель в отличие от некроза является ювелирно управляемым, энергозатратным процессом, направленным на сохранение и поддержание морфофункциональных характеристик органов и тканей. Наиболее
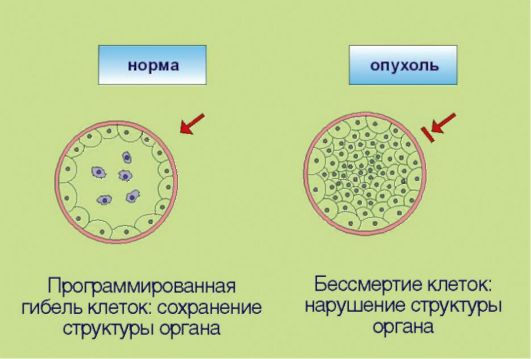 Рис. 5.3.Иммортализация (бессмертие)
Рис. 5.3.Иммортализация (бессмертие)
изученная разновидность программируемой клеточной гибели - апоптоз - обеспечивает «плановую» элиминацию клеток; этот процесс особенно выражен в тканях с высокой интенсивностью обновления клеток - в эпителии ЖКТ, коже, крови. Помимо этого клетка способна распознавать собственные повреждения ДНК и другие биохимические изменения, представляющие угрозу с точки зрения злокачественной трансформации. При появлении подобных нарушений запускается «суицидная» программа, приводящая к самоуничтожению потенциально опасных клеток. Раковые клетки в отличие от нормальных утратили способность к самоэлиминации, что позволяет им сохранять жизнеспособность, несмотря на наличие повреждений ДНК и ассоциированных с гиперпролиферацией стрессовых условий существования.
4. Неограниченный репликативный потенциал клеток (преодоление «лимита Хэйфлика»), сопряженный с реактивацией экспрессии фермента теломеразы и как следствие отсутствием физиологического укорачивания теломер (рис. 5.4). Представим, что в организме возник клон клеток, обладающий способностью к аутостимуляции деления, не чувствительный к супрессорам митоза и утративший способность к самоэлиминации посредством апоптоза. Даже эти клетки, обладающие целым набором характеристик злокачественной трансформации, не смогут сформировать клинически распознаваемую опухоль! В многоклеточных организмах существует еще один уровень защиты: ограничение
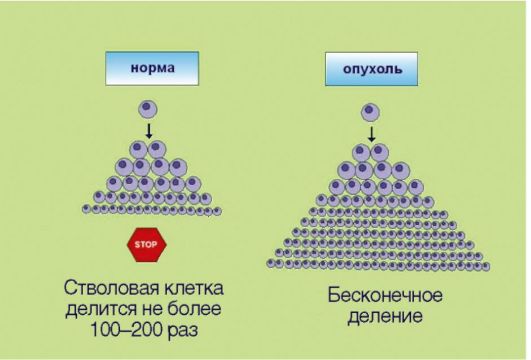 Рис. 5.4.Неограниченный репликативный потенциал (бесконечное деление)
Рис. 5.4.Неограниченный репликативный потенциал (бесконечное деление)
репликативного потенциала делящихся клеток. В 1961-1962 гг. американский ученый L. НауШек установил, что нормальные клетки могут делиться не более 100-150 раз, после чего весь клон (т.е. исходная клетка и ее потомки, обладающие соответственно меньшим резервом возможных делений) утрачивает возможность к самовоспроизведению. Этот феномен, зачастую называемый лимитом Хэйфлика, по крайней мере отчасти лежит в основе биологических механизмов старения: установлено, что репликативный потенциал клеток уменьшается с возрастом индивидуума. Более того, преодоление лимита Хэйфлика является необходимым условием злокачественной трансформации; демонстрацией этого свойства является тот факт, что в лабораторных условиях только опухолевые клетки могут подвергаться многолетнему культивированию, в то время как долгосрочные культуры нормальных клеток получить не удается. Неограниченный репликативный потенциал опухолевых клеток принято объяснять активацией фермента теломеразы, которая компенсирует наблюдаемое в ходе клеточного деления физиологическое укорочение концевых участков хромосом. Теломераза, по-видимому, является одной из самых перспективных молекулярных мишеней для противоопухолевой терапии.
5. Стимуляция процессов ангиогенеза в опухоли, вызванная экспрессией трансформированными клетками ангиогенных факторов и направленная на удовлетворение повышенных потребностей быстроделящихся неопластичес-
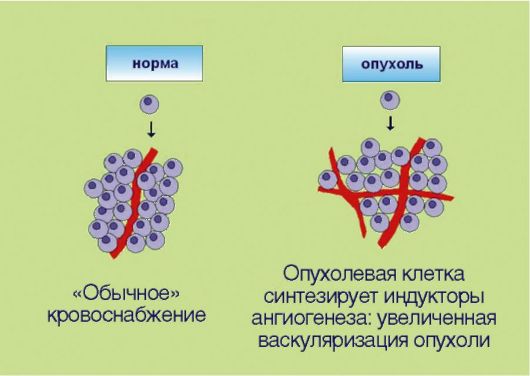 Рис. 5.5. Индукция ангиогенеза
Рис. 5.5. Индукция ангиогенеза
ких компонентов в оксигенации (рис. 5.5). Длительное время опухолевым клеткам приписывалась полная самодостаточность. Предполагалось, что трансформированный клон пролиферирует сам по себе, а все остальные элементы опухоли - строма, сосуды, фибробласты - являются лишь пассивными вспомогательными компонентами. Изменение этих представлений связано с именем выдающегося американского ученого J. Folkman, который совмещал повседневную работу врачахирурга с основополагающими, фундаментальными исследованиями в области экспериментальной онкологии. J. Folkman предположил и экспериментально доказал, что опухолевые клетки могут сформировать клинически распознаваемое новообразование лишь в том случае, если они продуцируют факторы неоангиогенеза. Таким образом, формирование сосудистой сети опухоли происходит не само по себе, а за счет активных, управляемых трансформированными клетками биологических процессов. К настоящему времени идентифицированы десятки факторов, провоцирующих или, наоборот, ингибирующих ангиогенез. Примечательно, что разработка антиангиогенных препаратов считается одним из самых перспективных направлений в онкологии. Дело в том, что во взрослом организме практически не происходит формирования новых сосудов (исключение составляют посттравматическая регенерация тканей и некоторые процессы, связанные с репродуктивным циклом у женщин). Предполагается, что антиангиогенные препараты должны обладать прекрасным
терапевтическим индексом, т.е. эффективно тормозить рост опухолевой массы без каких-либо побочных воздействий на организм.
6. Способность к инвазии и метастазированию, ассоциированная с продукцией опухолью гистолитических ферментов (протеаз), а также факторов, угнетающих локальный иммунитет (рис. 5.6). Эта особенность злокачественной трансформации почти всегда упоминается как ключевой компонент опухолевого роста. Внимание к инвазии и метастазированию связано с клинической значимостью данных процессов: именно они компрометируют результаты хирургического лечения рака и приводят к летальному исходу у онкологических больных. В контексте сказанного отметим, что ни один из перечисленных признаков опухолевого роста не является достаточным для клинической манифестации онкологического процесса. В частности, процесс метастазирования нетрансформированных клеток характерен для заболевания женской репродуктивной системы - эндометриоза, которое никоим образом не является онкологической патологией.
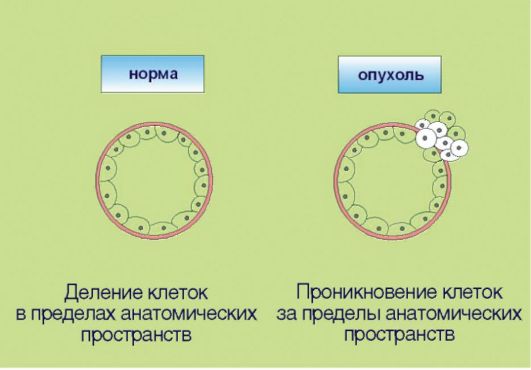 Рис. 5.6.Инвазия и метастазирование
Рис. 5.6.Инвазия и метастазирование
7. Геномная нестабильность, опосредованная инактивацией систем репарации ДНК и нарушениями в молекулярном контроле клеточного цикла (рис. 5.7). Для опухолевой клетки характерно ускоренное накопление мутаций, что по крайней мере отчасти связано со снижением эффективности процессов репарации ДНК. Подобная особенность приводит к чрезвычайной биологической пластичности новообразований, которые способны быстро приспосабливаться
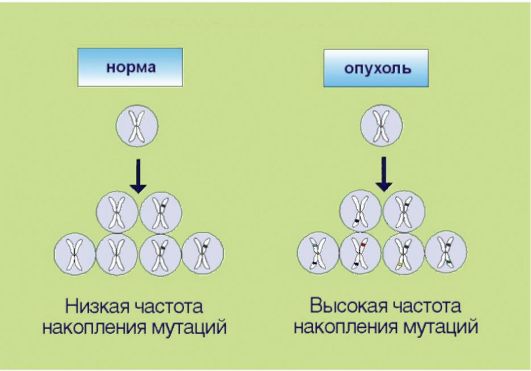 Рис. 5.7.Геномная нестабильность
Рис. 5.7.Геномная нестабильность
к изменяющимся условиям метаболизма и разнообразным лечебным воздействиям. Существенно, что геномная нестабильность, по-видимому, является основным свойством опухолевых клеток, обеспечивающим «терапевтическое окно» при назначении цитостатических препаратов. Ранее полагали, что механизм лечебного действия цитостатиков связан с избирательным подавлением делящихся клеток. Это утверждение остается в силе, однако нуждается в важном дополнении. Противоопухолевый эффект химиотерапии и радиации связан с индукцией повреждений ДНК, которые действительно проявляются лишь в процессе клеточного деления; однако опухолевые клетки, по крайней мере в теории, обладают большей чувствительностью к ДНК-повреждающим агентам, так как их способность к репарации химических изменений структуры нуклеиновых кислот ниже, чем у неизменных компонентов органов и тканей.
8. Перестройка стромальных компонентов, создающая более благоприятные условия для эволюции злокачественного клона (рис. 5.8). Длительное время предполагалось, что элементы стромы образуют лишь пассивный каркас для размножающихся опухолевых клеток. В последние годы установлено, что подобное утверждение далеко от истины. Многочисленные факты свидетельствуют о том, что стромальные компоненты опухолей заметно отличаются от таковых в нормальных тканях; некоторые исследователи даже настаивают
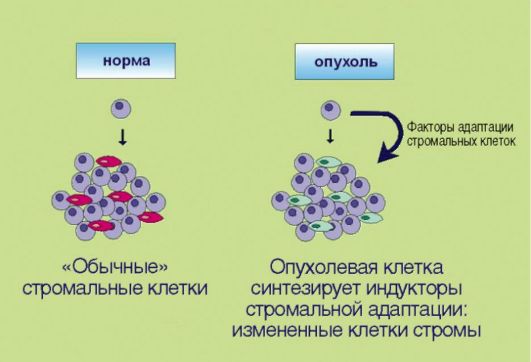 Рис. 5.8.Адаптация стромальных клеток к особенностям опухолевого роста
Рис. 5.8.Адаптация стромальных клеток к особенностям опухолевого роста
на том, что фибробласты, инфильтрирующие эпителиальные новообразования, содержат соматические мутации, отличные от таковых в опухолевых клетках и необходимые для жизнедеятельности злокачественного новообразования. Продемонстрированы многочисленные случаи симбиоза трансформированных клеток и окружающих их фибробластов. В частности, независимость малигнизированного эпителия от внешних пролиферативных сигналов может обеспечиваться не аутокринной стимуляцией как таковой, а секрецией факторов роста фибробластами, населяющими опухоль. В свою очередь, эпителиальные клетки секретируют целый спектр биологически активных веществ, регулирующих адаптацию стромальных элементов к потребностям опухолевого роста.
Подобная «диссекция» ключевых признаков опухолевого роста имеет существенное практическое значение. Эмпирический подход, сопряженный со случайным перебором тысяч биологически активных химикатов, постепенно замещается научно обоснованным, молекулярно-направленным поиском действительно специфических противораковых средств, направленных на активацию или инактивацию ключевых биохимических компонентов опухолевой трансформации. Первые подобные средства уже внедрены в практическую медицину. По-видимому, их количество увеличится в ближайшие годы в десятки раз, что приведет к существенному улучшению результатов противоопухолевой терапии.
Дата добавления: 2015-07-24; просмотров: 2713;
