Высокоэнергетические соединения. Атф — универсальная форма химической энергии в клетке
Стерилизация
Выделение отдельных видов бактерий из исследуемого материала, содержащего, как правило, смесь различных микроорганизмов, является одним из этапов любого бактериологического исследования, проводимого с различными целями: диагностики заболеваний, определения микробной обсеменен-ности окружающей среды и т.д. Для выделения чистой культуры применяют методы, основанные на: 1) механическом разобщении бактериальных клеток; 2) предварительной обработке исследуемого материала с помощью физических или химических факторов, оказывающих избирательное антибактериальное действие; 3) избирательном подавлении размножения сопутствующей микрофлоры физическими или химическими факторами во время инкубации посевов; 4) способности некоторых бактерий быстро размножаться в организме чувствительных к ним лабораторных животных (биопробы). ,
Таблица 1.Методы стерилизации, разрешенные для применения в ЛПУ.
| Тип метода | Метод | Стерилизующий агент | |
| Физический (термический) | Паровой | Водяной насыщенный пар под избыточным давлением | |
| Воздушный | Сухой горячий воздух | ||
| Инфракрасный | Инфракрасное излучение | ||
| Гласперленовый | Среда нагретых стеклянных шариков | ||
| Химический | Газовый | Окись этилена или ее смесь с другими компонентами | |
| Окись этилена или ее смесь с другими компонентами | |||
| Окись этилена или ее смесь с другими компонентами | |||
| Плазменный | Пары перекиси водорода в сочетании с их низкотемпературной плазмой | ||
| Жидкостный | Растворы химических средств (альдегид-, кислород- и хлорсодержащие) |
Анализ имеющихся в настоящее время разработок в области стерилизации позволяет
Облучатель предназначен для обеззараживания воздуха помещений ЛПУ в условиях постоянного ультрафиолетового излучения с целью профилактики бактериального загрязнения. Облучатель обеспечивает готовность к эксплуатации помещений ЛПУ в соответствии с нормами и требованиями, регламентированными органами санэпиднадзора МЗ РФ. Облучатель размещают в операционных , перевязочных , смотровых , стоматологических кабинетах и других помещениях , где требуется работа со стерильными медицинскими инструментами и средой, в том числе в помещениях категории I (уровень бактерицидной эффективности не менее 99,9%).
Бактерицидная камера для хранения стерильных медицинских изделий
Рециркулятор предназначен для обеззараживания воздуха помещений в присутствии и отсутствии людей в процессе принудительной циркуляции воздушного потока через корпус, внутри которого размещены две бактерицидные лампы низкого давления.
Устранимый бактериальный фильтр
Реакции энергетического обмена представляют важнейшую функцию микроорганизмов, связанную с их преимущественно химическим взаимодействием со средой. Это взаимодействие полностью определяется термодинамическими закономерностями. Бактерии удивительно полно используют возможности получения энергии, но в этом отношении действует ряд ограничений, обусловленных способами ее превращения.
Источниками энергии для организмов могут служить свет и восстановленные химические соединения. Способность использовать энергию света свойственна фотосинтезирующим микроорганизмам, представляющим несколько филогенетически и функционально различных групп. Наибольшее распространение получил оксигенный фотосинтез, осуществляемый цианобактериями и всеми фототрофными эукариотами. Для природоведческой микробиологии его значение связано прежде всего с первичной продукцией, представляющей исходный этап большинства трофических цепей, и с образованием молекулярного кислорода, обеспечивающего существование аэробов.
Способность использовать химическую энергию присуща всем без исключения организмам. Особенно многообразны возможности прокариот. Это относится как к природе окисляемых субстратов, которыми могут быть неорганические (например, Н2, S2-, S0, S2О3-2, NH3, Fe2+, CO) или многочисленные органические соединения, так и окислителей (О2 Fe3+, NO3-, SO42, S0, CO2, органические вещества). Организмы используют в первую очередь субстраты, дающие наибольший выигрыш энергии.
Брожением называется анаэробный процесс превращения безазотистых органических веществ (главным образом углеводов) микроорганизмами, при котором происходит накопление продуктов неполного окисления (спиртов, органических кислот, углеводов и др.) и который сопровождается выделением энергии. Биологическое значение брожения заключается в образовании энергии для осуществления жизнедеятельности микроорганизмов подобно дыханию животных и растений.
Изучение у прокариот электронтранспортных цепей, функционирующих в процессах дыхания и фотосинтеза I и II типа, выявило принципиальное сходство между ними. В обеих системах электронного транспорта есть флавопротеины, хиноны, цитохромы и белки, содержащие негемовое железо, позволяющие переносить электроны вниз по термодинамической лестнице. Таким образом, по существу обе электронтранспортные цепи являются окислительными. Разнообразие в их организации обнаружено при более детальном изучении и выражается как в широком наборе доноров и акцепторов электронов, так и в конкретной организации самих цепей: химическом строении переносчиков, принадлежащих к одному типу, их наборе, расположении и т. д.
В процессах дыхания и фотосинтеза освобождающаяся при переносе электронов энергия запасается первоначально в форме электрохимического трансмембранного градиента ионов водорода (DmH+), т. е. имеет место превращение химической и электромагнитной энергии в электрохимическую. Последняя затем может быть использована для синтеза АТФ. Поскольку в обоих процессах синтез АТФ обязательно связан с мембранами, реакции, приводящие к его образованию, получили название мембранзависимого фосфорилирования. Последнее подразделяется на два вида: окислительное (АТФ образуется в процессе электронного переноса при окислении химических соединений) и фотосинтетическое (синтез АТФ связан с фотосинтетическим электронным транспортом) фосфорилирование. Следует подчеркнуть, что принципы генерации АТФ при фотосинтезе и дыхании, т. е. механизмы мембранзависимого фосфорилирования, одинаковы. Таким образом, энергия, получаемая в процессах брожения, дыхания или фотосинтеза, запасается в определенных формах.
Существуют две универсальные формы энергии, которые могут быть использованы в клетке для выполнения разного рода работы: энергия высокоэнергетических химических соединений (химическая) и энергия трансмембранного потенциала ионов водорода (электрохимическая).
Высокоэнергетические соединения. Атф — универсальная форма химической энергии в клетке
У прокариот существует несколько типов богатых энергией химических соединений. Самую большую группу составляют соединения с высокоэнергетической фосфатной связью: ацилфосфаты, фосфорные эфиры енолов (фосфоенолпируват), нуклеотидди- и трифосфаты, аденозинфосфосульфат. Другая распространенная группа — соединения с высокоэнергетической тиоэфирной связью — ацилтиоэфиры.
Эти соединения характеризуются тем, что по крайней мере одна из входящих в состав молекулы групп имеет высокий энергетический потенциал. При переносе этой группы происходит разрыв связи, соединяющей ее с молекулой, что приводит к резкому уменьшению свободной энергии, заключенной в молекуле химического соединения. Такие связи называются высоко-энергетическими, или макроэргическими. Присоединение группы с высоким энергетическим потенциалом к молекуле-акцептору повышает уровень ее свободной энергии, переводя, таким образом молекулу в активированную форму, в которой это соединение может участвовать в биосинтетических реакциях.
Центральное место в процессах переноса химической энергии принадлежит системе АТФ. АТФ образуется в реакциях субстратного и мембранзависимого фосфорилирования. При субстратном фосфорилировании источником образования АТФ служат реакции двух типов:
I. Субстрат ~ Ф20 + АДФ « субстрат + АТФ; II. Субстрат ~ X + АДФ + ФцН « субстрат + Х + АТФ.
20 Символ "~", введенный американским биохимиком Ф. Липманом (F. Lipmann), служит для обозначения макроэргической связи.
В реакциях первого типа осуществляется перенос высокоэнергетической фосфатной группы от молекулы-донора на АДФ катализируемый соответствующими киназами. Реакциями такого типа являются реакции субстратного фосфорилирования на пути анаэробного превращения Сахаров. У прокариот, имеющих ЦТК, реакция превращения сукцинил-КоА в янтарную кис лоту сопровождается запасанием энергии в фосфатной связь ГТФ, который затем отдает фосфатную группу АДФ. Эту реакцию можно рассматривать как реакцию субстратного фосфорилирования второго типа.
АТФ образуется также за счет энергии Dm в процессе мембранзависимого фосфорилирования. В общих чертах этот механизм фосфорилирования изложен в следующем разделе.
Молекула АТФ содержит две макроэргические фосфатные связи, при гидролизе которых высвобождается значительное количество свободной энергии:
АТФ + H2 ® АДФ + ФН; DG0' = –31,8 кДж/моль; АДФ + H2 ® АМФ + ФН; DG0' = –31,8 кДж/моль; Отщепление последней фосфатной группы от молекулы АМФ приводит к значительно меньшему высвобождению свободной энергии:
АМФ + H2 ® аденозин + ФН; DG0' = –14,3 кДж/моль; Молекула АТФ обладает определенными свойствами, которые и привели к тому, что в процессе эволюции ей была отведена столь важная роль в энергетическом метаболизме клеток. Термодинамически молекула АТФ нестабильна, что вытекает из большой отрицательной величины DG ее гидролиза. В то же время скорость неферментативного гидролиза АТФ в нормальных условиях очень мала, т. е. химически молекула АТФ высокостабильна. Последнее свойство обеспечивает эффективное сохранение энергии в молекуле АТФ, поскольку химическая стабильность молекулы препятствует тому, чтобы запасенная в ней энергия бесполезно рассеивалась в виде тепла. Малые размеры молекулы АТФ позволяют ей легко диффундировать в различные участки клетки, где необходим подвод энергии извне для выполнения химической, осмотической, механической работы.
И наконец, еще одно свойство молекулы АТФ, обеспечившее ей центральное место в энергетическом метаболизме клетки. Изменение свободной энергии при гидролизе АТФ составляет — 31,8 кДж/моль. Если сравнить эту величину с аналогичными величинами для ряда других фосфорилированных соединений, то мы получим определенную шкалу. На одном из ее полюсов будут расположены фосфорилированные соединения, гидролиз которых приводит к высвобождению значительного количества свободной энергии (высокие отрицательные значения DG). Это так называемые "высокоэнергетические соединения". На другом полюсе будут располагаться фосфорилированные соединения, DG гидролиза которых имеет невысокое отрицательное значение ("низкоэнергетические" соединения). Пример высокоэнергетического соединения — фосфоенолпировиноградная кислота (DG0' = –58,2 кДж/моль), низкоэнергетического — глицеро-1-фосфат (DG0' =—9,2 кДж/моль). АТФ на этой шкале занимает промежуточное положение, что и дает ему возможность наилучшим образом выполнять энергетические функции: переносить энергию от высокоэнергетических к низкоэнергетическим соединениям.
Если часто АТФ называют "энергетической валютой клетки, то, продолжая эту аналогию, можно сказать, что "валютная единица" выбрана клеткой в процессе эволюции весьма рационально. Порция свободной энергии в макроэргической фосфатной связи АТФ — это как раз та энергетическая порция, использование которой в биохимических реакциях делает клетку высокоэффективным энергетическим механизмом.
Dmh+ — вторая универсальная форма клеточной энергии
В течение длительного времени считали, что АТФ и другие высокоэнергетические соединения, находящиеся в равновесии с ним, представляют собой единственную форму энергии, которая может использоваться живыми клетками во всех энергозависимых процессах. Вопрос о характере связи между транспортом электронов, с одной стороны, и превращением фосфорных соединений, с другой, долгое время оставался неясным. Было установлено, что использование энергетических ресурсов (органических или неорганических соединений при дыхании, света при фотосинтезе) связано с переносом электронов по цепи, состоящей из белковых и небелковых компонентов, способных к обратимому окислению — восстановлению. В результате этого переноса освобождающаяся на отдельных участках дыхательной или фотосинтетической цепи энергия трансформируется в химическую энергию фосфатных связей АТФ. Молекулярный механизм фосфорилирования, сопряженный с электронным транспортом, был неизвестен.
Позднее были получены экспериментальные данные о существовании еще одной формы энергии, также используемой клеткой для совершения разного рода работы. Открытие этой формы энергии принадлежит английскому биохимику Питеру Митчеллу (Р. Mitchell), разработавшему в 60-х гг. хемиосмотическую теорию энергетического сопряжения, объясняющую превращение (трансформацию) энергии, освобождающейся при электронном транспорте, в энергию фосфатной связи АТФ. П. Митчелл постулировал, что при переносе электронов по окислительно-восстановительной цепи, локализованной в мембранах определенного типа, называемых энергопреобразующими, или сопрягающими, происходит неравномерное распределение H+ в пространстве по обе стороны мембраны (рис. 25). Предложенная им модель предусматривает определенное расположение переносчиков электронов в сопрягающей мембране, например ЦПМ, которые могут быть погружены в глубь мембраны или локализованы у наружной и внутренней ее поверхностей так, что образуют "петли" в цепи переноса электронов. В каждой "петле" (у прокариот электронтранспортные цепи в сопрягающих мембранах могут формировать разное число "петель") два атома водорода движутся от внутренней стороны ЦПМ к наружной с помощью переносчика водорода (например. хинона). Затем два электрона возвращаются к внутренней стороне мембраны с помощью соответствующего электронного переносчика (например, цитохрома), а два протона освобождаются во внешнюю среду.
| Рис. 25. Схема переноса электронов и протонов по электронтранспортной цепи и протонной АТФ-синтазы: АНг и В — донор и акцептор электронов соответственно; 1, 2, 3 — компоненты электронтранспортной цепи. Объяснения см. в тексте |
Таким образом, в каждой окислительно-восстановительной "петле" два H+ переносятся из цитоплазмы клетки во внешнюю среду. Общее число протонов, перенесенных через ЦПМ и выделенных во внешнюю среду, при переносе двух электронов по электронтранспортной цепи зависит от числа образуемых ею окислительно-восстановительных "петель". Расположение переносчиков электронов в ЦПМ прокариот таково, что при работе любой электронтранспортной цепи (фотосинтетической или дыхательной) во внешней среде происходит накопление ионов водорода (протонов), приводящее к подкислению среды, а в клеточной цитоплазме — их уменьшение, сопровождающееся ее подщелочением, т. е. на мембране возникает ориентированный поперек (трансмембранный) градиент ионов водорода.
Поскольку H+ — химические частицы, несущие положительный заряд, неравномерное их накопление по обе стороны мембраны приводит к возникновению не только химического (концентрационного) градиента этих частиц, но и ориентированного поперек мембраны электрического поля (суммарный положительный заряд, где происходит накопление H+, и отрицательный заряд по другую сторону мембраны). Таким образом, при переносе электронов на ЦПМ возникает трансмембранный электрохимический градиент ионов водорода, обозначаемый символом DmH+, и измеряемый в вольтах (В, мВ), который состоит из электрического (трансмембранная разность электрических потенциалов Dy) и химического (концентрационного) компонентов (градиент концентраций H+ — D pH). Измерения показали, что на сопрягающих мембранах прокариот при работе дыхательных и фотосинтетических электронтранспортных цепей DmH+ достигает 200–250 мВ, при этом вклад каждого компонента непостоянен. Он зависит от физиологических особенностей организма и условий его культивирования.
Часть свободной энергии, высвобождаемой в окислительно-восстановительных реакциях, может быть использована для синтеза АТФ, который служит важнейшим, но не единственным переносчиком энергии в клетке. Помимо АТФ в метаболизме клетки участвуют другие богатые энергией соединения, к ним относятся другие нуклеотид ди- и трифосфаты, аденозинфосфосульфат, ацилфосфаты (например, карбамоилфосфат), фосфоенолпируват. Важнейшим макроэргическим соединением для анаэробов служит ацетил-КоА. Однако все эти соединения обмениваются с АТФ и поэтому представления об АТФ, как универсальном переносчике энергии, достаточно.
АТФ может синтезироваться путем субстратного фосфори-лирования, чаще всего за счет переноса фосфорильной группы от богатого энергией соединения на АДФ. Такой способ реализуется при гликолизе, разнообразных видах брожения и некоторых других процессах. Субстратное фосфорилирование осуществляется в цитоплазме и может быть воспроизведено в бесклеточных экстрактах.
Второй механизм синтеза АТФ, мембранное фосфорилирова-ние, необходимо зависит от наличия энергизованной мембраны и связан с использованием энергии трансмембранного электрохимического градиента ионов (в общем случае Δμl), чаще всего ионов водорода (Δμ,Н). Этот механизм реализуется в процессах дыхания (окислительное фосфорилирование) и фотосинтеза (фотофосфорилирование).
Окислительно-восстановительные реакции, в результате которых бактерии получают энергию, представляют собой перенос электронов от окисляемого вещества (донора электронов) к окислителю (акцептору). Перенос электронов от донора к акцептору осуществляется по градиенту редокс-потенциала через ряд последовательно функционирующих переносчиков. Часть из них закреплена в мембране, а часть находится в цитоплазме и сопрягает эти два компонента клетки. Набор переносчиков характерен для каждого организма.
Комплекс переносчиков электронов работает как универсальная структура для всех окисляемых веществ, лишь бы в метаболизме была реакция, совмещающая окислительное преобразование субстрата с цепью переноса электронов, на конце которой находится окислитель, например для О2 - цитохромоксидаза. Вместе с тем универсальным продуктом реакции должна быть генерация АТФ. Она осуществляется мембранным ферментом АТФ-синтазой, катализирующим синтез АТФ путем конверсии энергии трансмембранного электрохимического градиента протонов μH в энергию АТФ.
У аэробных органотрофов донором электронов служат органические вещества, окисление которых приводит к восстановлению переносчика водорода НАД в НАДН. Последний реагирует с электронтранспортной цепью. Моделью для окислительного фосфорилирования служит митохондрия эукариот (рис. 4).
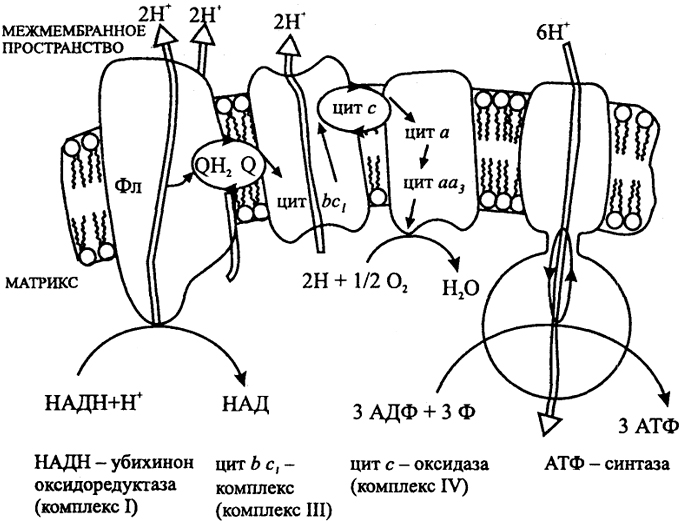
Рис. 4. Дыхательная цепь митохондрий
Цит - цитохром, Q - хинон, Фл - флавопротеин
Суммарный процесс переноса электронов разбит на три стадии, которые катализируются комплексами I, III и IV. Каждый комплекс представляет собой весьма крупное образование, построенное из многих полипептидных цепей. Первая стадия окисления НАДН катализируется комплексом I (НАДН: убихинон-оксидоредуктазой) и ведет к восстановлению убихинона Q. В состав комплекса I входит флавопротеин и FeS-кластеры. Вторая стадия, реакция окисления восстановленного убихинона и сопряженного восстановления цит с катализируется комплексом III (убихинон: цит с-оксидоредуктазой или вс1 - цитохромным комплексом). В его состав входит FeS-белок Риске, цит с1, или f, цит в. Третья стадия, перенос электронов от цит с на О2, катализируется комплексом IV, цитохромоксидазой. Перенос электронов сопряжен с переносом протонов через сопрягающую мембрану и генерацией ΔμН. Превращение энергии ΔμН в энергию АТФ осуществляется АТФ-синтазой.
У фотосинтезирующих организмов процессы преобразования световой энергии, приводящие к синтезу АТФ и образованию восстановителя, необходимого, например, для фиксации СO2, включают следующие этапы. Энергия света поглощается пигментами светособирающих антенных комплексов и передается в реакционный центр (РЦ), в котором происходит превращение электромагнитной формы энергии в энергию электрохимического
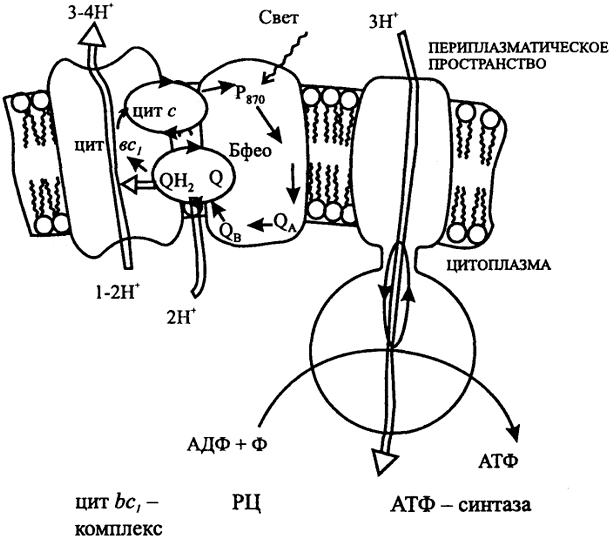
Рис. 5. Цепь переноса электронов при фотосинтезе А. Аноксигенный фотосинтез (пурпурные бактерии)
Р870 - бактериохлорофилл; Бфео - бактериофеофитин; Q - хинон (Q, - плас-тохинон); цит - цитохром; Р680' Р700 - хлорофилл; Фео - феофитин; Фд - фер-редоксин; ПЦ - пластоцианин; ФС - фотосистема; РЦ - реакционный центр; ФНР - ферредоксин:НАДФ оксидоредуктаза.
Электроны от фотовозбужденного Р870 передаются на убихинон Q, восстанавливая его, далее на цит bс1, комплекс и через цит с и c1, возвращаются к молекуле окисленного Р870. Перенос электронов сопряжен с трансмембранным переносом протонов при окислении убихинопа цит bc1, комплексом, что ведет к генерированию ΔμH. Результатом циклического переноса электронов является синтез АТФ.
разделения разрядов. Фотохимически активный хлорофилл (или бактериохлорофилл) РЦ, обозначаемый обычно буквой Р (от англ, pigment), переходит в электронно-возбужденное состояние и окисляется, отдавая электрон первичному акцептору. Перенос электрона на вторичный акцептор и восстановление окисленного Р первичным донором электронов стабилизирует разделение зарядов в РЦ. Дальнейшие процессы связаны с переносом электрона по электронтранспортной цепи, сопряженным с синтезом АТФ
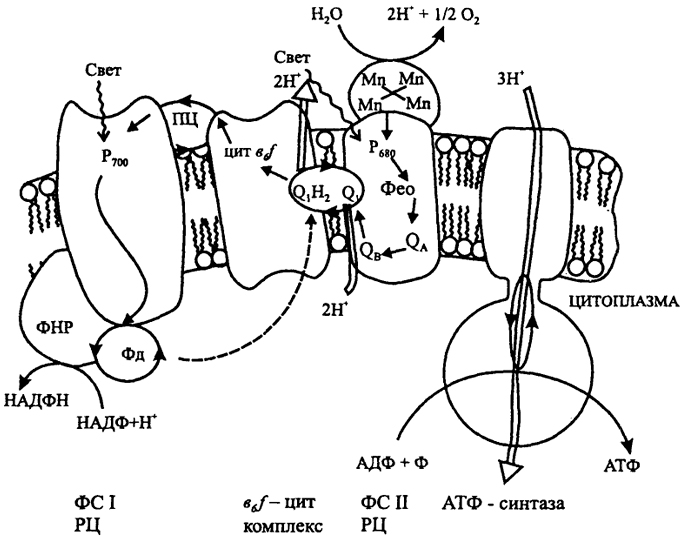
Б. Оксигенный фотосинтез
У оксигенных фототрофов имеются две фотосистемы: ФС I (с Р700) и ФС II (с Р680). В состав ФС II входит Mn-содержащий комплекс, осуществляющий разложение Н2О. Электроны от фотовозбужденного Р680 через ряд переносчиков РЦ передаются на пластохинон, далее в цит b6f комплекс и через пластоцианин на Р700. От фотовозбужденного Р700 (через ряд переносчиков РЦ) электроны поступают на Фд, связывающий ФС I с НАДФ-редуктазой (ФНР), которая восстанавливает НАДФ. Таким образом, происходит последовательный перенос электронов от воды к НАДФ. Реакции электронного транспорта, связанные с разложением воды в ФС II и окислением молекулы пластохинола цит b6f комплексом, сопровождаются трансмембранным переносом протонов, сопряженным с генерированием ΔμH и синтезом АТФ. Образование АТФ возможно и в результате связанного с ФС I циклического преноса электронов (показан пунктиром).
(рис. 5 А, Б). Природа акцепторов электронов в РЦ и состав переносчиков электронов у разных групп фототрофов различаются. Существенно, что часть переносчиков являются общими для фотосинтетической и дыхательной электронтранспортной цепи, обусловливая у бактерий взаимосвязь процессов фотосинтеза и дыхания.
Различают циклический или нециклический пути переноса электронов. Циклический путь, свойственный, например, пурпурным бактериям, обеспечивает синтез АТФ (см. рис. 5 А), но не восстановителя. Поэтому восстановление НАД у этих микроорганизмов происходит в результате АТФ-зависимого обратного переноса электронов. У зеленых серобактерий перенос электронов осуществляется по нециклическому пути, обеспечивая синтез АТФ и восстановление НАД. Донорами электронов у аноксигенных, т.е. не выделяющих О2, организмов служат восстановленные соединения серы, S°, H2, Fe2+ или некоторые органические вещества. Цианобактерии и эукариотные фототрофы используют в качестве донора электронов Н2О и осуществляют фотосинтез с выделением О2 - оксигенный. В отличие от аноксигенных бактерий, имеющих одну фотосистему (ФС), у них последовательно функционируют две фотосистемы (см. рис. 5 Б) и может осуществляться как нециклический (так называемая Z-схема), так и индуцируемый ФС I циклический перенос электронов. Окисление Н2О осуществляется Mn-содержащим комплексом, связанным с ФС П. Особый тип фотосинтеза известен у экстремально галофильных архебактерий (галобактерий). В этом случае трансмембранный перенос Н+ и конверсия энергии света в энергию ΔμH с последующим синтезом АТФ осуществляются в результате светоиндуцированных преобразований бактериородопсина - пигмент-белкового комплекса, содержащего каротиноид ретиналь.
| Брожение-это такой метаболический процесс, при котором регенерируется АТР, а продукты расщепления органического субстрата могут служить одновременно и донорами, и акцепторами водорода. Реакции, приводящие к фосфорилированию ADP, являются реакциями окисления. От окисленного углерода клетка избавляется, выделяя С02. Отдельные этапы окисления представляют собой дегидрирование, при котором водород переносится на NAD. Акцепторами водорода, находящегося в составе NADH2, служат промежуточные продукты расщепления субстрата. При регенерации NAD последние восстанавливаются, а продукты восстановления выводятся из клетки. При сбраживании углеводов и ряда других веществ образуются (по отдельности или в смеси) такие продукты, как этанол, лактат, пропио-нат, формиат, бутират, сукцинат, капронат, ацетат, н-бутанол, 2,3-бутан-диол, ацетон, 2-пропанол, С02 и Н2. В зависимости от того, какие продукты преобладают или являются особенно характерными, различают спиртовое, молочнокислое, пропионовокислое, муравьинокислое, масля-нокислое и уксуснокислое брожение. Молекулярный кислород в процессах брожения не участвует: «Брожение-это жизнь без воздуха» (Л. Па-стер). Многие микроорганизмы, осуществляющие брожение,-обли-гатные анаэробы, а некоторые-факультативные анаэробы, способные расти как в присутствии кислорода, так и без него; при этом кислород подавляет брожение и оно сменяется дыханием. Регенерация АТР при брожении. При сбраживании глюкозы микроорганизмами образуется от 1 до 4 молей АТР: Продукты C*DP)+ Pj 1-4 С*Т?) Ввиду большого числа возможных продуктов брожения кажется удивительным, что в преобразовании энергии путем фосфорилирования на уровне субстрата участвуют лишь немногие реакции, из которых здесь будут представлены три наиболее важные: У большинства микроорганизмов, осуществляющих брожение, используются только реакции, катализируемые фосфоглщераткиназой (1) или пируваткиназой (2), а необходимые акцепторы водорода образуются при этом из пирувата и ацетилкофермента А. При сбраживании одного моля глюкозы образуется лишь от двух до трех молей АТР, а продуктами оказываются лактат, этанол, ацетон, бутират, н-бутанол, 2-пропа-нол, 2,3-бутандиол, капронат, ацетат, С02 и молекулярный водород. При использовании ацетаткиназы [реакция (3)] бактерии получают дополнительный АТР. Ацетилфосфат образуется из ацетил-СоА и неорганического фосфата с помощью фосфотрансацетилазы: Ацетил-СоА + Р; -* Ацетилфосфат + СоА Кроме того, возможно образование ацетилфосфата из фосфорилиро-ванных Сахаров (ксилулозо-5-фосфата, фруктозо-6-фосфата) при участии фосфокетолазы. Способность бактерий использовать реакцию, катализируемую аце-таткиназой (3), зависит от того, могут ли они выделять молекулярный водород (Н2). В случае переноса восстановительных эквивалентов (электронов) на протоны они могут выделяться в виде молекулярного водорода; поэтому клетке нет надобности синтезировать акцепторы водоро- да. Чтобы понять это, нужно остановиться на механизмах высвобождения Н2. Анаэробные бактерии окисляют пируват в ацетил-СоА двумя способами (см. реакции (2) и (3) в начале раздела 7.2.4). В реакции, катализируемой пируват : ферредоксин-оксидоредуктазой (эта реакция свойственна, в частности, клостридиям), восстанавливается ферредоксин (Fd). Его окислительно-восстановительный потенциал очень низок (Е° = = - 420 мВ), поэтому с помощью специальной гидрогеназы-ферредоксин :Н2-оксидоредуктазы-может освобождаться газообразный водород: В реакции, катализируемой пируват: формиат-лиазой (как у энтеробак-терий), наряду с ацетил-СоА образуется также формиат. Он может расщепляться гидрогенлиазной системой: Формиат---- ► н2 + С02 Оба механизма выделения Н2 имеют между собой то общее, что у предшественников (FdH и формиата) очень низкие окислительно-восстановительные потенциалы. Поэтому клетке нетрудно избавляться от восстановительных эквивалентов, образующихся при окислении пирува-та в ацетил-СоА. В отличие от этого водород, образующийся при дегидрировании глицеральдегид-3-фосфата и связанный в форме NADH2, у большинства анаэробных бактерий передается затем на органические акцепторы. Многие бактерии обладают, однако, способностью высвобождать и эти восстановительные эквиваленты в виде Н2 благодаря ферменту NADH2 : ферредоксин-оксидоредуктазе, катализирующему реакцию NADH2 + 2 Fd-- ► NAD + 2 FdH С помощью гидрогеназы от FdH может отделяться Н2. Так как эти реакции связаны с увеличением потенциала Н (от £„' = - 320 мВ для NADH2 до £„' = - 420 мВ для ферредоксина) и их равновесие неблагоприятно для выделения Н2, они протекают только тогда, когда образующийся и выделяющийся молекулярный водород непрерывно удаляется. Поэтому организмы, способные к образованию Н2 из NADH2, могут воспользоваться этим изящным способом избавления от водорода в форме Н2 только тогда, когда живут вместе с другими видами, непрерывно потребляющими Н2. Именно так обычно обстоит дело в природе. Такое явление называют межвидовой передачей водорода и говорят об особой форме симбиоза в микробных сообществах. Бактерии, способные таким образом избавляться от связанного с NAD водорода, выделяя его в виде Н2, естественно, могут обходиться без превращения ацетил-СоА в акцепторы для NADH2. Поэтому они могут превращать ацетил-СоА в ацетилфосфат и регенерировать АТР путем ацетилкиназнои реакции. Выделяют они главным образом ацетат и при сбраживании одного моля глюкозы способны регенерировать до четырех молей АТР (как, например, Ruminococcus albus; см. стр. 299). Роль процессов брожения в балансе природы. Виды, осуществляющие брожение, играют важную роль в природном круговороте веществ. Большая часть целлюлозы, поедаемой растительноядными животными, выводится в непереваренном виде с калом. Когда этот содержащий целлюлозу детрит попадает в анаэробные слои почвы или донных осадков водоемов, целлюлозу сбраживают разлагающие ее клостридии и некоторые другие строго анаэробные бактерии. При этом образуются названные выше продукты брожения, в том числе почти всегда молекулярный водород. Водород находится в начале анаэробной пищевой цепи, главные продукты которой метан и (или) сероводород: В осадках пресноводных озер и в рубце жвачных Н2 превращается метанобразующими бактериями в метан, а в морских анаэробных экосистемах сульфатредуцирующие бактерии превращают Н2 и сульфат в сероводород. |
| <== предыдущая лекция | | | следующая лекция ==> |
| ЗАКЛЮЧЕНИЕ. Проблема конституции имеет многовековую историю, до настоящего времени нет общепринятой формулировки этого понятия | | | Ознакомление с представленной документацией |
Дата добавления: 2015-07-22; просмотров: 5971;
