Базальные ядра
Базальные ядра обеспечивают двигательные функции,.отличные от таковых, контролируемых пирамидным (кортико-спинальным) трактом. Термин экстрапирамидный подчеркивает это различие и относится к ряду заболеваний, при которых поражаются базальные ядра. К семейным заболеваниям относят болезнь Паркинсона, хорею Гентингтона и болезнь Вильсона. В этом параграфе рассматривается вопрос о базальных ядрах и описываются объективные и субъективные признаки нарушений их деятельности.
Анатомические связи и нейротрансмиттеры базальных ядер. Базальные ядра представляют собой парные подкорковые скопления серого вещества, образующие обособленные группы ядер. Основными являются хвостатое ядро и скорлупа (вместе формирующие полосатое тело), медиальная и латеральная пластинки бледного шара, субталамическос ядро и черное вещество (рис. 15.2). Полосатое тело получает афферентные сигналы из многих источников, включая кору больших полушарий, ядра зрительного бугра, ядра шва ствола мозга и черное вещество. Корковые нейроны, связанные с полосатым телом, выделяют глутаминовую кислоту, обладающую возбуждающим эффектом. Нейроны ядер шва, связанные с полосатым телом, синтезируют и выделяют серотонин. (5-ГТ). Нейроны компактной части черного вещества синтезируют и выделяют дофамин, который воздействует на нейроны полосатого тела в качестве тормозного медиатора. Трансмиттеры, выделяемые проводниками таламуса, не определены. Полосатое тело содержит 2 вида клеток: местные обходные нейроны, аксоны которых не выходят за пределы ядер и остальные нейроны, аксоны которых идут к бледному шару и черному веществу. Местные обходные нейроны синтезируют и выделяют ацетилхолин, гамма-аминомасляную кислоту (ГАМК) и нейропептиды, такие как соматостатин и вазоактивный интестинальный полипептид. Нейроны полосатого тела, обладающие подавляющим воздействием на ретикулярную часть черного вещества, выделяют ГАМК, тогда как те, которые возбуждают черное вещество, выделяют субстанцию Р (рис. 15.3). Стриарные проекции к бледному шару выделяют ГАМК, энкефалины и субстанцию Р.
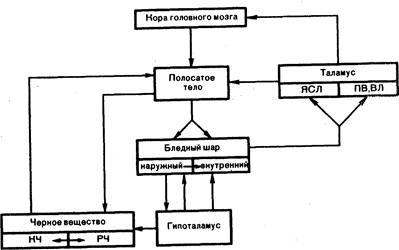
Рис. 15.2. Упрощенная схематическая диаграмма основных нейрональных связей между базальными ядрами, зрительным бугром и корой больших полушарий.
Проекции из медиального сегмента бледного тара образуют основной эфферентный проводящий путь от базальных ядер. КЧ — компактная часть, РЧ — ретикулярная часть, ЯСЛ — ядра средней линии, ПВ — передневентральное, ВЛ — вентролатеральное.
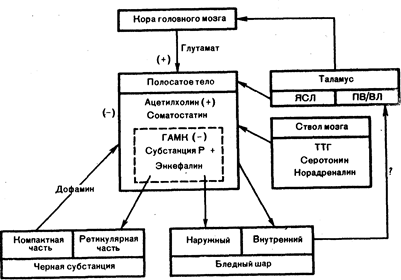
Рис. 15.3. Схематическая диаграмма стимулирующих и тормозных влияний нейрорегуляторов, выделяемых нейронами проводящих путей базальных ядер. Область полосатого тела (очерченная штриховой линией) указывает нейроны с эфферентными проекционными системами. Другие трансмиттеры полосатого тела находятся во внутренних нейронах. Знак + означает возбуждающее ностсинаптнческое влияние. Знак -- означает тормозное влияние. ЯСЛ — ядра средней линии. ГАМК—g-амнномасляная кислога; ТТГ --тиреотропный гормон. ПВ/ВЛ -- нередневентральное и вентролатералыюе.
Аксоны, выходящие из медиального сегмента бледного шара, образуют основную эфферентную проекцию базальных ядер. Существует значительное количество проекций, проходящих через внутреннюю капсулу или рядом с ней (петля и лентикулярный пучок, проходящие через поля Фореля) к переднему и латеральному вентральным ядрам таламуса, а также к внутрипластинчатым ядрам таламуса, включая парацентральное ядро. Медиаторы этого пути неизвестны. К другим эфферентным проекциям базальных ядер относят прямые дофаминергические связи между черным веществом и лимбической областью и корой лобных отделов больших полушарий, ретикулярная часть черного вещества также посылает проекции в ядра таламуса и к верхнему бугорку.
Современные морфологические исследования выявили распределение восходящих волокон из таламуса в коре головного мозга. Вентральные таламические нейроны проецируются в премоторную и моторную зоны коры; медиальные ядра таламуса проецируются в первую очередь в префронтальную область коры. Дополнительная двигательная кора получает множество проекций со стороны базальных ядер, включая дофаминергическую проекцию из черного вещества, тогда как первичная двигательная кора и премоторная область получают множество проекций из мозжечка. Таким образом, имеется ряд параллельных петель, соединяющих специфические образования базальных ядер с корой больших полушарий. Хотя точный механизм, посредством которого различные сигналы превращаются в координированное целенаправленное действие, остается неизвестным, ясно, что значительное влияние со стороны базальных ядер и мозжечка на двигательную кору во многом обусловлено влиянием ядер зрительного бугра. Основные проекции мозжечка, проходящие через верхнюю ножку мозжечка, оканчиваются вместе с волокнами, идущими от бледного шара в вентральном переднем и вентролатеральном ядрах зрительного бугра. В этой части таламуса образуется широкая петля, состоящая из восходящих волокон от базальных ядер и мозжечка к двигательной коре. Несмотря на явную значимость этих образований, стереотаксическая деструкция вентральных отделов таламуса может приводить к исчезновению проявлений семейного эссенциального тремора, а также ригидности и тремора при болезни Паркинсона, не вызывая функциональных расстройств. Восходящие таламокортикальные волокна проходят через внутреннюю капсулу и белое вещество, так что при возникновении очагов поражения в этой области в патологический процесс могут одновременно вовлекаться и пирамидная, и экстрапирамидная системы.
Аксоны некоторых корковых нейронов образуют внутреннюю капсулу (кортико-спинальный и кортико-бульбарный пути); они также проецируются в полосатое тело. Образуется завершенная петля — от коры головного мозга к полосатому телу, затем к бледному шару, к таламусу и вновь к коре головного мозга. Аксоны, выходящие из парацентрального ядра таламуса, отдают проекции назад, к полосатому телу, завершая, таким образом, петлю подкорковых ядер — от полосатого тела к бледному шару, затем к парацентральному ядру и вновь к полосатому телу. Существует еще одна петля базальных ядер между полосатым телом и черным веществом. Дофаминергические нейроны компактной части черного вещества проецируются в полосатое тело, а отдельные нейроны полосатого тела, выделяющие ГАМК и субстанцию Р, посылают проекции в ретикулярную часть черного вещества. Существует реципрокная связь между ретикулярной и компактной частями черного вещества; ретикулярная часть посылает проекции к вентральному отделу зрительного бугра, верхнему бугорку, а также к ретикулярной формации ствола мозга. Субталамическое ядро получает проекции из образований новой коры и из латерального сегмента бледного шара; нейроны внутри субталамического ядра образуют реципрокные связи с латеральным сегментом бледного шара, а также посылают аксоны к медиальному сегменту бледного шара и ретикулярной части черного вещества. Нейрохимические агенты, участвующие в этих процессах, остаются неизвестными, хотя выявлено участие ГАМК.
Физиология базальных ядер. Записи активности нейронов бледного шара и черного вещества в состоянии бодрствования, выполненные у приматов, подтвердили, что основной функцией базальных ядер является обеспечение двигательной деятельности. Эти клетки участвуют в самом начале процесса движения, так как их активность усиливалась перед тем, как движение становилось видимым и определяемым при ЭМГ. Повышение активности базальных ядер было связано преимущественно с движением контралатеральной конечности. Большинство нейронов повышают свою активность во время медленных (плавных) движений, активность других усиливается во время быстрых (баллистических) движений. В медиальном сегменте бледного шара и ретикулярной части черной субстанции существует соматотопическое распределение для верхней и нижней конечностей и лица. Эти наблюдения дали возможность объяснить существование ограниченных дискинезий. Очаговая дистония и поздняя дискинезия могут возникнуть при локальных нарушениях биохимических процессов в бледном шаре и черном веществе, поражающих только те области, в которых имеется представительство руки или лица.
Хотя базальные ядра являются двигательными по функциям, нельзя установить особый вид движений, опосредованный деятельностью этих ядер. Гипотезы о функциях базальных ядер у человека строятся на основании полученных корреляций между клиническими проявлениями и локализацией очагов поражения у больных с нарушениями экстрапирамидной системы. Базальные ядра являются скоплением ядер вокруг бледного шара, через который импульсы посылаются в зрительный бугор и дальше к коре головного мозга (см. рис. 15.2). Нейроны каждого вспомогательного ядра вырабатывают возбуждающие и тормозные импульсы, и сумма этих воздействий на основной путь от базальных ядер к зрительному бугру и коре головного мозга при определенном влиянии со стороны мозжечка определяет плавность движений, выражаемых посредством кортико-спинального и других нисходящих кортикальных путей. Если повреждается одно или несколько вспомогательных ядер, меняется сумма импульсов, поступающих в бледный шар, и могут возникать двигательные расстройства. Наиболее ярким из них является гемибаллизм; поражение субталамического ядра, по-видимому, снимает тормозное влияние черного вещества субстанции и бледного шара, что приводит к появлению насильственных непроизвольных резких вращательных движений руки и ноги на противоположной поражению стороне. Таким образом, поражение хвостатого ядра часто приводит к возникновению хореи, а противоположный феномен — акинезии, в типичных случаях развивается при дегенерации клеток черного вещества, вырабатывающих дофамин, освобождая интактное хвостатое ядро от тормозных влияний. Поражения бледного шара часто приводят к развитию торсионной дистонии и нарушению постуральных рефлексов.
Основные принципы нейрофармакологии базальных ядер. У млекопитающих в передаче информации от одной нервной клетки к другой обычно участвует один или несколько химических агентов, выделяемых первым нейроном в специальный участок рецептора второго нейрона, изменяя, таким образом, его биохимические и физические свойства. Эти химические агенты называют нейрорегуляторами. Выделяют 3 класса нейрорегуляторов: нейротрансмиттеры, нейромодуляторы и нейрогормональные вещества. Нейротрансмиттеры, такие как катехоламины, ГАМК и ацетилхолин, являются наиболее известным и клинически значимым классом нейрорегуляторов. Они вызывают коротколатентные кратковременные постсинаптические эффекты (например, деполяризацию) вблизи от места своего выделения. Нейромодуляторы, такие как эндорфины, соматостатин и субстанция Р, также действуют в зоне выделения, но обычно не вызывают деполяризации, Нейромодуляторы, по-видимому, могут усиливать или ослаблять влияние классических нейротрансмиттеров. Многие нейроны, содержащие классические нейротрансмиттеры, также накапливают и нейромодуляторные пептиды. Например, субстанция Р содержится в нейронах шва ствола мозга, синтезирующих 5-ГТ, а вазоактивный интестинальный пептид вместе с ацетилхолином — во многих кортикальных холинергических нейронах. Нейрогормональные вещества, такие как вазопрессин и ангиотензин II, отличаются от остальных нейрорегуляторов тем, что выделяются в кровеносное русло и транспортируются к отдаленным рецепторам. Их эффекты первоначально развиваются медленнее и имеют большую продолжительность действия. Отличия между различными классами нейрорегуляторов не являются абсолютными. Дофамин, например, действует как нейротрансмиттер в хвостатом ядре, однако по механизму действия в гипоталамусе является нейрогормоном.
Наиболее хорошо изучены нейротрансмиттеры базальных ядер. Кроме того, они более подвержены воздействию лекарственных препаратов. Нейротрансмиттеры синтезируются в пресинаптических окончаниях нейронов, а некоторые, например катехоламины и ацетилхолин, накапливаются в везикулах. При поступлении электрического импульса нейротрансмиттеры выделяются из пресинаптического окончания в синаптическую щель, распространяются в ней и соединяются с особыми участками рецепторов постсинаптической клетки, инициируя ряд биохимических и биофизических изменений; сумма всех постсинаптических возбуждающих и тормозных воздействий определяет, вероятность того, что произойдет разряд. Биогенные амины дофамин, норадре-иалин и 5-ГТ инактивируются путем обратного захвата пресинаптическими окончаниями. Ацетилхолин инактивируется путем внутрисинаптического гидролиза. Кроме того, на пресинаптических окончаниях имеются рецепторные участки, называемые ауторецепторами, раздражение которых обычно приводит к снижению синтеза и выделения трансмиттера. Сродство ауторецептора со своим нейротрансмиттером часто бывает значительно более высоким, чем у постсинаптического рецептора. Препараты, возбуждающие ауторецепторы дофамина, должны уменьшать» дофаминергическую передачу и, вероятно, могут быть эффективны для лечения таких гиперкинезов, как хорея Гентингтона и поздняя дискинезия. По характеру ответной реакции на воздействие различных фармакологических агентов. рецепторы разделяют на группы. Существует по меньшей мере две популяции рецепторов дофамина. Например, раздражение участка Д1 активирует аденилатциклазу, тогда как возбуждение участка Д2 такого эффекта не оказывает. Алкалоид спорыньи бромокриптин, использующийся при лечении болезни Паркинсона, активирует рецепторы Д2 и блокирует рецепторы Д1. Большинство нейролептиков блокируют рецепторы Д2.
Клинические проявления поражения базальных ядер. Акинезия. Если разделять экстрапирамидные заболевания на первичные нарушения функций (отрицательный признак, обусловленный повреждением связей) и вторичные эффекты, связанные с выделением нейрорегуляторов (положительный признак, обусловленный повышенной активностью), то акинезия является выраженным отрицательным признаком или синдромом дефицита. Акинезия — это неспособность больного самому активно начинать движение и выполнять обычные произвольные движения легко и быстро. Проявление меньшей степени выраженности определяется терминами брадикинезия и гипокинезия. В отличие от паралича, который является отрицательным признаком, обусловленным поражением кортико-спинального тракта, в случае акинезии сила мышц сохраняется, хотя отмечается запаздывание в достижении максимальной силы. Акинезию также следует отличать от апраксии, при которой требование выполнить определенное действие никогда не достигает двигательных центров, управляющих искомым движением. Акинезия приносит наибольшие неудобства людям, страдающим болезнью Паркинсона. У них возникает тяжелейшая обездвиженность, резкое снижение активности; они довольно долго могут сидеть практически без движения, не изменяя положения тела, тратят вдвое больше времени по сравнению со здоровыми людьми на такие повседневные действия, как питание, одевание и умывание. Ограниченность движений проявляется в потере автоматических содружественных движений, таких как моргание и свободное размахивание руками при ходьбе. Вследствие акинезии, по-видимому, развиваются такие известные симптомы болезни Паркинсона, как гипомимия, гипофония, микрография и затрудненные вставание со стула и начало ходьбы. Хотя патофизиологические подробности остаются неизвестными, клинические проявления .акинезии подтверждают гипотезу о том, что базальные ядра в значительной степени влияют на начальные этапы движения и автоматическое выполнение приобретенных двигательных навыков.
Нейрофармакологические данные дают основание предполагать, что сама по себе акинезия является результатом дефицита дофамина.
Ригидность. Мышечным тонусом называют уровень сопротивления мышц при пассивном движении расслабленной конечности. Для ригидности характерно длительное пребывание мышц в сокращенном состоянии, а также постоянное сопротивление пассивным движениям. При экстрапирамидных заболеваниях ригидность на первый взгляд может напоминать спастичность, возникающую при поражениях кортико-спинального тракта, поскольку в обоих случаях происходит повышение мышечного тонуса. Дифференциальную диагностику можно провести по некоторым клиническим особенностям этих состояний уже при осмотре больного. Одним из различий ригидности и спастичности является характер распределения повышенного мышечного тонуса. Хотя ригидность развивается как в мышцах-сгибателях, так и в разгибателях, более выраженной она бывает в тех мышцах, которые способствуют сгибанию туловища. Легко определить ригидность больших групп мышц, однако она возникает и в мелких мышцах лица, языка и глотки. В отличие от ригидности спастичность, как правило, приводит к повышению тонуса в мышцах-разгибателях нижних конечностей и в мышцах-сгибателях верхних конечностей. В дифференциальной диагностике этих состояний используют также качественное исследование гипертонуса. При ригидности сопротивление пассивным движениям остается постоянным, что дает основание называть его «пластическим» или по типу «свинцовой трубки». В случае спастичности может наблюдаться свободный промежуток, после которого возникает феномен «складного ножа»; мышцы не сокращаются, пока они не растянуты в значительной степени, а позже, при растяжении, мышечный тонус быстро снижается. Глубокие сухожильные рефлексы не изменяются при ригидности и оживляются при спастичности. Повышенная активность рефлекторной дуги растяжения мышцы приводит к возникновению спастичности вследствие центральных изменений, без повышения чувствительности мышечного веретена. Спастичность исчезает при перерезке задних корешков спинного мозга. Ригидность менее связана с повышенной активностью дуги сегментарных рефлексов и больше зависит от повышения частоты разрядов альфа-мотонейронов. Особой формой ригидности является симптом «зубчатого колеса», который особенно характерен для болезни Паркинсона. При пассивном растяжении мышцы с повышенным тонусом ее сопротивление может выражаться в ритмичном подергивании, как будто бы оно контролируется храповиком.
Хорея. Хорея — болезнь, название которой образовано от греческого слова, обозначающего пляску, относится к распространенным- аритмичным гиперкинезам быстрого, порывистого, беспокойного типа. Хореические движения отличаются крайней беспорядочностью и разнообразием. Как правило, они длительны, могут быть простыми и сложными, вовлекать любой участок тела. По сложности они могут напоминать произвольные движения, однако никогда не объединяются в координированное действие, пока больной не включит их в целенаправленное движение для того, чтобы сделать их менее заметными. Отсутствие паралича делает возможными нормальные целенаправленные движения, однако они часто бывают слишком быстрыми, неустойчивыми и деформированными под воздействием хореических гиперкинезов. Хорея может иметь генерализованный характер или ограничиваться одной половиной тела. Генерализованная хорея является ведущим симптомом при болезни Гентингтона и ревматической хореи (болезни Сиденгама), вызывающих гиперкинезы мышц лица, туловища и конечностей. Кроме того, хорея часто возникает у больных паркинсонизмом в случае передозировки леводопы. Другое известное хореиформное заболевание, поздняя дискинезия, развивается на фоне длительного приема нейролептиков. Хореическим движениям при этом заболевании бывают обычно подвержены мышцы щек, языка и челюстей, хотя в тяжелых случаях могут вовлекаться мышцы туловища и конечностей. Для лечения хореи Сиденгама применяют седативные средства, такие как фенобарбитал и бензодиазепины. Для подавления хореи при болезни Гентингтона обычно используют нейролептики. Препараты, усиливающие холинергическую проводимость, такие как фосфатидилхолин и физостигмин, применяют примерно у 30% больных поздней дискинезией.
Особая форма пароксизмальной хореи, временами сопровождающаяся атетозом и дистоническими проявлениями, встречается в виде спорадических слу чаев или наследуется по аутосомно-доминантному типу. Впервые она возникает в детском или подростковом возрасте и продолжается в течение всей жизни. У больных возникают пароксизмы, продолжающиеся в течение нескольких минут или часов. Одна из разновидностей хореи является кинезогенной, т. е. возникающей при внезапных целенаправленных движениях. Факторами, провоцирующими хорею, особенно у тех лиц, у которых в детстве выявляли болезнь Сиденгама, могут являться гипернатриемия, употребление алкоголя и прием дифенина. В некоторых случаях приступы можно предотвратить с помощью противосудорожных препаратов, включая фенобарбитал и клоназепам, а иногда и леводопы.
Атетоз. Название происходит от греческого слова, означающего неустойчивый или изменчивый. Атетоз характеризуется неспособностью удерживать мышцы пальцев рук и ног, языка и другие мышечные группы в одном положении. Возникают длительные плавные непроизвольные движения, наиболее выраженные в пальцах рук и предплечьях. Эти движения заключаются в разгибании, пронации, сгибании и супинации руки с чередующимся сгибанием и разгибанием пальцев. Атетозные движения более медленные по сравнению с хореиформными, однако имеются состояния, называемые хореоатетозом, при которых бывает трудно отличить эти два вида гиперкинезов. Генерализованный атетоз можно наблюдать у детей со статической энцефалопатией (детским церебральным параличом). Кроме того, он может развиваться в случае болезни Вильсона, торсионной дистонии и при гипоксии головного мозга. Односторонний постгемиплегический атетоз наблюдается чаще у детей, перенесших инсульт. У больных с атетозом, развившимся на фоне детского церебрального паралича или гипоксии головного мозга, отмечают и другие двигательные расстройства, возникающие вследствие сопутствующего поражения кортико-спинального тракта. Больные часто не в состоянии выполнить отдельные самостоятельные движения языком, губами и руками, попытки проделать эти движения приводят к сокращению всех мышц конечности или какой-либо другой части тела. Все разновидности атетоза вызывают ригидность различной степени выраженности, что, по-видимому, обусловливает замедленность движений при атетозе в отличие от хореи. Лечение атетоза, как правило, безуспешно, хотя у некоторых больных отмечают улучшение при приеме препаратов, использующихся для лечения хореических и дистонических гиперкинезов.
Дистонии. Дистонией называют повышение тонуса мышц, приводящее к образованию фиксированных патологических поз. У некоторых больных с дистонией позы и жесты могут меняться, становясь нелепыми и вычурными, что обусловлено неравномерными сильными сокращениями мышц туловища и конечностей. Спазмы, возникающие при дистонии, напоминают атетоз, однако более медленные и чаще охватывают мышцы туловища, чем конечностей. Явления дистонии усиливаются при целенаправленных движениях, волнении и эмоциональных перенапряжениях; они уменьшаются при расслаблении и, как большинство экстрапирамидных гиперкинезов, полностью исчезают во сне. Первичная торсионная дистония, ранее именовавшаяся деформирующей мышечной дистонией, часто наследуется по аутосомно-рецессивному типу у евреев семьи Ашкенази и по аутосомно-доминантному типу у лиц других национальностей. Описаны также спорадические случаи. Признаки дистонии обычно появляются в первые два десятилетия жизни, хотя описаны и более поздние дебюты болезни. Генерализованные торсионные спазмы могут возникать у детей, страдающих билирубиновой энцефалопатией, или в результате гипоксии головного мозга.
Термин дистония используют и в другом значении — для описания любой фиксированной позы, возникающей в результате поражения двигательной системы. Например, дистонические явления, возникающие при инсульте (согнутая рука и вытянутая нога), часто называют гемиплегической дистонией, а при паркинсонизме — сгибательной дистонией. В отличие от подобных стойких дистонических явлений некоторые препараты, такие как нейролептики и леводопа, могут спровоцировать развитие временных дистонических спазмов, исчезающих после прекращения приема препаратов.
Вторичные, или локальные, дистонии встречаются более часто, чем торсионная дистония; к ним относят такие заболевания, как спастическая кривошея, писчий спазм, блефароспазм, спастическая дистония и синдром Мейжа- В целом, при локальных дистониях симптоматика обычно остается ограниченной, стабильной и не распространяется на другие участки тела. Локальные дистонии чаще развиваются у людей среднего и старшего возраста, как правило спонтанно, без фактора наследственной предрасположенности и провоцирующих их предшествовавших заболеваний. Наиболее известной разновидностью локальной дистонии является спастическая кривошея. При этом заболевании возникает постоянное или длительное напряжение грудинно-ключично-сосцевидной, трапециевидной и других мышц шеи, обычно более выраженное с одной стороны, приводящее к насильственному повороту или наклону головы. Больной не может преодолеть эту насильственную позу, что отличает заболевание от привычного спазма или тика. Дистонические явления бывают наиболее выражены при сидении, стоянии и ходьбе; прикосновение к подбородку или челюсти часто способствует уменьшению мышечного напряжения. Женщины в возрасте 40 лет заболевают в 2 раза чаще, чем мужчины.
Торсионную дистонию относят к экстрапирамидным заболеваниям даже при отсутствии патологических изменений в базальных ядрах или других отделах головного мозга. Затруднения в подборе лекарственных препаратов усугубляются недостаточными знаниями об изменениях нейротрансмиттеров в случае данного заболевания. Лечение вторичных дистонических синдромов также не приносит заметного улучшения. В некоторых случаях положительное влияние оказывают такие седативные препараты, как бензодиазепины, а также большие дозы холинергических препаратов. Иногда положительный эффект возникает при помощи леводопы. Улучшение состояния иногда отмечают при лечении с помощью биоэлектрического управления, психиатрическое лечение не приносит пользы. При тяжелой спастической кривошее у большинства больных положительное влияние оказывает хирургическая денервация пораженных мышц (от C1 до С3 с двух сторон, С4 с одной стороны). Блефароспазм лечат с помощью инъекций ботулотоксина в мышцы, окружающие глазное яблоко. Токсин вызывает временную блокаду нервно-мышечной передачи. Лечение необходимо повторять каждые 3 мес.
Миоклонус. Этот термин используют для описания кратковременных насильственных беспорядочных мышечных сокращений. Миоклонус может развиваться спонтанно в покое, в ответ на раздражения или при целенаправленных движениях. Миоклонии могут возникать в единичной двигательной единице и напоминать фасцикуляции, или одновременно вовлекать группы мышц, в результате чего изменяется положение конечности или деформируются целенаправленные движения. Миоклонус является следствием множества генерализованных метаболических и неврологических расстройств, вместе называемых миоклониями. Постгипоксический интенционный миоклонус — это особый миоклонический синдром, развивающийся в качестве осложнения временной аноксии головного мозга, например при кратковременной остановке сердца. Умственная деятельность обычно не страдает; возникает мозжечковая симптоматика, вследствие миоклонуса, вовлекающего мышцы конечностей, лица, искажаются произвольные движения и голос. Миоклонус действия искажает все движения и в значительной степени затрудняет возможность принимать пищу, разговаривать, писать и даже ходить. Эти явления могут возникать при болезни накопления липидов, энцефалите, болезни Крейтцфельдта — Якоба или метаболических энцефалопатиях, возникающих на фоне дыхательной, хронической почечной, печеночной недостаточности или нарушения баланса электролитов. Для лечения постаноксического интенционного и идиопатического миоклонуса используют 5-гидрокситриптофан — предшественник 5-ГТ (рис. 15.4); в качестве альтернативного лечения применяют баклофен, клоназепам и вальпроевую кислоту.
Астериксис. Астериксисом («порхающим» тремором) называют быстрые неритмичные движения, возникающие вследствие кратковременных прерываний фоновых тонических сокращений мышц. До некоторой степени астериксис можно считать отрицательным миоклонусом. Астериксис можно наблюдать в любой поперечнополосатой мышце во время ее сокращения, однако обычно клинически он бывает представлен в виде кратковременного падения постурального тонуса с восстановлением при произвольном разгибании конечности со сгибанием назад в запястье или голеностопном суставе. Астериксис характеризуется периодами молчания от 50 до 200 мс при непрерывном исследовании активности всех мышечных групп одной конечности с помощью ЭМГ (рис. 15.5). Это приводит к тому, что запястье или голень опускаются вниз перед тем, как возобновится мышечная активность и конечность вернется в исходное положение. Двусторонний астериксис часто наблюдают при метаболических энцефалопатиях, а в случае печеночной недостаточности он носит оригинальное название «печеночный хлопок». Астериксис может быть вызван применением некоторых лекарственных средств, включая все противосудорожные препараты и рентгенографическое контрастное вещество метризамид (Metrizamide). Односторонний астериксис может развиваться после поражений головного мозга в зоне кровоснабжения передней и задней мозговых артерий, а также вследствие мелкоочагового поражения головного мозга, охватывающего образования, которые разрушаются при стереотаксической криотомии вентролатерального ядра таламуса.
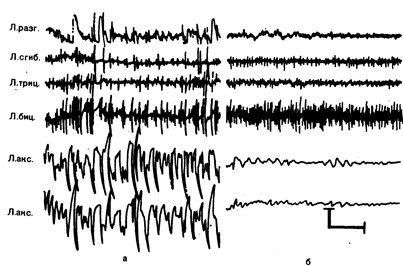
Рис. 15.4. Электромиограммы мышц левой руки у больного с постгипоксическим ннтенционным миоклонусом до (а) и во время (б) лечения 5-гидрокситриптофаном.
В обоих случаях рука находилась в горизонтальном положении. На первых четырех кривых представлен ЭМГ-сигнал с мышц-разгибателей кисти, сгибателя кисти, двуглавой и трехглавой. Нижние две кривые—регистрация с двух акселерометров, расположенных под прямым углом друг к другу на руке. Горизонтальная калибровка 1 с, а — продолжительные высокоамплитудные толчкообразные подергивания во время произвольных движений на ЭМГ представлены аритмическими разрядами биоэлектрической активности, перемежающимися с нерегулярными периодами молчания. Начальные положительные и последующие отрицательные изменения возникли синхронно в мышцах-антагонистах; б — наблюдается только слабовыраженный нерегулярный тремор, ЭМГ стала более равномерной (из J. Н. Crowdon et al., Neurology, 1976, 26, 1135).
Гемибаллизм. Гемибаллнзмом называют гиперкинез, характеризующийся насильственными бросковыми движениями в верхней конечности на стороне, противоположной очагу поражения (обычно сосудистого генеза) в области субталамического ядра. Могут возникать вращательный компонент при движениях плеча и бедра, сгибательные или разгибательные движения в кисти или стопе. Гиперкинезы сохраняются во время бодрствования, но обычно исчезают во время сна. Сила и тонус мышц могут быть несколько снижены на стороне поражения, точные движения затрудняются, однако признаков паралича нет. Экспериментальные данные и клинические наблюдения показывают, что субталамическое ядро, по-видимому, оказывает контролирующее влияние на бледный шар. При повреждении субталамического ядра это сдерживающее влияние устраняется, что приводит к гемибаллизму. Биохимические последствия этих нарушений остаются неясными, однако косвенные признаки позволяют предположить, что в других образованиях базальных ядер возникает усиление дофаминергического тонуса. Применение нейролептиков с целью блокады рецепторов дофамина, как правило, приводит к уменьшению проявлений геми-баллизма. При отсутствии эффекта от консервативного лечения возможно хирургическое лечение. Стереотаксиче-ское разрушение гомолатерального бледного шара, таламического пучка или вентролатерального ядра таламуса может привести к исчезновению гемибаллизма и нормализации двигательной активности. Хотя восстановление может быть полным, у некоторых больных отмечают гемихорею различной степени выраженности, охватывающую мышцы кисти и стопы.

Рис. 15.5. Астериксис, записанный с вытянутой левой руки у больного с энцефалопатией, вызванный приемом метризамида.
Верхние четыре кривые получены с тех же мышц, что и на рис. 15.4. Последняя кривая получена с акселерометра, расположенного на тыльной поверхности кисти. Калибровка 1 с. Запись сплошной кривой произвольной ЭМГ прервалась в области стрелки коротким непроизвольным периодом молчания во всех четырех мышцах. После периода молчания последовало изменение -позы с судорожным возвращением, что было зафиксировано акселерометром.
Тремор. Это достаточно распространенный симптом, характеризующийся ритмическими колебаниями определенной части тела относительно фиксированной точки. Как правило, тремор возникает в мышцах дистальных отделов конечностей, головы, языка или челюсти, в редких случаях — туловища. Существует несколько разновидностей тремора, и каждый имеет свои клинические и патофизиологические особенности, способы лечения. Часто у одного и того же больного можно наблюдать одновременно несколько разновидностей тремора, и каждый требует индивидуального лечения. В лечебном учреждении общего профиля у большинства больных с подозрением на тремор на самом деле имеют дело с астериксисом, возникшим на фоне какой-либо метаболической энцефалопатии. Различные виды тремора можно разделить на отдельные клинические варианты по их локализации, амплитуде и влиянию на целенаправленные движения.
Тремор в покое представляет собой крупноразмашистое дрожание со средней частотой 4—5 мышечных сокращений в секунду. Как правило, тремор возникает в одной или обеих верхних конечностях, иногда в челюсти и языке; является частым признаком болезни Паркинсона. Для этого вида тремора характерным является то, что он возникает при постуральном (тоническом) сокращении мышц туловища, тазового и плечевого пояса в покое; волевые движения временно ослабляют его (рис. 15.6). При полном расслаблении мышц проксимальных отделов тремор обычно исчезает, но так как больные редко достигают такого состояния, тремор держится постоянно. Иногда он изменяется с течением времени и может распространяться с одной группы мышц на другую при прогрессировании заболевания. У одних лиц с болезнью Паркинсона тремора не бывает, у других он очень слабый и ограничивается мышцами дистальных отделов, у некоторых больных паркинсонизмом и у лиц с болезнью Вильсона (гепатолентикулярная дегенерация) часто отмечают более выраженные расстройства, охватывающие и мышцы проксимальных отделов. Во многих случаях возникает ригидность пластического типа различной степени выраженности. Хотя этот вид тремора и приносит определенные неудобства, выполнению целенаправленных движений он препятствует незначительно: нередко больной с тремором может без особого труда поднести стакан воды ко рту и выпить его, не пролив при этом ни капли. Почерк становится мелким и неразборчивым (микрография), походка семенящая. Синдром Паркинсона характеризуется тремором в покое, замедленностью движений, ригидностью, сгибательными позами без истинного паралича и неустойчивостью. Часто болезнь Паркинсона сочетается с тремором, возникающим при сильном волнении, вызываемом значительным скоплением народа (одна из разновидностей усиленного физиологического тремора—см. ниже), или с наследственным эссенциальным тремором. Оба сопутствующих состояния усугубляются повышением уровня катехоламинов в крови и уменьшаются при приеме препаратов, блокирующих бета-адренорецепторы, например анаприлина.
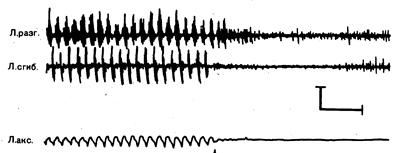
Рис. 15.6. Тремор в покое у больного с паркинсонизмом. Верхние две кривые ЭМГ сняты с разгибателей и сгибателей левой кисти, нижняя кривая сделана акселерометром, расположенным на левой руке. Горизонтальная калибровка 1 с. Тремор в покое возникает в результате чередующихся сокращений мышц-антагонистов с частотой примерно 5 Гц. Стрелкой указано изменение ЭМГ после того, как больной согнул кисть назад и тремор в покое исчез.
Точная патолого-морфологическая картина изменений при треморе покоя не известна. Болезнь Паркинсона вызывает видимые поражения преимущественно в черном веществе. Болезнь Вильсона, при которой тремор сочетается с мозжечковой атаксией, вызывает диффузные поражения. У людей пожилого возраста тремор в покое может не сопровождаться ригидностью, замедленностью движений, согбенной позой и неподвижностью мышц лица. В отличие от больных паркинсонизмом у лиц с подобными проявлениями подвижность сохранена, эффекта от приема противопаркинсонических препаратов нет. В каждом конкретном случае невозможно точно предсказать, является ли тремор начальным проявлением болезни Паркинсона. Больных с шаткостью при ходьбе и тремором в покое в проксимальных отделах конечностей (рубральный тремор) как симптом мозжечковых расстройств можно отличить от больных паркинсонизмом по наличию атаксии и дисметрии.
Интенционный тремор развивается при активном движении конечностей или при удерживании их в определенном положении, например в вытянутом. Амплитуда дрожания может несколько увеличиваться при выполнении более тонких движений, но никогда не достигает такого уровня, который наблюдают в случае мозжечковой атаксии/дисметрии. Интенционный тремор легко исчезает при расслаблении конечностей. В некоторых случаях Интенционный тремор представляет собой резко усугубившийся нормальный физиологический тремор, который может возникать в некоторых ситуациях у здоровых людей. Подобный тремор может возникать также у больных с эссенциальным тремором и болезнью Паркинсона. В этот процесс вовлекаются рука, находящаяся в вытянутом положении, голова, губы и язык. В целом это дрожание является следствием гиперадренергического состояния, а иногда имеет ятрогенное происхождение (табл. 15.2).
При активации b2-адренорецепторов в мышцах нарушаются их механические свойства, что приводит к возникновению интенционного тремора. Эти нарушения проявляются в повреждении афферентных образований мышечного веретена, что приводит к расстройству деятельности дуги рефлекса растяжения мышцы и способствует увеличению амплитуды физиологического тремора. Подобные виды тремора не возникают у больных с нарушением функциональной целостности дуги рефлекса растяжения мышцы. Препараты, блокирующие b2-адренорецепторы, уменьшают повышенный физиологический тремор. Интенционный тремор возникает при многих терапевтических, неврологических и психиатрических заболеваниях, поэтому интерпретировать его труднее, чем тремор в покое.
Таблица 15.2. Состояния, при которых усиливается физиологический тремор
Состояния, сопровождающиеся повышенной адренергической активностью:
— тревога
— прием бронхолитиков и других бета-миметиков
— возбужденное состояние
— гипогликемия
— гипертиреоз
— феохромоцитома
— периферические промежуточные продукты обмена леводопы.
— волнение перед выступлением на людях
Состояния, которые могут сопровождаться повышенной адренергической активностью:
— прием амфетаминов
— прием антидепрессантов
— абстинентный синдром (алкоголь, наркотики)
— ксантины в чае и кофе
Состояния неизвестной этиологии:
— лечение кортикостероидами
— физическая нагрузка
— повышенная усталость
— лечение препаратами лития
Существует также другой вид интенционного тремора, более медленный, как правило, в виде моносимптома, возникающий либо в виде спорадических случаев, либо у нескольких членов одной семьи. Он называется эссенциальным наследственным тремором (рис. 15.7) и может появиться в раннем детстве, однако чаще развивается в более позднем возрасте и наблюдается в течение всей жизни. Тремор приносит определенные неудобства, так как создается впечатление, что больной находится в возбужденном состоянии. Своеобразной особенностью данного тремора является то, что он исчезает после приема двух-трех глотков алкогольного напитка, однако после прекращения действия алкоголя становится более выраженным. Эссенциальный тремор уменьшается при приеме гексамидина и b-адреноблокаторов, влияющих на деятельность ЦНС, таких как анаприлин.
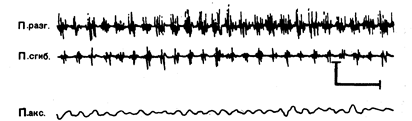
Рис. 15,7. Тремор действия у больного с эссенциальным тремором. Запись произведена с мышц правой руки во время сгибания кисти назад; в остальном записи сходны с таковыми на рис. 15.4. Калибровка 500 мс. Необходимо отметить, что во время тремора действия разряды биоэлектрической активности на ЭМГ с частотой примерно 8 Гц возникали синхронно в мышцах-антагонистах.
Термин интенционный тремор является несколько неточным: патологические движения, безусловно, не являются умышленными, намеренными и изменения правильнее было бы назвать дрожательной атаксией. При истинных треморах страдает, как правило, мускулатура дистальных отделов конечностей, дрожание бывает более ритмичным, как правило, в одной плоскости. Мозжечковая атаксия, которая вызывает ежеминутное изменение направления патологических движений, проявляется при точных целенаправленных движениях. Атаксия не проявляется в неподвижных конечностях и во время первого этапа произвольного движения, однако при продолжении движений и необходимости большей точности (например, при прикосновении к предмету, носу больного или пальцу врача) возникают толчкообразные, ритмичные подергивания, затрудняющие продвижение конечности вперед, с колебаниями в стороны. Они продолжаются до тех пор, пока действие, не будет завершено. Подобная дисметрия может создавать больному значительные помехи в выполнении дифференцированного действия. Иногда вовлекается голова (в случае пошатывающейся походки). Данное расстройство движений, без сомнения, указывает на поражение мозжечковой системы и ее связей. Если поражение значительное, каждое движение, даже поднятие конечности, приводит к таким изменениям, что больной теряет равновесие. Подобное состояние иногда отмечают при рассеянном склерозе, болезни Вильсона, а также сосудистых, травматических и других поражениях покрышки среднего мозга и субталамической области, но не мозжечка.
Привычные спазмы и тики. У многих людей в течение всей жизни существуют привычные гиперкинезы. Известными примерами могут служить шмыганье носом, откашливание, выпячивание подбородка, привычка теребить воротничок. Их называют привычными спазмами. Люди, совершающие подобные действия, признают, что движения являются целенаправленными, однако они вынуждены совершать их, чтобы преодолеть чувство напряжения. Привычные спазмы могут уменьшаться с течением времени или усилием воли больного, однако при отвлечении внимания возобновляются вновь. В некоторых случаях они настолько укореняются, что человек не замечает и не может контролировать их. Особенно часто привычные спазмы отмечают у детей от 5 до 10 лет.
Тики характеризуются стереотипными непреднамеренными нерегулярными движениями. Самой известной и самой тяжелой формой является синдром Жилля де ля Туретта — нейропсихиатрическое заболевание с расстройством движений и поведения. Как правило, первые симптомы этой болезни появляются в первые двадцать лет жизни, мужчины заболевают в 4 раза чаще, чем женщины. К двигательным расстройствам относят множественные кратковременные спазмы мышц, известные как судорожные тики в области лица, шеи и плеч. Часто возникают вокальные тики, больной издает хрюкающие и лающие звуки. Изменения поведения проявляются в виде копролалии (ругань и повторение других нецензурных выражений) и повторении слов и фраз, услышанных от окружающих (эхолалия). Происхождение синдрома Жилля де ля Туретта не установлено. Неясными также остаются патофизиологические механизмы. Лечение нейролептиками уменьшает выраженность и частоту тиков у 75—90% больных в зависимости от тяжести заболевания. Для лечения синдрома Жилля де ля Туретта применяют также клофелин, препарат из группы адреномиметиков.
Обследование и дифференциальная диагностика при экстрапирамидных синдромах. В широком смысле все экстрапирамидные расстройства необходимо рассматривать с точки зрения первичной недостаточности (отрицательные симптомы) и появившихся новых проявлений (изменение положения тела и гиперкинезы). Положительные симптомы возникают вследствие высвобождения от тормозного воздействия неподвижных образований нервной системы, ответственных за движения, и наступающего в результате этого нарушения их равновесия. Врач должен точно описывать наблюдаемые нарушения движений, не следует ограничиваться только названием симптома и подгонять его под готовую категорию. Если врач знает типичные проявления болезни, то он без труда выявит полную симптоматику экстрапирамидных заболеваний. Необходимо помнить, что для болезни Паркинсона характерны замедленность движений, слабовыраженная мимика, тремор в покое и ригидность. Так же легко идентифицировать типичные изменения позы при генерализованной форме дистонии или спастической кривошеи. В случае атетоза, как правило, наблюдают нестабильность поз, непрерывные движения пальцев и кистей рук, напряжение, при хорее с характерными быстрыми сложными гиперкинезами, при миоклонусе с порывистыми толчкообразными движениями, приводящими к изменению положения конечности или туловища. При экстрапирамидных синдромах чаще всего нарушаются целенаправленные движения.
Особые диагностические трудности представляют собой, как и в случае многих других заболеваний, ранние или стертые формы болезни. Часто до появления тремора остается незамеченной болезнь Паркинсона. Неуравновешенность и появление семенящей походки (ходьба мелкими шажками) у людей пожилого возраста часто ошибочно относят за счет потери уверенности и боязни падения. Больные могут жаловаться на нервозность и беспокойство и описывать затруднение движений и болезненность в различных частях тела. Если нет явлений паралича и рефлексы не изменены, эти жалобы могут быть расценены как ревматические или даже психогенные по характеру. Болезнь Паркинсона может начинаться с гемиплегических проявлений, и по этой причине может быть ошибочно диагностирован тромбоз сосудов или опухоль головного мозга. В этом случае диагностика может быть облегчена выявлением гипомимии, умеренной ригидности, недостаточной амплитуды размаха рук при ходьбе или нарушений других сочетанных действий. В каждом случае атипичных экстрапирамидных расстройств следует исключать болезнь Вильсона. Умеренную или раннюю хорею часто путают с повышенной возбудимостью. Решающее значение имеет осмотр больного в покое и во время активных движений. Однако в некоторых случаях невозможно отличить простое беспокойное состояние от ранних проявлений хореи, особенно у детей, не существует и лабораторных тестов для постановки точного диагноза. Отмечая первоначальные изменения поз при дистонии, врач может ошибочно предположить у больного истерию и только позже, когда изменения поз становятся устойчивыми, возможно правильно поставить диагноз.
Двигательные расстройства чаще возникают в комплексе с другими нарушениями. Экстрапирамидные синдромы, как правило, сопровождают поражения кортико-спинального тракта и мозжечковых систем. Например, при прогрессирующем надъядерном параличе, оливопонтоцеребеллярной дегенерации и синдроме Шая — Дрейджера наблюдают многие признаки болезни Паркинсона, а также отмечают нарушение произвольных движений глазных яблок, атаксию, апраксию, постуральную гипотензию или спастичность с двусторонним симптомом Бабинского. Для болезни Вильсона характерны тремор в покое, ригидность, замедленность движений и сгибательная дистония в мышцах туловища, тогда как атетоз, дистония и интенционный тремор возникают редко. Могут также отмечаться умственные и эмоциональные расстройства. Болезнь Геллервордена—Шпатца может вызывать общую ригидность и сгибательную дистонию, в редких случаях возможен хореоатетоз. При некоторых формах болезни Гентингтона, особенно если заболевание началось, в юношеском возрасте, ригидность сменяется хореоатетозом. При спастическом двустороннем параличе у детей может развиваться сочетание пирамидных и экстрапирамидных расстройств. Некоторые из дегенеративных заболеваний, вызывающих поражение одновременно и кортико-спинального тракта, и ядер, описываются в гл. 350.
Морфологические исследования базальных ядер, а также данные исследований содержания нейротрансмиттеров позволяют оценивать поражения базальных ядер и контролировать лечение таких заболеваний. Лучше всего это иллюстрируют болезни Гентингтона и Паркинсона. При болезни Паркинсона содержание дефамина в полосатом теле снижено вследствие гибели нейронов черного вещества и дегенерации их аксональных проекций к полосатому телу. В результате снижения содержания дофамина нейроны полосатого тела, синтезирующие ацетилхолин, освобождаются от тормозного влияния. Это приводит к преобладанию холинергической нервной передачи по сравнению с дофаминергической, что объясняет большинство симптомов болезни Паркинсона. Выявление такого дисбаланса служит основанием для рационального медикаментозного лечения. Препараты, усиливающие дофаминергическую передачу, такие как леводопа и бромокриптин, вероятно, должны восстанавливать равновесие между холинергическими и дофаминергическими системами. Эти лекарственные средства, назначаемые в комбинации с антихолинергическими препаратами, в настоящее время являются основными в лечении болезни Паркинсона. Применение избы точных доз леводопы и бромокриптина приводит к возникновению различных гиперкинезов вследствие перераздражения рецепторов дофамина в полосатом теле. Наиболее частым из них является краниофациальный хореоатетоз, могут также развиваться генерализованный хореоатетоз, тики в области лица и шеи, дистонические изменения поз, миоклонические подергивания. С другой стороны, назначение препаратов, блокирующих рецепторы дофамина (например, нейролентики) или вызывающих истощение накопленного дофамина [тетрабенацин (Tetrabenazine) или резерпин], может привести к возникновению синдрома паркинсонизма у практически здоровых людей,
Хорея Гентингтона во многих отношениях является клинической и фармакологической противоположностью болезни Паркинсона. При болезни Гентингтона, характеризующейся изменениями личности и деменцией, нарушением ходьбы и хореей, происходит гибель нейронов хвостатого ядра и скорлупы, что приводит к истощению ГАМК и ацетилхолина при неизмененном содержании дофамина. Считают, что хорея возникает вследствие относительного избытка дофамина по сравнению с другими нейротрансмиттерами в полосатом теле; препараты, блокирующие рецепторы дофамина, например нейролептики, в большинстве случаев оказывают положительный эффект при хорее, тогда как леводопа усиливает ее. Таким же образом физостигмин, усиливающий холинергическую передачу, может уменьшать признаки хореи, тогда как антихолинергические препараты усиливают их.
Эти примеры из клинической фармакологии также свидетельствуют о тонком равновесии между стимулирующими и тормозными процессами в базальных ядрах. У всех больных различные клинические проявления, отмечаемые во время лечения, бывают обусловлены изменениями в нейрохимической среде, .морфологические повреждения остаются неизменными. Эти примеры иллюстрируют возможности медикаментозного лечения поражений базальных ядер и дают основание с оптимизмом смотреть на перспективы лечения больных с экстрапирамидными двигательными расстройствами.
Список литературы
Delong M. R., Georgopoulos A. P. Motor functions of the basal ganglia. — In:
Handbook of Physiology/Ed. V. B. Brooks, sect. I.: The Nervous System, vol. II: Motor Control, part 2. Bethesda: Amer. Physiol. Society, 1981, 1017— 1062.
Delwaide P. 3 ., Young R. R. (Eds.) Restorative Neurology, vol. I. Clinical Neurophysiology in Spasticity. — Amsterdam: Elsevier, 1985.
Emson P. C. (Ed.) Chemical Neuroanatomy. — New York: Raven Press, 1983.
Feldman R. G. et al. (Ed.) Spasticity: Disordered Motor Control — Chicago: Year Book Medical Publishers, 1980.
Geschwind N. The apraxias: Neural mechanisms of disorders of learned movements. — Amer. Sci., 1975, 63, 188.
Growdon J. H., Scheife R. T. Medical Treatment of extrapyramidal diseases. — In: Update III: Harrison s Principles of Internal Medicine/Eds. K. J. Issel-bacher et al..New York: McGraw-Hill, 1982, 185—208.
Kuypers H. G. J. M. Anatomy of the descending pathways. — In: Handbook of Physiology, Sect. I, The Nervous System, vol. II, Motor Control, part I/Ed. V. B. Brooks. Bethesda: Amer. Physiol. Society, 1981, 597—666.
Lawrence D. G., Kuypers H. G. J. M. The "functional organisation of the motor system in the monkey. — Brain, 1968, 91, 1.
Marsden С. D. The mysterious motor function of the basal ganglia. — Neurology, 1982, 32, 514.
Martin J. B. Huntington s disease: New approaches to an old problem. — Neurology, 1984, 34, 1059.
Young R. R., Shahani B. T. Asterixis: One type of negative myoclonus. — In:
Myoclonus/Eds. S. Fahn et al. New York: Raven Press, 1985, 12—30.
Young R. R., Delwaide P. J. Drug therapy: Spasticity. — New Engl. J. Med., 1981, 304, 28.
Дата добавления: 2015-07-22; просмотров: 1464;
