Основные типы кристаллических решеток
Основные характеристики кристаллических структур. Для количественной оценки степени упакованности кристаллической решетки удобно пользоваться специальными показателями. Рассмотрим наиболее важные из них.
Число атомов на ячейку nя - это число атомов, целиком принадлежащих данной элементарной ячейке. Например, в примитивной кубической решетке число атомов на ячейку равно 1 (атомы размещены только в вершинах куба и каждый из них принадлежит ячейке на 1/8). В сложной объемно-центрированной решетке их 2 (помимо восьми вершинных есть один атом в центре куба, целиком принадлежащий ячейке); наконец, в гранецентрированной уже 4 (кроме вершинных, имеется шесть атомов в центре каждой грани куба, принадлежащих ячейке лишь наполовину).
Координационное число К представляет собой количество ближайших равноудаленных атомов, окружающих данный атом. Как отмечалось, в гранецентрированной кубической и гексагональной компактной решетках К=12, в то же время для объемно-центрированной кубической К=8.
Коэффициент компактности (заполнения) q характеризует отношение объема Vа , занятого в ячейке атомами, к объему всей ячейки Vя , т.е. q = V а / V я . Коэффициент заполнения для простой кубической решетки составляет 0,52, для объемно-центрированной кубической - 0,68 и для плотнейшей упаковки (гранецентрированной
Подавляющее большинство металлов (около 75%) имеет кристаллические структуры трех видов - это решетки типа вольфрама, меди и магния. Познакомимся с ними.
Структурный тип вольфрама (рис.1). Решетка Браве является объемно-центрированной кубической (ОЦК). Слоев с плотнейшей упаковкой эта решетка не имеет. В отличие от других плоскостей более упакованными являются плоскости типа {110}, в которых содержится по два плотноупакованных направления <111> (рис.1,а). Микропоры имеют форму октаэдра и тетраэдра (рис.1,б,в), причем размер октапор оказывается меньше тетраэдрических ( rок.п / rат = 0,15 и rт.п / rат = 0,29 соответственно, при этом rок.п , rт.п и rат - размеры октаэдрической, тетраэдрической пор и атома).
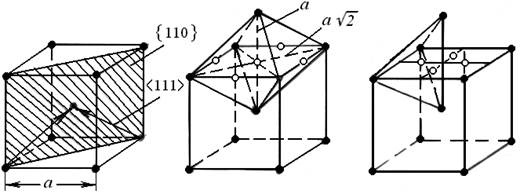
А б в
Рис. 1. Кубическая объемно-центрированная решетка:
а - элементарная ячейка и плотноупакованные
плоскости и направления;
б - октаэдрические поры (о);
в - тетраэдрические поры (о); (·) - атомы металла
С наличием этих пор связана одна примечательная особенность - примесные атомы внедрения, размещающиеся в междоузлиях ОЦК-решетки, предпочтительно располагаются в меньших по объему октаэдрических порах, нежели в относительно более крупных тетраэдрических. Это объясняется тем, что октаэдрическая пора, окруженная шестью атомами, имеет форму слегка сплюснутого октаэдра - два атома расположены ближе друг к другу (на расстоянии, равном периоду решетки a), чем остальные четыре (на удалении уже a 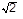 ) . В противоположность этому тетраэдрическая пора является симметричной, поэтому внедрение чужеродного атома в такую позицию вызовет одинаковое смещение всех четырех окружающих атомов. В то же время при попадании внедренного атома в октаэдрическую пору только два атома окажутся смещенными, соответственно в решетке произойдет деформация вдоль направления, соединяющего ближайшие атомы в октаэдре. Таким образом, размещение примесных атомов внедрения в октапорах вызовет меньшее искажение решетки по сравнению с нахождением их в тетраэдрических позициях. Вместе с тем известны случаи, когда примесные атомы внедрения могут размещаться и в тетраэдрических порах (например, атомы водорода).
) . В противоположность этому тетраэдрическая пора является симметричной, поэтому внедрение чужеродного атома в такую позицию вызовет одинаковое смещение всех четырех окружающих атомов. В то же время при попадании внедренного атома в октаэдрическую пору только два атома окажутся смещенными, соответственно в решетке произойдет деформация вдоль направления, соединяющего ближайшие атомы в октаэдре. Таким образом, размещение примесных атомов внедрения в октапорах вызовет меньшее искажение решетки по сравнению с нахождением их в тетраэдрических позициях. Вместе с тем известны случаи, когда примесные атомы внедрения могут размещаться и в тетраэдрических порах (например, атомы водорода).
Структурой ОЦК обладают щелочные металлы Li, Na, K, Rb, Cs, переходные металлы V, Cr, Nb, Mo, Ta и W, а также полиморфные модификации таких металлов, как Fe, Ti и Zr.
Структурный тип меди (рис.2). Решетка Браве - гранецентрированная кубическая (ГЦК), имеет плотнейшие атомные слои типа {111}, чередующиеся в последовательности АВСАВС ... В каждом таком слое содержится три плотноупакованных атомных ряда <110> (рис.2,а). Имеются относительно большие по размеру и симметричные по форме октаэдрические поры (rок.п / rат = 0,41), заметно превышающие тетраэдрические (rт.п / rат = 0,22). Их изображение дано на рис.40,б,в.
Такая структура характерна для благородных металлов, которым относятся Cu, Ag, Au, а также металлы платиновой группы Pt, Pd, Rh, Ir, для многовалентных металлов Al и Pb, переходных металлов последних групп периодической системы Ni, а также соответствующих модификаций Fe, Co.
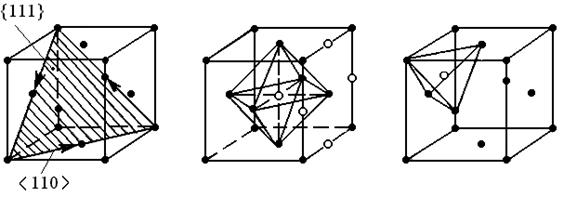
А б в
Рис. 2. Кубическая гранецентрированная решетка:
а - элементарная ячейка и плотноупакованные плоскости
и направления;
б - октаэдрические поры (о);
в - тетраэдрические поры (о); (·) - атомы металла
Структурный тип магния (рис.3). Решетка Браве - гексагональная примитивная. Плотная упаковка обеспечивается совмещением двух решеток Браве, в результате элементарная ячейка представляет собой четырехгранную призму, в которой помимо вершинных атомов содержится еще один, расположенный внутри. Плотнейшие слои типа {0001} размещаются в последовательности АВАВ ..., т.е. упаковка оказывается двухслойной. В каждой такой плоскости имеется три плотноупакованных направления типа <1120>. Плотное прилегание этих слоев получается, когда между периодами решетки а и с выдерживается определенное соотношение - с/а =1,633. У большинства металлов с такой структурой отношение с/а оказывается либо меньше (Be, Zr, Ti), либо больше (Zn, Cd) этой величины. Ближе к идеальной плотноупакованной гексагональной структуре подходят решетки Mg и Co.
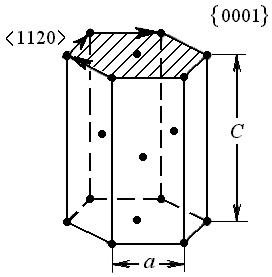
Рис. 3. Элементарная ячейка и плотноупакованные плоскости
и направления гексагональной плотноупакованной решетки
Подобная структура, которую принято называть гексагональной плот- ноупакованной (ГПУ), присуща переходным металлам первых групп Sс, Ti, Zr, Hf, двухвалентным металлам Be, Mg, Zn и Cd и большинству редкоземельных металлов.
Дата добавления: 2015-06-27; просмотров: 5387;
