Окисление углерода
В современных сталеплавильных процессах главной частью металлической шихты является твердый или жидкий чугун, содержание углерода в котором всегда значительно выше, чем должно быть в готовой стали. В связи с этим сталеплавильные процессы сопровождаются процессом удаления избыточного углерода из металла. Удаление 1 % С из металла связано с образованием газовой фазы, объем которой значительно больше объема жидкой ванны. Выделение из ванны пузырей газа, представляющего продукт окисления углерода, сопровождается интенсивным перемешиванием ее, ускорением процессов тепло- и массообмена, дегазации металла и удаления из него неметаллических включений.
Растворенный углерод в железе условно обозначают [С]. Продуктом реакции окисления углерода в расплаве является преимущественно монооксид углерода СО, хотя при низких концентрациях углерода в металле возможно образование незначительных количеств диоксида углерода СО2. Схематически можно представить реакцию окисления углерода в виде
[С] + [О] = {СО}
(фигурные скобки означают, что продукт реакции входит в самостоятельную газовую фазу). Константу равновесия реакции можно определить из следующего выражения
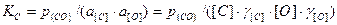 .
.
Для низких концентраций исходных компонентов приближенно считают значения 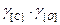 , равными единице. Тогда при
, равными единице. Тогда при 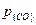 = 1 имеем КC = 1/[С].[О], а так как 1/КC = const, то произведение [С].[О] при данной температуре постоянно, его обозначают символом m, т.е. [С].[О] = m. Следовательно, от концентрации углерода зависит концентрация кислорода в металле. Чем выше содержание углерода в металле, тем ниже содержание кислорода в нем и наоборот. Однако в реальных условиях реакция равновесие не достигает и фактическое содержание кислорода в металле выше, чем равновесное.
= 1 имеем КC = 1/[С].[О], а так как 1/КC = const, то произведение [С].[О] при данной температуре постоянно, его обозначают символом m, т.е. [С].[О] = m. Следовательно, от концентрации углерода зависит концентрация кислорода в металле. Чем выше содержание углерода в металле, тем ниже содержание кислорода в нем и наоборот. Однако в реальных условиях реакция равновесие не достигает и фактическое содержание кислорода в металле выше, чем равновесное.
Выделение оксида углерода возможно, если присутствуют условия, облегчающие зарождение пузырей СО. Такими условиями могут быть продувка металла кислородом или воздухом и наличие шероховатости на поверхности огнеупорной футеровки, контактирующей с жидким металлом. В этих случаях имеются готовые газообразные полости в металле с развитой поверхностью раздела газ-металл, в которые беспрепятственно выделяется монооксид углерода СО, как продукт взаимодействия углерода и кислорода вблизи этой поверхности. Выделяющийся пузырь должен преодолеть давление, представляющее собой сумму давлений - атмосферы, столба шлака, столба металла и силы поверхностного натяжения σ расплава, т.е. 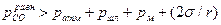 , где r - радиус пузыря монооксида углерода.
, где r - радиус пузыря монооксида углерода.
Повышение температуры способствует не только повышению скорости окисления углерода, но и повышает химическое сродство углерода к кислороду.
Снижение внешнего давления (создание разрежения над металлом) в соответствии с принципом Ле-Шателье приводит к смещению равновесия реакции [С] + [О] = {СО} в сторону образования продукта реакции. В равновесных условиях при этом окажется более низкая концентрация кислорода в металле, а углерод становится хорошим раскислителем.
Дата добавления: 2015-06-22; просмотров: 1395;
