Влияние температуры
Температура химической реакции влияет на скорость, и это влияние зависит от типа химической реакции. Рассмотрим такую зависимость для следующих реакций.
4.1.1 Простая необратимая экзо- или эндотермическая реакция
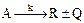 ;
;
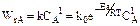 ; (4.4)
; (4.4)
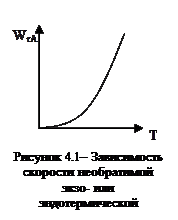
с ростом температуры для этих реакций растет скорость реакции (рисунок 4.1).
4.1.2 Простая обратимая экзотермическая реакция А 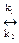 R+Q;
R+Q;
скорость химической реакции WrA=k1CA-k2CR.
Ранее получено CA=CA,0(1-XA); CR=CA,0XA; Kc=k1/k2.
После подстановки
WrA=k1CA,0(1-XA)-(k1/Кc)CА,0XA; (4.5)
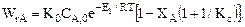 . (4.6)
. (4.6)
Проанализируем уравнение при условии, что ХА=const.
С ростом температуры: множитель 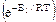 увеличивается; коэффициент Кс понижается, значение 1/Кс растет и величина
увеличивается; коэффициент Кс понижается, значение 1/Кс растет и величина
[1-ХА(1+1/Кс)] понижается, следовательно, зависимость скорости химической реакции от температуры проходит через максимум (рисунок 4.2).
|
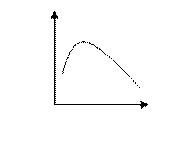
Рисунок 4.2 – Зависимость скорости обратимой
экзотермической реакции от температуры
Построим несколько кривых для различных значений степени превращения (рисунок 4.3).
|
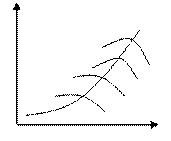
Рисунок 4.3 – Зависимость скорости обратимой экзотермической
реакции от температуры при различных степенях превращения
Чем больше степень превращения (Х1<X2<X3<X4), тем меньше скорость химической реакции.
Cоединим максимумы скоростей кривой АВ, которая носит название линии оптимальных температур (ЛОТ).
4.1.3 Простая обратимая эндотермическая реакция A 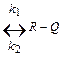 .
.
Аналогично обратимой экзотермической реакции получаем, что
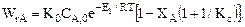 (4.7)
(4.7)
 Проанализируем уравнение при условии, что ХА= const. С ростом температуры множитель
Проанализируем уравнение при условии, что ХА= const. С ростом температуры множитель 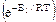 увеличивается, коэффициент Kc увеличивается, значение 1/Кс – уменьшается, величина [1-XA(1+1/Kc)] увеличивается.
увеличивается, коэффициент Kc увеличивается, значение 1/Кс – уменьшается, величина [1-XA(1+1/Kc)] увеличивается.
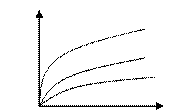
|
превращения (Х1 < X2 < X3) уменьшается скорость химической реакции (рисунок 4.4).
 Рассмотрим для этих же реакций изменение степени превращения (рисунки 4.5, 4.6, 4.7).
Рассмотрим для этих же реакций изменение степени превращения (рисунки 4.5, 4.6, 4.7).
A 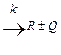 .
.
 При небольших температурах мала степень превращения (ХА), мала и скорость химической реакции. С возрастанием температуры резко увеличивается ХА и велика скорость химической реакции. В конце химической реакции скорость мала, а ХА асимптотически приближается к единице.
При небольших температурах мала степень превращения (ХА), мала и скорость химической реакции. С возрастанием температуры резко увеличивается ХА и велика скорость химической реакции. В конце химической реакции скорость мала, а ХА асимптотически приближается к единице.
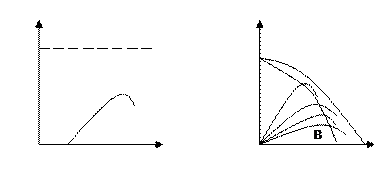
А 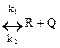 .
.
|
Для этих реакций при некотором времени τ величина Хфактич. проходит через максимум. Значение Хфактич. ограничено равновесной кривой, и в дальнейшем при увеличении температуры оно уменьшается, т.к. возрастает влияние термодинамических факторов. Если построить несколько зависимостей Хфактич. и их максимумы соединить кривой АВ, то получим линию оптимальных температур для реакций.
Для простых обратимых экзотермических реакций существует не какая-то оптимальная температура, а температурная последовательность, обеспечивающая максимальную скорость процесса. Чтобы создать такие оптимальные условия, процесс следует вначале вести при высокой температуре, когда скорость химической реакции велика, и из-за низкого значения степени превращения ХА не может быть достигнута высокая равновесная степень превращения ХА,е. Для увеличения степени превращения ХА необходимо снизить температуру и вести процесс по ЛОТ.
А 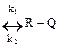 .
.
|
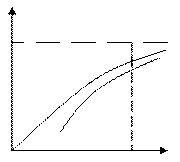
Рисунок 4.7 – Зависимость степени превращения от температуры
для простых обратимых эндотермических реакций
Для этих реакций приходится вводить понятие Топт., т.к. при дальнейшем росте температуры практически не меняется степень превращения.
Отрицательное влияние температуры выражается:
- в увеличении потерь целого продукта вследствие его испарения и образования побочных продуктов;
- в снижении прочности и химической стойкости материалов;
- в снижении степени превращения ХА в обратимых экзотермических реакциях;
- в возможном снижении селективности при проведении сложных реакций.
Дата добавления: 2015-06-17; просмотров: 3207;
