Получение металлов термическим разложением галогенидов и других соединений
Анализируя данные табл. 5 (см. выше), можно заметить, что прочность галогенидов металлов уменьшается от фторидов к иодидам, причем 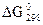 образования некоторых иодидов не превышает десятков единиц кДж/моль. Это позволяет предположить, что при благоприятных условиях возможна диссоциация иодида металла на исходный металл и йод. Аналогично могут вести себя и другие соединения металлов с небольшими отрицательными значениями
образования некоторых иодидов не превышает десятков единиц кДж/моль. Это позволяет предположить, что при благоприятных условиях возможна диссоциация иодида металла на исходный металл и йод. Аналогично могут вести себя и другие соединения металлов с небольшими отрицательными значениями 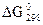 . Как отмечалось ранее, при диссоциации наблюдается сильное возрастание энтропии (∆S>0), в то время как энтальпия изменяется незначительно (∆H близко к нулю). Поэтому с ростом температуры ∆G уменьшается и при некотором значении температуры становится меньше нуля. Кроме того, имеет значение и летучесть иодидов. В ряде работ было показано, что иодид циркония ZrI4, переведенный в парообразное состояние (температура сублимации 431°C при давлении 101,33∙103 Па), термически разлагается на наколенной проволоке при температуре 1800°C:
. Как отмечалось ранее, при диссоциации наблюдается сильное возрастание энтропии (∆S>0), в то время как энтальпия изменяется незначительно (∆H близко к нулю). Поэтому с ростом температуры ∆G уменьшается и при некотором значении температуры становится меньше нуля. Кроме того, имеет значение и летучесть иодидов. В ряде работ было показано, что иодид циркония ZrI4, переведенный в парообразное состояние (температура сублимации 431°C при давлении 101,33∙103 Па), термически разлагается на наколенной проволоке при температуре 1800°C:
ZrI4  Zr + 2I2.
Zr + 2I2.
Элементарный цирконий осаждается на раскаленной проволоке, а йод остается в реакционном сосуде. Осаждение циркония на вольфрамовой нити начинается при 1300°С, а при 1800°С в случае точного соблюдения рекомендованных технических условий (толщина нити, сила тока и т. д.) образуются стержни очень чистого ковкого циркония, причем часто наблюдается Образование монокристаллов. Подобным методом можно получить ряд металлов, обладающих очень высокой температурой плавления. Например, удалось выделить кроме циркония титан, кремний, гафний и торий из иодидов, вольфрам, молибден и титан из паров хлоридов. Термическое разложение можно проводить иногда также в электрической дуге или в тлеющем разряде. Этим методом, например, из смеси SiHCl3 и SiCl c водородом был получен чистейший кремнии в виде монокристалла.
Достаточно легко разлагаются и карбонилы металлов. Так, Fe(СО)5 (температура кипения 105°С) разлагается при нагревании в соответствии с уравнением:
Fe (СO)5  Fe + 5СО.
Fe + 5СО.
Полученное таким образам карбонильное железо при соответствующей чистоте исходного вещества практически свободно от всех посторонних элементов, кроме небольших примесей C и O, образующихся в результате побочных реакций. Распад карбонила начинается на поверхности железа уже при 60°С, а индифферентной стенке металл начинает выделяться при 40°С; в свободном газовом пространстве пентакарбонил железа распадается только при температурах выше 180°С. На гладкой стенке металл осаждается в компактной форме в виде зеркала, в то время как при разложении в газовом пространстве образуется металл в дисперсном состоянии. Тонкий порошок железа образуется также при термическом разложении его оксалата по реакции:
Fe (COO)2  Fe + 2СО2.
Fe + 2СО2.
Аналогичная картина наблюдается для карбонила никеля Ni(CO)4, разложением которого при температуре 180–200°С получают никель высокой степени частоты.
Серебро и ртуть могут быть получены разложением соответствующих цианидов AgCN и Hg(CN)2 при температуре порядка 400°С:
2AgCN  2Ag + (CN)2.
2Ag + (CN)2.
Для получения ряда металлов путем термического разложения их соединений часто применяют глубокий вакуум, ибо при реакциях в большинстве случаев имеет место непрерывное, хотя и небольшое по количеству, выделение газа. В частности, осторожным разложением NaN3 при температуре 275° в высоком вакууме можно получить небольшие количества, очень чистого Na. Получение бария осторожным термическим разложением Ba(N3)2 сопровождается образованием нитрида, поэтому лучше применять восстановление оксида бария алюминием при температуре около 1050°С и затем отгонять барий в вакууме при 1100-1200°С.
Дата добавления: 2015-06-17; просмотров: 2330;
