Аминофенолы: дофамин, норадреналин, адреналин. Понятие о биологической роли этих соединений и их производных.
К аминофенолам относятся соединения, в которых функциональные группы NH2 и OH присоединены к бензольному кольцу.
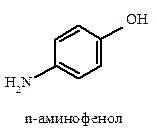
Два производных n-аминофенола применяются в медицине как обезболивающие и жаропонижающие средства. Это – парацетамол и, в меньшей степени, фенацетин
Катехоламины – дофамин, норадреналин, адреналин – биогенные амины, продукты метаболизма аминокислоты фенилаланина.
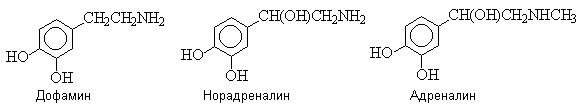
Катехоламины выполняют роль гормонов и нейромедиаторов. Адреналин является гормоном мозгового слоя надпочечников, норадреналин и дофамин – его предшественниками. Увеличение концентрации катехоламинов – типичная реакция на стресс. Их роль заключается в мобилизации организма на осуществление активной мозговой и мышечной деятельности.
Дофамин – гормон, нейромедиатор, улучшает доставку кислорода, усиливает силу сердечных сокращений, работу почек, влияет на двигательную активность.
Дофамин-гормон вырабатывается мозговым веществом надпочечников, а дофамин-нейромедиатор - областью среднего мозга, называемой «черным телом».
Дофамин-нейромедиатор. Известны четыре «дофаминовых пути» - проводящих пути мозга, в которых роль переносчика нервного импульса играет дофамин. Один из них - мезолимбический путь - считается ответственным за продуцирование чувств удовольствия. Считается, что дофамин также участвует в процессе принятия человеком решений. По крайней мере, среди людей с нарушением синтеза/транспорта дофамина многие испытывают затруднения с принятием решений. Это связано с тем, что дофамин отвечает за «чувство награды», которое зачастую позволяет принять решение, обдумывая то или иное действие ещё на подсознательном уровне.
Адреналин или метиламиноэтанолпирокатехин, образуется в надпочечниках и является гормоном, реализующим реакции типа «бей или беги». Его секреция резко повышается при стрессовых состояниях, пограничных ситуациях, ощущении опасности, при тревоге, страхе, при травмах, ожогах и шоковых состояниях.
Адреналин:
• усиливает и учащает сердцебиение
• вызывает сужение сосудов мускулатуры, брюшной полости, слизистых оболочек
• расслабляет мускулатуру кишечника, и расширяет зрачки..
Основная задача адреналина - адаптировать организм к стрессовой ситуации. Адреналин улучшает функциональную способность скелетных мышц. При продолжительном воздействии адреналина отмечается увеличение размеров миокарда и скелетных мышц. Вместе с тем длительное воздействие высоких концентраций адреналина приводит к усиленному белковому обмену, уменьшению мышечной массы и силы, похуданию и истощению. Это объясняет исхудание и истощение при дистрессе (стрессе, превышающем адаптационные возможности организма).
Адреналин повышает кровяное давление, в связи с чем стрессы могут способствовать стойкому повышению давления и заболеванию сердечно-сосудистой системы.
Адреналин часто применяют в качестве кровоостанавливающего средства. Получают его из надпочечников, а также синтетически из пирокатехина. Интересно, что лишь левовращающий (природный) адреналин обладает биологической активностью, тогда как правовращающий биологически неактивен.
Норадреналин - гормон и нейромедиатор. Норадреналин также повышается при стрессе, шоке, травмах, тревоге, страхе, нервном напряжении. В отличие от адреналина, основное действие норадреналина заключается исключительно в сужении сосудов и повышении артериального давления. Сосудосуживающий эффект норадреналина выше, хотя продолжительность его действия короче.
И адреналин, и норадреналин способны вызывать тремор - то есть дрожание конечностей, подбородка. Особенно ясно эта реакция проявляется у детей возраста 2-5 лет, при наступлении стрессовой ситуации.
Непосредственно после определения ситуации как стрессовой, гипоталамус выделяет в кровь кортикотропин (адренокортикотропный гормон), который, достигнув надпочечников, побуждает синтез норадреналина и адреналина.
«Бодрящий» эффект никотина обеспечивается выбросом в кровь адреналина и норадреналина. В среднем достаточно около 7 секунд после вдыхания табачного дыма, чтобы никотин достиг мозга. При этом происходит кратковременное ускорение сердцебиения, увеличение АД, учащение дыхания и улучшение кровоснабжения головного мозга. Сопровождающий это выброс дофамина способствует закреплению никотиновой зависимости.
Монокарбоновые кислоты: химические свойства с участием карбоксильной группы: (образование солей, сложных эфиров, амидов, ангидридов). Функциональные производные карбоновых кислот тиоэфиры – (АцетилКоА, АцилКоА).
Карбоновые кислоты, содержащие в своем составе одну карбоксильную группу, называют одноосновными, две - двухосновными и т. д. При взаимодействии карбоновых кислот со щелочами, карбонатами и гидрокарбонатами образуются соли:
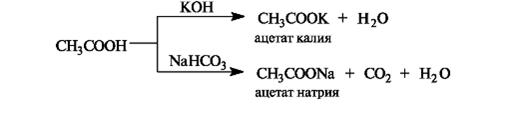
Наиболее важные реакции монокарбоновых кислот приведены на схеме 1.
Схема 1. Некоторые реакции нуклеофильного замещения в карбоновых кислотах
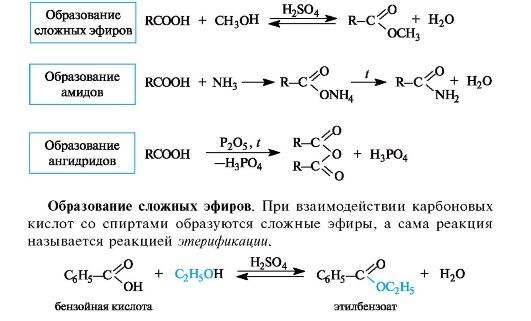
Реакция этерификации катализируется сильными кислотами.
Тиоэфиры- серные аналоги сложных эфиров - находят весьма ограниченное применение в классической органической химии, но играют важную роль в организме. Известно, что для проявления каталитической активности большинству ферментов, имеющих белковую природу, необходимо соучастие коферментов, которыми служат разнообразные по строению низкомолекулярные органические соединения небелковой природы. Одну из групп коферментов составляют ацилкоферменты, выполняющие функцию переносчиков ацильных групп. Из них наиболее распространен ацетилкофермент А. При всей сложности строения молекулы ацетилкофермента А с позиций химического подхода можно определить, что этот кофермент функционирует как тиоэфир. В качестве тиола, участвующего в его образовании, выступает кофермент А (сокращенно обозначаемый CoASH), молекула которого построена из остатков трех компонентов - 2-аминоэтантиола, пантотеновой кислоты и аденозиндифосфата (дополнительно фосфорилированного по положению 3 в рибозном фрагменте). Аденозиндифосфат (АДФ) рассмотрен в дальнейшем как представитель другой важной группы коферментов - нуклеозидполифосфатов. Пантотеновая кислота образует, с одной стороны, амидную связь с 2-аминоэтантиолом, а с другой - сложноэфирную связь с остатком АДФ.
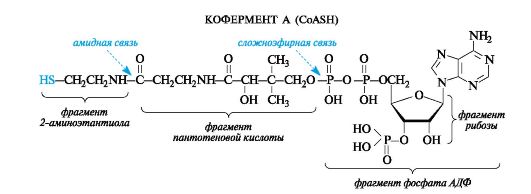
По ацилирующей способности все ацилкоферменты А и в том числе ацетилкофермент А, будучи тиоэфирами, занимают «золотую середину» между высокореакционными ангидридами и малоактивными карбоновыми кислотами и сложными эфирами. Их достаточно высокая активность обусловлена, в частности, повышенной стабильностью уходящей группы - аниона CoA-S- - по сравнению с гидроксид- и алкоксид-ионами кислот и сложных эфиров соответственно.
Ацетилкофермент А in vivo является переносчиком ацетильных групп на нуклеофильные субстраты.
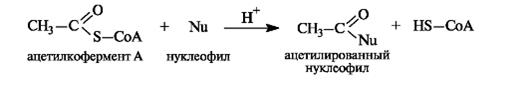
Этим путем, например, осуществляется ацетилирование гидроксилсодержащих соединений.
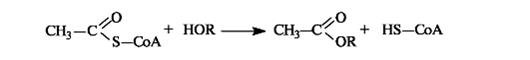
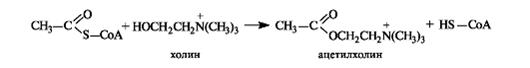
С использованием ацетилкофермента А протекает превращение холина в ацетилхолин, являющегося посредником при передаче нервного возбуждения в нервных тканях (нейромедиатором).
Кроме этого, можно отметить важное участие в процессах обмена веществ самого кофермента А, функционирующего в качестве тиола. В организме любые карбоновые кислоты активируются путем превращения в реакционноспособные производные - тиоэфиры.
АцилКоА образуется при активации жирных кислот. Свободная жирная кислота независимо от длины углеводородной цепи является метаболически инертной и не может подвергаться никаким биохимическим превращениям, в том числе окислению, пока не будет активирована. Активация жирной кислоты протекает на наружной поверхности мембраны митохондрий при участии АТФ, коэнзима A (HS-KoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой:
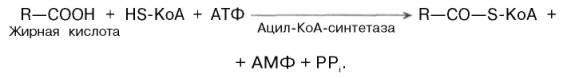
В результате реакции образуется ацил-КоА, являющийся активной формой жирной кислоты.
Насыщенные дикарбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая. Соли щавелевой кислоты - оксалаты. Превращение янтарной кислоты в фумаровую как пример биологической реакции дегидрирования.
В настоящем разделе будут рассмотрены некоторые представители дикарбоновых кислот алифатического и ароматического рядов (табл. 1). Все они представляют собой кристаллические вещества.
Таблица 1. Названия некоторых дикарбоновых кислот и их производных
| Название кислоты | Формула | Название аниона или основы сложного эфира |
| Щавелевая (этандиовая) | НООС-СООН | Оксалат |
| Малоновая (пропандиовая) | НООС-СН2-СООН | Малонат |
| Янтарная (бутандиовая) | НООС-(СН2)2-СООН | Сукцинат |
| Глутаровая (пентандиовая) | НООС-(СН2)3-СООН | Глутарат |
Систематические названия дикарбоновых кислот строятся по общим правилам заместительной номенклатуры. Однако для большинства из них предпочтительны тривиальные названия. Их латинские названия служат основой названия анионов и производных кислот, которые часто не совпадают с русскими тривиальными названиями (см. табл. 1).
Щавелевая кислота - простейшая двухосновная кислота. Некоторые ее соли, например оксалат кальция, трудно растворимы и часто образуют камни в почках и мочевом пузыре (оксалатные камни).
Янтарная кислота в заметном количестве была обнаружена в янтаре, откуда получила название сама кислота и ее производные сукцинаты (от лат. succinium - янтарь).
Глутаровая кислота (Пентандиовая кислота) - двухосновная предельная карбоновая кислота. Обладает достаточно высокой растворимостью в воде. Используется в производстве полимеров, типа полиэстера и полиамидов.
Кето-производное глутаровой кислоты - α-кетоглутаровая кислота (α-кетоглутарат) является важным биологическим соединением. Эта кетокислота образуется при дезаминировании глутамата, и является одним из промежуточных продуктов цикла Кребса.
Оксалаты - соли и эфиры щавелевой кислоты. Соли содержат в своём составе дианион (оксалат) C2O42− или (COO)22−, образующийся при двойном депротонировании щавелевой кислоты.
Большинство солей оксалатов малорастворимы в воде, например, оксалат кальция, который используется для обнаружения кальция. Хорошо растворимы оксалат калия и аммония.
Анион оксалата может выступать в качестве бидентатного лиганда, образуя пятичленный цикл MO2C2, как например, в ферриоксалате калия - K3[Fe(C2O4)3]. Благодаря его хорошей растворимости щавелевая кислота используется для удаления ржавчины.
Оксалаты широко распространены в природе, например, в щавеле. Корни и/или листья ревеня, гречихи содержат щавелевую кислоту. Накопление щавелевой кислоты происходит из-за неполного окисления углеводов в процессе биосинтеза.
Следующие съедобные растения содержат оксалаты в порядке уменьшения концентрации чёрный перец, петрушка, семена мака, шпинат, сахарная свекла, какао, шоколад, большинство орехов и ягод, фасоль.
Листья чайного куста содержат большое относительное количество оксалатов по отношению к другим растениям. Обычно его экстракты содержат от малых до средних концентраций оксалатов благодаря малой массе используемых листьев.
Сродство оксалата к двухвалентным катионам отражается в способности к образованию нерастворимых осадков. Так в организме оксалат соединяется с катионами, такими как Ca2+, Fe2+ и Mg2+. Вследствие чего накапливаются кристаллы соответствующих оксалатов, которые из-за своей формы раздражают кишечник и почки. Поскольку оксалаты связывают важные элементы, например кальций, то долгое питание пищей, содержащей много оксалатов, может вызвать проблемы со здоровьем.
Здоровый человек может безопасно питаться пищей с оксалатами в умеренных количествах, но для людей с болезнями почек, подагрой, ревматоидным артритом рекомендуется избегать пищи с большим количеством оксалатов. Кристаллы оксалата кальция, более известные как почечный камень, забивают почечные протоки. Считается, что 80 % почечных камней образуется из оксалата кальция.
Аналогично, большие поступления кальция совместно с пищей содержащей оксалаты приводит к выпадению оксалата кальция в пищеварительном тракте, уменьшая поступления оксалатов в организм на 97 %.
Окисление янтарной кислоты in vivo. Дегидрирование (окисление) янтарной кислоты в фумаровую, катализируемое в организме ферментом, осуществляется с участием кофермента ФАД. Реакция протекает стереоспецифично с образованием фумаровой кислоты (в ионной форме - фумарат).
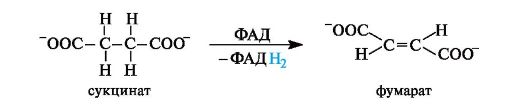
Сукцинатдегидрогеназа (КФ 1.3.99.2) катализирует превращение янтарной кислоты в фумаровую. Кофактором фермента является ФАД. Фермент прочно связан с внутренней мембраной митохондрий.
Дата добавления: 2015-05-26; просмотров: 15846;
