Калибровка реографического мониторинга
Расхожее мнение об ошибках реографического определения МОК побудило нас верифицировать результаты реомониторинга по какому-либо эталону. Это, с одной стороны, поедставлялось необходимым для независимой оценки точности метода, с другой — создавало возможность уточнить в динамике результаты неинвазивного измерения МОК, единожды откалибровав реомонитор на конкретном больном.
Более низкая воспроизводимость и большая частота "зксцессивных" результатов термодилюции по сравнению с реографией заставили нас отказаться от первоначального намерения калибровать реомонитор по катетеру Swan-Ganz. Метод Фика и допплерография были отвергнуты также из-за значительных и разнонаправленных погрешностей. Более того, современное представление о "независимых" нормативах МОК, измеренного различными способами [1039, 1455], породило следующую идею. Несостоятельность всех методов измерения МОК, включая термодилюцию, в роли эталона измерения побуждает искать принципиальную альтернативу, которой мог бы стать эталон измеряемой величины (потока) — искусственно создаваемый МОК со строго заданными параметрами. Такие условия создают либо работа имплантированного искусственного сердца (эта модель использовалась J.J. Rouby и соавт. для изучения в чистом виде вазотропных эффектов анестетиков [1289, 1290]), либо традиционное искусственное кровообращение во время кардиохирургических операций.
Доступ к последнему методу предоставило нам сотрудничество с кардиохирургическим центром ДГБ №1. Перфузиологи во главе с И.Н. Меньшугиным, изучая постперфузионный водный баланс у детей, применили для этой цели реографический монитор, аналогичный нашему. Начав работать вместе, мы стали параллельно изучать баланс водных секторов и гемодинамику оперируемых детей в исходном состоянии, во время ИК и в постперфузионном периоде.
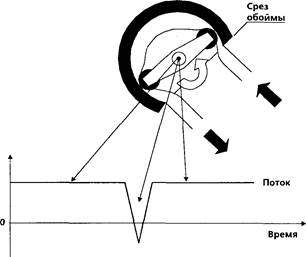
Рисунок 17.
Уже первые записи выявили ряд неожиданных для нас моментов. Главным из них оказалось отсутствие принципиальной физической разницы между непрерывным и пульсирующим потоком. Поясним механизм этого феномена схемой (рис.17). Работа роликового перистальтического насоса в режиме непрерывного потока соответствует вращению его ротора с постоянной угловой скоростью. Однако конструкция насоса такова, что подача жидкости осуществляется дискретными порциями, объем которых соответствует отрезкам насосного сегмента между роликами. При этом в момент, когда ролик проходит точку выхода насосного сегмента из обоймы, не только прерывается подача жидкости, на благодаря релаксации сжатого роликом отрезка трубки в выходной магистрали возникает кратковременный обратный ток. Это создает "квазинепрерывный" поток, пульсации которого хорошо видны не только на реомониторе, на также на кривых инвазивного монитора АД и пульсоксиметра; частота пульсации равна удвоенной частоте вращения двухроликового ротора. Образец реосигнала, записанного у ребенка с массой тела 12 кг при частоте вращения ротора 66 мин-1 в режиме "непрерывного" потока, показан на рис.18. Вверху приведена ось с отметкой времени и длительностью записи (426 с); частота пульсации потока составляет 132 мин-1.
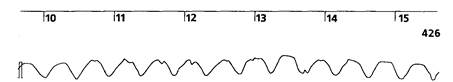
Рисунок 18.
С пульсирующим потоком дело обстоит сложнее из-за несовпадения заданного объема подачи за один такт и объема насосного сегмента между роликами. Совершив поворот на угол, соответствующий отрезку насосного сегмента с заданным (тактовым) объемом, ротор останавливается в различных угловых положениях по отношению к срезу обоймы. Это несовпадение приводит к периодичному фазовому сдвигу структуры рабочего цикла. Поскольку при управлении насосом выдерживается постоянный для данного режима угол поворота ротора за один такт, а угловые положения ротора в момент остановки не учитываются, тактовый объем подачи также циклически меняется — колеблется с периодом, зависящим от его величины и диаметра насосного сегмента. Реограмма, приведенная на рис. 19, отражает наложение по крайней мере двух частот: стрелками под кривой отмечены остановки ротора, формирующие заданные пульсации потока, стрелки вверху маркируют "внеплановые" колебания потока, возникающие из-за прохождения ротором среза обоймы. Видно, что поток в течение цикла становится бимодальным, и, таким образом, допущения формулы М.И. Тищенко [180], как и большинства других, оказываются недействительными. Кроме того, такие комплексы нередко не распознаются реомонитором, становится невозможной разметка кривой и, следовательно, автоматическая обработка реограммы.
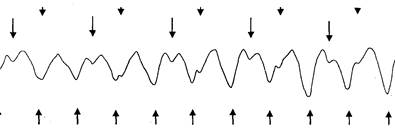
Рисунок 19.
Еще более интересной оказалась реографическая картина при совместной работе АИК и сердца ребенка в случае "неполного" ИК. Кривая, представленная на рис. 20 А, отражает феномен, известный в теории колебаний какбиения и обусловленный интерференцией колебаний различной частоты. Это различие частот приводит к периодичному фазовому сдвигу, минимум которого соответствует максимуму амплитуды результирующих колебаний и наоборот. Период фазового сдвига равен наименьшему общему кратному периодов интерферирующих колебаний. Сигнал, представленный на рис. 20 А, записан во время неполного ИК у ребенка 4 лет 2 мес. при ЧСС 90 мин-1 (ЭКГ, синхронная с реосигналом, представлена на рис. 20 Б), частоте пульсации АИК 105 мин-1 и объемной скорости перфузии 1600 мл•мин-1.
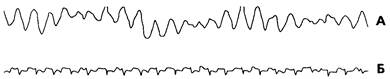
Рисунок 20.
Несмотря на такую сложность фазовой структуры потока, мы записывали реосигналы при всех возможных режимах работы АИК. Если обработка кривой не выполнялась автоматически, что нередко встречалось при пульсирующем потоке, ее проводили после ручной разметки границ отдельных кардиоциклов. Учитывая отмеченную выше принципиальную разницу между пульсирующим и "непрерывным" потоком, мы исследовали соответствующие им группы реосигналов раздельно. В общей сложности было обработано 30 записей, сделанных на фоне пульсирующего и 18 — на фоне "непрерывного" потока. Поскольку непосредственно рассчитываемой величиной при реографии является ударный объем, анализу подверглись все величины тактовой производительности АИК, зафиксированные в 20-секундных фрагментах записей, сделанных на фоне пульсирующего потока и в 40-секундных — на фоне "непрерывного" потока (выбор длины фрагментов диктовался ограничением максимально допустимого размера матрицы в пакете "MatLab"). Далее по результатам расчета каждого отдельно взятого кардиоцикла (аппаратный "УОК") вычислялось соответствующее ему значение реографического СИ (СИр), которое затем сопоставлялось с заданным СИ АИК (СИа). Для пульсирующего потока, таким образом, общий объем выборки составил 1042 реографических измерения при 25 дискретных значениях тактовой производительности артериального насоса, варьировавших от 2,6 до 40,4 мл. На фоне "непрерывного" потока оказались доступны 1406 результатов реографического расчета, соответствующих всего лишь1величине реальной тактовой производительности — 12,7 мл. Такое единообразие в последнем случае объясняется тем. что в режиме "непрерывного" потока тактовая производительность однозначно определяется диаметром используемого насосного сегмента, типоразмер которого применялся всего лишь один — с внутренним диаметром 9,53 мм (3/8 дюйма).
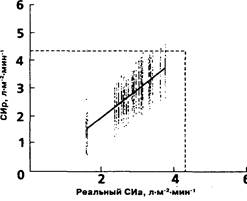
Рисунок 21.
Результаты обработки первой группы данных представлены на графике (рис. 21): величина коэффициента линейной корреляции между СИа и СИр составила 0,76. Таким образом, корреляция данных реографии с эталонным потоком АИК оказалась более низкой, чем с результатами термодилюционного метода измерения МОК. Заметно и принципиальное отличие от графика, демонстрирующего сравнение термодилюции и реографии (рис. 14): в случае АИК объемная производительность (СИа) является заданной величиной. Поэтому результаты отдельных замеров образуют на графике не облако точек, как в случае с термодилюцией, а группы точек, лежащих на одной прямой. Точечная проекция этих комплексов на ось абсцисс отражает соответствующие им фиксированные значения заданного СИа. Линейная аппроксимация зависимости между СИа и СИр, представленная на графике прямой, выражается следующими равносильными уравнениями регрессии, полученными методом наименьших квадратов:
СИр = 1,03СИа - 0,13 (20)
СИа= 0,97СИр + 0,13 (21)
Из уравнений следует, что реогрофия несколько занижает реальные величины производительности АИК в нормальном диапазоне их значений (а именно при СИа < 4,33 л•м2•мин-1; это граничное значение отмечено на графике пунктирными линиями). График, отражающий результаты обработки реосигналов, записанных на фоне "непрерывного" потока, представлен на рис. 22. Коэффициент корреляции реальной и измеренной величин СИ составил здесь 0,84, превысив, таким образом, степень корреляции данных реографии и термодилюции. Уравнения регрессии для данной выборки выглядят следующим образом:
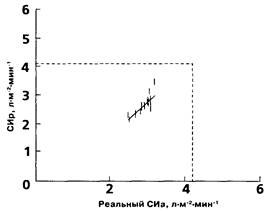
,
Рисунок 22.
СИр=1,19СИа-0,78 (22)
СИа=0,84СИр+0,66 (23)
Интересно, что при более тесной корреляции реальной и измеренной величинточность измерения тактовой производительности АИК в этом случае оказывается ниже (в уравнениях регрессии вида y=kx+z вo втором случае k больше отличен от 1, а z—от 0). Из уравнений (22) и (23) следует, что точка равенства реального СИа и СИр соответствует 4,11л•м2•мин-1 (отмечено пунктиром). Как видно из графика и величины Rxy самым заметным отличием случая "непрерывного" потока от предыдущего (рис. 21) является значительно меньшая величина разброса результатов реографического расчета СИ. Причина этого, по-видимому, заключается в разобранной выше сложной структуре потока при пульсирующем режиме: больший разброс результатов реографии может отражать дисперсию реальных значений тактовой производительности артериального насоса. Для проверки этой гипотезы мы проанализировали статистическое распределение ошибки реографического определения тактовой производительности АИК в режимах пульсирующего и "непрерывного" потоков. Результаты, представленные на графиках, свидетельствуют о значительных различиях формы распределения (рис. 23: абсцисса — отклонение СИр от СИа, выраженное в процентах последней величины с шагом шкалы10%: ордината — абсолютная частота встречаемости данной величины ошибки в выборке). В случае пульсирующего потока (рис. 23 А) пик распределения сглаживается, отражая набор вариантов тактовой производительности, обусловленных периодичным фазовым сдвигом. В то же время случай "непрерывного" потока (рис. 23 Б), исключающий различие производительности насоса от такта к такту, демонстрирует распределение ошибки с более выраженной модой.
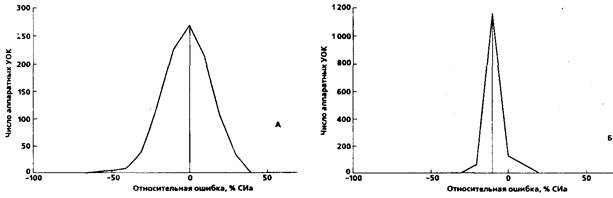
Рисунок 23.
Необходимо отметить, однако, что если в случае А (пульсирующий поток) пик распределения приходится на нулевую ошибку, то в случае Б ("непрерывный" поток) он сдвинут к величине ошибки, равной - 10%. Таким образом, графики наглядно подтверждают вытекающее из соответствующих коэффициентов корреляции и уравнений регрессии превалирование в случае А случайной, а в случае Б — методической ошибки. Несимметричный характер распределения ошибки в случае А (площадь под кривой в секторе отрицательных значений ошибки больше, чем в секторе ее положительных значений) объясняется, по-видимому, тем, что ось абсцисс на графике А представлена неистинными, а расчетными значениями тактовой производительности. Первая величина оказывается меньше второй, очевидно, за счеттого, что заданный угол поворота ротора (рад) за один такт рассчитывается как постоянная величина, равная
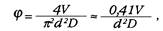 (24)
(24)
где V — заданная тактовая производительность, мл, d — внутренний диаметр насосного сегмента. см, D — внутренний диаметр его обоймы, см. При этом не учитывается описанный выше изменяющийся фазовый сдвиг углов старта и остановки ротора, приводящий < уменьшению тактовой производительности на отличную от нуля переменную величину. Из такого вида мономодального распределения ошибки для случая пульсирующего потока вытекает, что

где k и z — соответственно, коэффициент и свободный член линейного уравнения вида (20), в данном случае 1,03 и -0,13. Практически это означает, что при увеличении числа обработанных кардиоциклов результат расчета производительности АИК реографическим способом монотонно стремится к значению, задаваемому уравнением регрессии. Точность расчета здесь повышается еще и за счет полной идентичности периодов всех обрабатываемых циклов, что исключено при работе сердца в собственном ритме. Таким образом, наличие случайной ошибки реографического определения МОК, имеющей распределение с выраженной нулевой модой, обосновывает эмпирически предложенные "усредняющие" алгоритмы обработки реосигнала [551]. Проблемой остается, таким образом, методический компонент ошибки, который в наших наблюдениях, как это ни странно на первый взгляд, оказался выше при большей стереотипности реальной тактовой производительности АИК. Мы предположили, что причиной более выраженной методической ошибки в случае "непрерывного" потока является более высокая тактовая частоте искусственных кардиоциклов. В самом деле. этот фактор был наиболее существенным отличием между группами: если взять полные объемы выборок, средний период при пульсирующем потоке составил 0,57±0,05 с, тогда как при "непрерывном" потоке эта величина, не ограничиваемая здесь физиологическими нормативами, оказалась равной 0,45 ± 0,07 с. Для проверки этой гипотезы мы исследовали зависимость относительной ошибки реографического определения СИ (А = (СИр-СИа)•СИа) от величины периода кардиоцикла Т (с) раздельно в группах пульсирующего и "непрерывного" потоков. Результаты представлены на рис. 24 (соответственно, А и Б). В случае А коэффициент корреляции между периодом и величиной ошибки оказался несущественным (0,16). В то же время в случае Б была выявлена значимая корреляция (R, = 0,92), а взаимосвязь выразилась уравнением регрессии:
Δ =0,69T-0,4 (26)
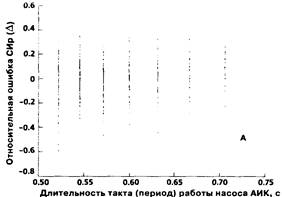
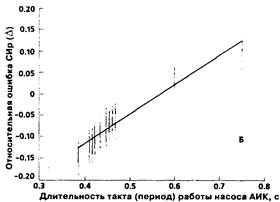
Рисунок 24.
Таким образом, в случае "непрерывного" потока величина ошибки действительно оказалась зависимой от периода (или частоты) ритма. При этом визуальная оценка графика (рис. 24 Б) позволяла предположить, что особенно значимая корреляция между Т и Д существует при значениях Т < 0,5 с, тогда как при больших значениях периода (т.е. в зоне перекрывания диапазонов Т пульсирующего и "непрерывного" потоков) зависимость слабеет. Действительно, исключение из выборки значений Т>0,5 сдало еще более яркую картину зависимости относительной ошибки от периода (рис. 25). Коэффициент корреляции здесь составил 0,82, а уравнение регрессии выглядело как
Δ=1,15T-0,59 (27)
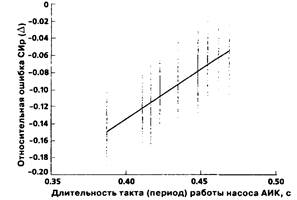
Рисунок 25.
График и уравнение (27) демонстрируют более резко выраженную зависимость А от Т (по сравнению с уравнением (26) аналогичного вида у = кх + z в уравнении (27) больше величина k и модуль величины z). Меньшее значение коэффициента корреляции отражает меньшую величину отношения баз расчета Rxy по абсциссе и ординате к дисперсии ординаты (соотношение "полезный сигнал/шум").
Следовательно, методическая ошибка реографии, занижающая тактовую производительность артериального насоса АИК, действительно существует и прогрессивно нарастает с увеличением частоты следования тактов работы насоса: в нашей выборке наблюдений особенно заметно влияние этой ошибки сказывалось при длительности периода Т < 0,5 с, соответствующей тактовым частотам выше 120 мин-1. Возможно, причиной данного феномена является экспоненциально нарастающая по мере укорочения периода нелинейность артериального наполнения и венозного оттока, прогрессивно выводящая процесс за рамки допущений формулы М.И. Тищенко [180]. Дополнительным фактором, ослабляющим влияние частоты на ошибку измерений при Т > 0,5 с, является отмеченное выше преобладание при пульсирующем потоке случайной ошибки, снижающей общий коэффициент корреляции данных до 0,76.
Пользуясь данными, полученными во время искусственного кровообращения, у 13 детей осуществили реографический мониторинг в постперфузионном периоде. При этом для целей настоящего исследования было записано 16 образцов реосигнала. Принцип калибровки реографического мониторинга по АИК, лежавший в основе данной программы, предполагал экстраполяцию уравнения регрессии, полученного по эталонному потоку, на измерение производительности сердца больного. Вывод уравнения вида y=kx+z, основанный на предположении о линейном характере ошибки, требует наличия данных расчета СИр не менее чем при двух значениях эталонного потока; достоверность результата при этом оказывается тем выше, чем больше различие этих двух значений (база расчета регрессии). Такое оказалось возможным в трех случаях, когда объемная скорость перфузии менялась в ходе ИК. В качестве примера полной серии наблюдений на рис. 26 приведены записи реосигнала у ребенка 8 мес. до начала (А), во время ИК в режиме пульсирующего потока с частотой 115 мин-1 при ОСП 11 20 мл•мин-1 (Б) и 570 мл•мин-1 (В) и в постперфузионном периоде (Г).
В итоге оказалось возможным, во-первых, сделать более точным неинвазивное измерение МОК после завершения ИК, во-вторых, сравнить дооперационную величину сердечного выброса (также уточненную по данным калибровки) с его постперфузионным значением. Так, в приведенном на рис. 26 примере скорректированное значение СИр до операции составило 2,6 л•м2•мин-1 (против 2,45 по некорректированным показаниям монитора), а после операции — 2,35 л•м-2•мин-1 (запись, приведенная на рис. 26 Г; некорректированное значение здесь составило 2,2 л•м-2•мин-1).

Рисунок 26.
Таким образом, даже при существенно измененной структуре кардиоцикла, не встречающейся в естественных условиях, и заметно отличающихся от взрослых пропорциях тела ребенка, мониторинг интегральной реограммы тела по М.И. Тищенко обеспечивает хорошую корреляцию результатов с истинными значениями расхода крови в большом круге кровообращения. Калибровка реографического монитора на конкретном больном по эталонному потоку аппарата искусственного кровообращения позволяет осуществить коррекцию получаемых результатов, уменьшив влияние методической ошибки.
Заключение
Состояние кровообращения определяют три главные составляющие: объем крови, тонус сосудов и механика миокарда. В виде преднагрузки, постнагрузки и сократительного статуса желудочков влияние этих трех детерминант фокусируется в величине минутного объема кровообращения, определяющего, в свою очередь, глобальную доставку кислорода. Сердечный выброс, падение которого играет центральную роль в патогенезе всех вариантов острой циркуляторной недостаточности, является главным гарантом гемодинамичёской стабильности организма. Однако мониторинг минутного объема до сих пор сопряжен со значительными техническими трудностями. Исторически первые методы, основанные на использовании газообразных индикаторов, помимо трудоемкости и дороговизны, страдают большими методическими погрешностями. Анализ разведения жидких индикаторов получил широкое распространение в виде термодилюции — высокоинвазивной процедуры, многие годы считавшейся эталонным методом измерения сердечного выброса.
Сегодня одной из доминирующих тенденций стал отказ от инвазивности во всех ситуациях, где это только возможно, даже при условии сознательной потери некоторого количества диагностической информации. По этой причине термодилюции все чаще предпочитают эхолокационные и импедансометрические методы. Однако развитие эхолокации концентрируется на уникальных возможностях оценки локальной кинетики стенки сердца, тогда как в измерении объемов точнее оказалась импедансометрия. Техническое удобство и экономическая выгода также на стороне последнего метода.
Сравнение точности различных методов привело к выводу о правомерности существования независимых стандартов измерения МОК, в частности термодилюционного, эхографического и импедансометрического.
Важной проблемой является энергетическая оценка кровообращения — с позиций как глобального аэробного обмена, так и адекватности энергозатрат сердца. К сожалению, в литературе отсутствует системное представление об оптимальной пропорции между этими взаимосвязанными аспектами гомеостаза. В клинике управление сердечным выбросом нередко подчинено доктринам, экстремизм которых означает выбор между системной гипоксией и ишемией миокарда.
Итак, мониторинг МОК считается "крайне полезным для пациентов в операционной и палате интенсивной терапии" [11 83] и "необходимым для больных с заболеваниями сердца, требующих оперативного лечения" [609]. Однако использование такого мониторинга является, особенно в нашей стране, почти исключительной прерогативой кардиоанестезиологии — несмотря на то, что проблема адекватности насосной функции сердца намного шире. Она актуальна не только для каждого хирургического больного с сопутствующей сердечно-сосудистой патологией, на и во всех ситуациях, чреватых развитием во время анестезии острых циркуляторных расстройств.
Таким образом, сегодня логичным следующим шагом представляется концептуальное и методическое обоснование внедрения мониторинга МОК в практику общей анестезиологии. В клиническом материале нашего собственного исследования оказались представлены плановая и экстренная хирургия, включая общехирургические и специальные вмешательства, в том числе операции на открытом сердце у детей в условиях гипотермии и искусственного кровообращения. Таким образом, сформированная выборка клинических наблюдений является достаточно представительной для суждения о предмете настоящего исследования. Спектр методов обезболивания включил практически все применяемые сегодня методики: от традиционных видов общей, регионарной и комбинированной анестезии до наиболее современных вариантов, в том числе адренопозитивной и аденозиновой аналгезии. Уровень технического обеспечения анестезии также варьировал от широко распространенной устаревшей аппаратуры до вполне современных образцов. Для исследования гемодинамики во время операции и анестезии использовали практически весь набор современных методик как инвазивного, так и неинвазивного характера. При этом значительную долю показателей регистрировали в реальном масштабе времени (мониторинг), а главное внимание уделяли динамической оценке минутной производительности сердца и системного сосудистого сопротивления. С целью верификации значений этих показателей применяли дублирование методик их измерения.
Статистическая обработка данных была ориентирована на предельную строгость математических подходов, в результате чего обеспечивалось полное отсутствие произвольных допущений (информационных артефактов обработки) и, с другой стороны, предотвращалась потеря информации.
Предложена специальная графическая форма представления результатов, повышающая его наглядность и возможности анализа данных. Таким образом, представительность материала, выбор методов исследования и представления показателей создают все необходимые предпосылки для достоверности как первичных данных, так и результатов их обработки и анализа. Опыт клинического использования реографического мониторинга центральной гемодинамики позволяет охарактеризовать его как простой в использовании и не имеющий противопоказаний неинвазивный метод контроля кровообращения во время анестезии. С метрологической точки зрения он отличается достаточно высокой точностью, подтвержденной не только сравнением его результатов с результатами метода термодилюции, на и калибровкой по эталонному потоку различной фазовой структуры, создаваемому аппаратами искусственного кровообращения в условиях гипотермии и кардиоплегии. Воспроизводимость данных реографического мониторинга оказалась выше, чем у термодилюционного измерения сердечного выброса и не зависела при этом от реальной величины МОК. Основной проблемой метода остается сравнительно невысокая помехозащищенность, приводящая в условиях операционной к появлению многочисленных артефактов и заставляющая в ряде случаев переходить на огрубленные алгоритмы обработки сигнала. В то же время точное соблюдение технических деталей позволяем значительно снизить уровень помех. Создание алгоритмов обработки сигнала, снижающих влияние помех и артефактов записи, также может существенно повысить точность и надежность метода.
Катетеризация легочной артерии баллонным катетером Swan-Ganz, примененная нами в качестве метода сравнения по общепринятым клиническим показаниям, проявила себя относительно несложным технически и при условии неторопливого исполнения достаточно безопасным методом. Не предоставляя врачу дополнительной ценной информации относительно производительности сердца и ОПСС, методика оказывалась незаменимой в условиях рассогласования преднагрузки желудочков.
Ситуации, предрасполагающие к такому рассогласованию, и являются основным показанием к катетеризации ЛА, тогда как контроль сердечного выброса и сосудистого сопротивления большого круга может успешно осуществляться с помощью неинвазивного реомониторинга.
Интересной клиника-экспериментальной моделью является реографическое измерение потока, создаваемого во время операций с искусственным кровообращением артериальным насосом АИК, работающим в различных режимах. Теоретическое значение данной модели состоит в возможности оценки точности реографии по эталонному потоку различной временной и фазовой структуры, а практическое — в калибровке реографического метода по эталонному потоку на конкретном больном, что повышает точность измерения производительности сердца в постперфузионном периоде.
Дата добавления: 2015-06-10; просмотров: 1311;
