Биуретовая реакция
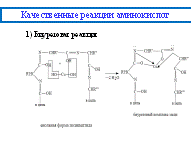 При взаимодействии 1-2 мл разбавленного белка с 2-3 мл 1% раствора CuSO4 в щелочной среде (2-4 мл 30% раствора NaOH) развивается фиолетовое окрашивание.
При взаимодействии 1-2 мл разбавленного белка с 2-3 мл 1% раствора CuSO4 в щелочной среде (2-4 мл 30% раствора NaOH) развивается фиолетовое окрашивание.
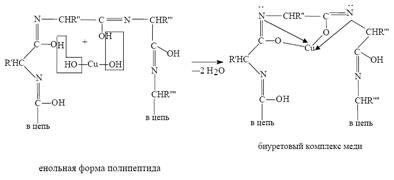
Механизм данной реакции связан с образованием комплексных соединений меди с атомами азота полипептидной цепи. Щелочная среда требуется для депротонирования атомов азота.
2) Нингидриновая реакция на α-аминокислоты
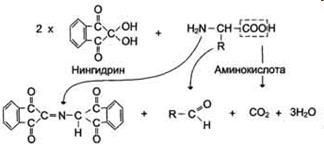
Эта реакция основана на том, что бесцветный нингидрин, реагируя с аминокислотой, конденсируется в виде димера через атом азота, отщепляемый от α -аминогруппы аминокислоты. В результате образуется пигмент красно-фиолетового цвета. Одновременно происходит декарбоксилирование аминокислоты, что приводит к образованию СО2 и соответствующего альдегида. Нингидриновую реакцию широко используют при изучении первичной структуры белков (см. схему ниже).
Аргинин определяют с помощью качественной реакции на гуанидиновую группу (реакция Сакагучи), а цистеин выявляют реакцией Фоля, специфичной на SH-группу данной аминокислоты. Наличие ароматических аминокислот в растворе определяют ксантопротеиновой реакцией (реакция нитрования), а наличие гидроксильной группы в ароматическом кольце тирозина - с помощью реакции Миллона.
При взаимодействии белка со спиртовым раствором нингидринапри температуре 700 С развивается сине-фиолетовое окрашивание.
Реакция проходит в 2 стадии:
1- стадия. Эта реакция основана на том, что бесцветный нингидрин, реагируя с аминокислотой с образованием дикетодигринамина. Одновременно происходит декарбоксилирование аминокислоты, что приводит к образованию СО2 и соответствующего альдегида.
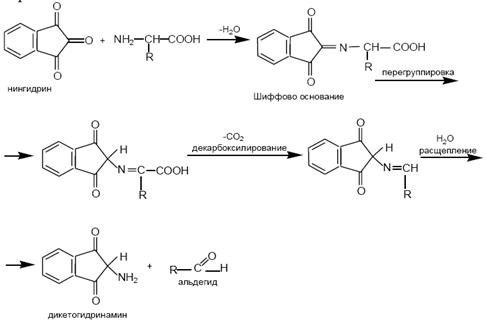
2 стадия.Дикетодигринамин конденсируется в виде димера через атом азота, отщепляемый от α -аминогруппы аминокислоты.
В результате образуется пигмент сине-фиолетового цвета (пурпура Руэманна).
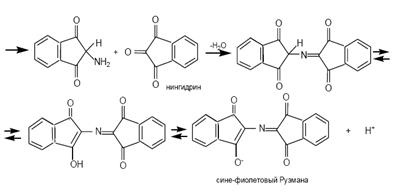
Нингидриновую реакцию широко используют при изучении первичной структуры белков (см. схему ниже).
3) Ксантопротеиновая реакция – например, по ароматическому кольцу тирозина
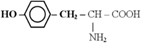
При взаимодействии белка с концентрированной азотной кислотой белок выпадает в осадок. При нагревании раствор и осадок окрашиваются в ярко-желтый цвет. При этом осадок почти полностью растворяется.
Смесь охладить и по каплям добавить избыток NH4OH или NaOH до щелочной реакции. Вначале выпадает осадок кислотного альбумина растворяется и раствор окрашивается в ярко-оранжевый цвет.
Переход желтой окраски в оранжевую в щелочной среде обусловлен изменением структуры щелочных солей этих нитросоединений.
Желатина, не содержащая ароматических аминокислот, не дает этой реакции.
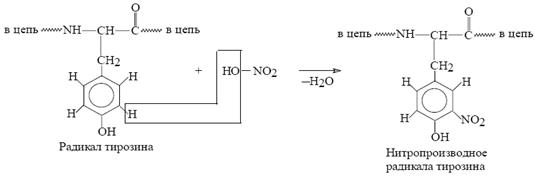
2) 3)
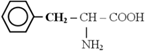
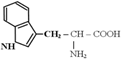
фенилаланин триптофан
Ксантопротеиновая реакция зависит от наличия в белках остатков ароматических аминокислот [фенилаланина (2), тирозина (1), триптофана (3)].
Эти аминокислоты в результате нитрования образуют желтоокрашенные нитросоединения.
Дата добавления: 2015-06-05; просмотров: 4937;
