Разделение аминокислот с помощью ионообменной хроматографии
Смесь аминокислот, полученных кислотным гидролизом белков, разделяют в колонке с катионообменной смолой. Такая синтетическая смола содержит прочно связанные с ней отрицательно заряженные группы (например, остатки сульфоновой кислоты -SO3-), к которым присоединены ионы Na+ (рис. 3).
В катионообменник вносят смесь аминокислот в кислой среде (рН = 3,0), где аминокислоты в основном представляют катионы, т.е. несут положительный заряд. Положительно заряженные аминокислоты присоединяются к отрицательно заряженным частицам смолы. Чем больше суммарный заряд аминокислоты, тем прочнее её связь со смолой. Так, аминокислоты лизин, аргинин и гистидин наиболее прочно связываются с катионообменником, а аспарагиновая и глутаминовая кислоты - наиболее слабо.
Высвобождение аминокислот из колонки осуществляют вымыванием (элюированием) их буферным раствором с увеличивающейся ионной силой (т.е. с увеличением концентрации NaCl) и рН. При увеличении рН аминокислоты теряют протон, в результате уменьшается их положительный заряд, а, следовательно и прочность связи с отрицательно заряженными частицами смолы.
Каждая аминокислота выходит из колонки при определённом значении рН и ионной силы. Собирая с нижнего конца колонки раствор (элюат) в виде небольших порций, можно получить фракции, содержащие отдельные аминокислоты.
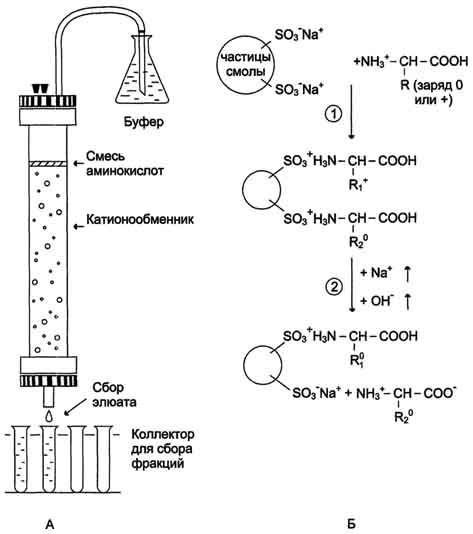
Рис. 3. Разделение аминокислот с помощью ионообменной хроматографии.
А. Хроматограсрическая колонка, наполненная катионообменной смолой.
Б. Этапы разделения аминокислот: 1 - присоединение аминокислот к частицам смолы; 2 - высвобождение аминокислот при определённом значении рН и концентрации NaCl.
Дата добавления: 2015-05-26; просмотров: 9188;
