Формы выражения теплоемкости.
Из уравнения первого начала после его дифференцирования по температуре следует:
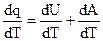 , (2.1)
, (2.1)
где 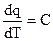 и называется истинной теплоемкостью.
и называется истинной теплоемкостью.
Истинная теплоемкость показывает, какое количество теплоты следует подвести к системе для заданного повышения ее температуры.
Часто, особенно при решении практических задач, пользуются величиной средней теплоемкости:
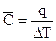 , (2.2)
, (2.2)
где 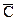 - средняя теплоемкость;
- средняя теплоемкость;
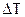 - изменение температуры системы.
- изменение температуры системы.
В зависимости от того, к какому количеству (массе) вещества относится рассматриваемая теплоемкость, различают:
а) удельную теплоемкость, определяющую то количество теплоты, которое необходимо сообщить системе массой 1 кг для ее нагрева в заданном температурном интервале, Дж/кг К;
б) молярную теплоемкость, характеризующую то количество теплоты, которое необходимо сообщить системе с количеством вещества 1 моль, для ее нагрева в заданном температурном интервале, Дж/моль К.
Функция q не является функцией состояния, поэтому и теплоемкость так же зависима от условий совершения процесса теплопередачи.
В этой связи различают изобарическую (СР) и изохорическую (СV) теплоемкости.
Из уравнения (2.1) следует, что для условий V = const (изохорический процесс) справедливо следующее:
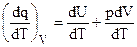 , (2.3)
, (2.3)
где dV = 0, поэтому:
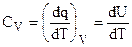 . (2.4)
. (2.4)
Для изобарических условий ведения процесса (р = const):
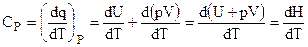 . (2.5)
. (2.5)
Сравним СV и СР:
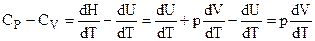 . (2.6)
. (2.6)
Из уравнения состояния идеального газа:
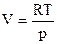 . (2.7)
. (2.7)
Тогда (2.6) с учетом (2.7) запишется в виде (2.8):
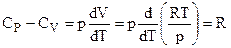 ,
,
т. е.
СР - СV = R. (2.8)
Соотношение (2.8) называется формулой Майера для идеальных газов.
Для твердых веществ различие между СР и СV невелико, а их взаимозависимость описывается более сложным соотношением:
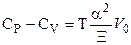 , (2.9)
, (2.9)
где Т - температура;
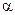 - изобарический коэффициент линейного расширения;
- изобарический коэффициент линейного расширения;
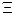 - изотермический коэффициент сжатия;
- изотермический коэффициент сжатия;
V0 - молярный объем вещества при 0 К.
Дата добавления: 2015-05-21; просмотров: 1450;
