У СХЕМАХ ВПУ
4.1. ЗАГАЛЬНІ ПОЛОЖЕННЯ|становища|
У зв'язку з наростаючим значенням захисту водоймищ від скидань|скидів| різних домішок|нечистот| з промислових підприємств, у тому числі і з|із| ВПУ ТЕС, останніми роками зросла увага до безреагентних методів для знесолення води. В наш час|нині| найбільш розроблені для практичного застосування мембранні методи. Відомо декілька видів мембранних процесів: ультрафільтрація|, зворотний осмос (гіперфільтрація), електродіаліз, діаліз. У основі| всіх мембранних методів лежить перенесення|перенос| домішок|нечистот| або розчинників через мембрани. Природа сил, що викликають|спричиняють| це перенесення|перенос|, може бути різною. Відповідно розрізняються і мембрани, що застосовуються в таких процесах. При використанні сил тиску|тиснення| (ультрафільтрація| і зворотний осмос) мембрани повинні пропускати розчинник (воду), в максимальному ступені|мірі| затримуючи іонні і молекулярні домішки|нечистоти|. При використанні електричних сил мембрани мають бути проникні для іонів і не повинні пропускати воду.
Сфери застосування мембранних процесів для очищення води різні. Так, якщо зворотний осмос для уникання застосування дуже високого тиску найбільш економічний в основному для розчинів з концентрацією розчинених речовин до 1 г/кг, то електродіаліз використовується, як правило, для більш концентрованих розчинів. В порівнянні з іншими методами мембранні методи мають наступні переваги:
1) відсутні фазові переходи при відділенні домішок, що дозволяє зводити до мінімуму витрату енергії на проведення процесів:
2) розділення можна проводити при низьких температурах води, які визначаються властивостями мембрани;
3) якщо виключити забивання мембрани, процеси мають безперервний характер;
4) їх можна здійснювати без додавання хімічних реагентів (якщо добавки і вводяться, то в дуже невеликих кількостях);
5) апарати для здійснення цих процесів відносно прості і не мають рухомих часток.
Кількість енергії, необхідної для мембранних процесів, зазвичай не перевищує 2 – 2,5кВт·год./м3 фільтрату.
До безреагентних| методів відносяться також десорбційні методи видалення|віддалення| газів з|із| води.
4.2. ЗВОРОТНИЙ ОСМОС І УЛЬТРАФІЛЬТРАЦІЯ|
Методи зворотного осмосу і ультрафільтрації| заключаются| у фільтруванні розчинів через спеціальні напівпроникні мембрани. При цьому мембрана пропускає або тільки|лише| молекули розчинника (води), або частково з|із| розчинником проходять іони і молекули затримуваних речовин. При зворотному осмосі здійснюється відділення|відокремлення| часток|частинок| (молекул, гідратованих іонів), розміри яких сопоставимы| з розмірами молекул розчинника, тоді як при ультрафільтрації| мінімальні розміри затримуваних часток|частинок| на порядок більше, причому максимальні їх розміри не повинні перевищувати 0,5 мкм|.
Якщо частки|частинки| мають розміри більше 0,5 мкм|, для їх відділення|відокремлення| необхідно застосовувати власне фільтрування. Інколи|іноді| нижня межа часток|частинок|, що видаляються|віддаляють| ультрафільтрацією|, характеризують їх молекулярною масою, рівною 500.
В основу процесу зворотного осмосу покладено явище осмосу – самовільного| переходу розчинника через спеціальну напівпроникну перегородку (мембрану) в розчин|. Якщо яке-небудь вічко|комірку| розділити мембраною і залити ліву частину|частину| чистою водою, а праву розчином (рис. 4.1), то буде спостерігатися самовільний перехід молекул води з|із| лівої частини|частини| в праву. Рушійною силою процесу при цьому є|з'являється| різниця концентрацій води в лівій і правій частинах|частинах| вічка|комірки|. При цьому рівень води в лівій частині|частині| вічка|комірки| знижуватиметься, а в правій підвищуватися. Унаслідок|внаслідок| виникнення гідравлічного натиску|напору| за рахунок різниці рівнів води в обох частинах|частинах| вічка|комірки| вода буде переходити з|із| правої частини|частини| вічка|комірки| в ліву, причому швидкість переходу води зліва направо падатиме внаслідок|внаслідок| убування різниці концентрацій | домішок |нечистот| по обидві сторони мембрани (розбавлення розчину в
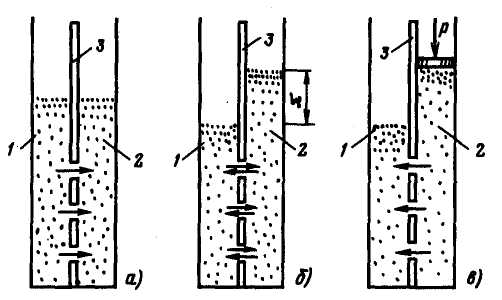
Рис. 4.1. Принципова схема прямого і зворотного осмосу:
а – початок осмотичного перенесення; б – рівноважний стан; в – зворотній осмос; 1 – прісна вода; 2 – солона вода; 3 – мембрана
правій частині|частині| вічка|комірки|), а швидкість переходу води справа наліво зростатиме через збільшення різниці рівнів по обидві сторони мембрани. Природно, що при певному гідростатичному тиску|тисненні| настане|наступить| рівновага такої системи, коли рівні в обох частинах|частинах| вічка|комірки| не змінюватимуться. Гідростатичний тиск|тиснення|, відповідний рівноважному стану|достатку| такої системи, називається осмотичним тиском|тисненням|.
Якщо з боку розчину прикласти зовнішній тиск|тиснення|, що перевищує осмотичний, то швидкість переходу через мембрану| води з|із| розчину буде більшою, ніж води в розчин. Таким чином, рушійна сила процесу зворотного осмосу з урахуванням того, що мембрани зазвичай|звично| пропускають деяку кількість іонів разом з водою і фільтрат представляє собою розчин, але|та| значно менш концентрований, ніж початковий, буде рівна
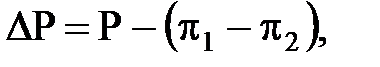
| (4.1) |
де Р – надлишковий тиск над початковим розчином;
π1 і π2 – осмотичний тиск відповідно початкового розчину і розчину, що пройшов через мембрану.
Осмотичний тиск|тиснення| розчину в загальному|загальному| випадку визначається згідно|згідно з| рівнянню Вант-Гоффа
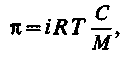
| (4.2) |
де i = 1 – a – коефіцієнт Вант-Гоффа (а – ступінь дисоціації розчиненої речовини);
R – універсальна газова постійна, рівна 8,3143 Дж/(моль·К);
Т – абсолютна температура розчину, К;
С – концентрація розчиненої речовини, кг/м3;
М – маса 1 моля розчиненої речовини, кг.
Емпіричний коефіцієнт Вант-Гоффа дорівнює середньому сумарному числу часток|частинок|, що утворюються при електролітичній дисоціації однієї молекули:
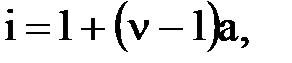
| (4.3) |
де ν – загальна кількість іонів, що утворюються при дисоціації однієї молекули.
У розведених|розлучених| розчинах або сильнорозчинних| речовинах можна вважати дисоціацію за повну|цілковиту|, і тоді коефіцієнт Вант-Гоффа можна брати як цілу величину залежно від числа іонів, що утворюються при дисоціації молекули речовини (наприклад, для NaCl| = 2).
З (4.2) видно, що осмотичний тиск залежить від хімічної природи розчиненої речовини і його концентрації. Наприклад, для розчину NaCl концентрацією 35 кг/м3 (приблизно рівної солевмісту океанської води) при Т =293 К осмотичний тиск
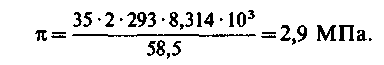
При розділенні|поділі| води і розчинених в ній домішок|нечистот| потрібні витрати|затрати| енергії не менш певної мінімальної| її кількості, рівної необхідному (згідно термодинамічному| розрахунку) для оберненого відділення|відокремлення| води. Мінімальна енергія, потрібна для оберненого перенесення|переносу| 1 моля води через мембрану, наприклад, при розділенні|поділі| морської води, оцінюється 45,2 Дж/моль, або 0,58 кВт|··год./моль. Це значення отримано термодинамічним розрахунком, і тому воно справедливе для будь-яких процесів розділення|поділу| морської води. Проте|однак| при витраті|затраті| мінімального значення вільної енергії швидкість розділення|поділу| розчину практично дорівнює нулю. Оскільки в реальних процесах продуктивність установок має бути технологічно прийнятною|допустимою|, то і робочий тиск|тиснення| в них повинен значно перевершувати осмотичний. Звичайний|звичний| робочий тиск|тиснення| підтримується в інтервалі| 5 – 8 МПа.
У розчинах, що містять|утримують| високомолекулярні речовини з|із| максимальним діаметром часток|частинок| 0,5 мкм| (або молекулярною масою не більше 500), осмотичний тиск|тиснення| малий. Для їх розділення|поділу| застосовують процес ультрафільтрації| на спеціальних мембранах, що пропускають лише воду, іони і молекули низькомолекулярних з'єднань|сполук|. В цьому випадку робочий тиск|тиснення| в апараті не перевищує 0,5 МПа.
Зворотний осмос і ультрафільтрація| принципово відрізняються від процесів фільтрування, оскільки|тому що| при їх здійсненні утворюється не осад, як при фільтруванні, а лише два розчини з|із| різними концентраціями домішок|нечистот|. Утворення ж осаду на мембранах неприпустимо|недопустимий|, щоб уникнути їх засмічення і зниження ефективності роботи.
Не дивлячись на|незважаючи на| простоту процесу зворотного осмосу і ультрафільтрації||видається|, до теперішнього часу немає єдиного погляду на механізм переходу води через мембрани. Існує декілька гіпотез, що пояснюють|тлумачать| процес відділення|відокремлення| води від солей|соль| при фільтруванні води через мембрану: гіперфільтрація (ситова), сорбційна|, дифузійна, електростатична та ін. Серед них найбільше застосування мають дві перші гіпотези.
Згідно сорбційної моделі механізм переходу води через мембрану полягає в адсорбції на поверхні мембрани і в її порах молекул води. В результаті цього на поверхні мембрани утворюється шар прісної води (завтовшки l). Вважається, що вода в цьому шарі володіє аномальними властивостями: майже повною втратою розчинювальної здатності, зниженою рухливістю і т.п. При діаметрі пір мембрани d < 2l черезних буде проходити тільки вода, а розчинені речовини затримуватимуться.
Ця модель добре описує процес розділення|поділу| води і розчинених домішок|нечистот| при фільтруванні розчинів через мембрани з|із| гідрофільних речовин, зокрема через ацетилцелюлозні| мембрани.
Більшість радянських дослідників дотримуються гіперфільтраційної гіпотези, згідно якої в напівпроникній мембрані є пори з діаметром, достатнім, щоб пропускати молекули води ( 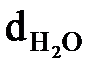 = 0,276 нм), але малим для проходження гідратованих іонів (d > 0,4 нм) і молекул розчинених речовин. Проте в реальних мембранах неможливо практично створити пори однакового розміру, і тому завжди є крупніші пори, через які можуть проходити окрім молекул води також і гідратовані іони, що і пояснює явище селективності. Окрім наявності в мембрані пір певних розмірів при розгляді гіперфільтраційної моделі враховується також, що молекули (частки) в рідині коливаються (кожна) біля тимчасових положень рівноваги, тобто переходять з одного тимчасового положення рівноваги в інше. Таким чином, якщо мембрана розділяє чисту воду і розчин, то в якийсь момент часу розчинена у воді частка може перекрити повністю пору в мембрані для проходу води, але в інший момент часу частка стрибком відкриє пору для молекули води.
= 0,276 нм), але малим для проходження гідратованих іонів (d > 0,4 нм) і молекул розчинених речовин. Проте в реальних мембранах неможливо практично створити пори однакового розміру, і тому завжди є крупніші пори, через які можуть проходити окрім молекул води також і гідратовані іони, що і пояснює явище селективності. Окрім наявності в мембрані пір певних розмірів при розгляді гіперфільтраційної моделі враховується також, що молекули (частки) в рідині коливаються (кожна) біля тимчасових положень рівноваги, тобто переходять з одного тимчасового положення рівноваги в інше. Таким чином, якщо мембрана розділяє чисту воду і розчин, то в якийсь момент часу розчинена у воді частка може перекрити повністю пору в мембрані для проходу води, але в інший момент часу частка стрибком відкриє пору для молекули води.
Ефективність процесів зворотного осмосу і ультрафільтрації| значною мірою визначається властивостями мембран, що застосовуються, які повинні відповідати наступним|слідуючим| вимогам|: вони повинні володіти високою розділяючою здатністю (селективністю), високою питомою проникністю, стійкістю до дії середовища|середовища|, незмінністю характеристик в процесі експлуатації, достатньої механічною міцністю|, мати низьку вартість.
Експериментально показано, що при осмотичному перенесенні|переносі| води через мембрану швидкість цього перенесення|переносу| підкоряється рівнянню
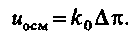
| (4.4) |
Коефіцієнт ko у випадку розбавлених розчинів визначається так:
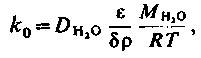
| (4.5) |
де 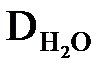 – коефіцієнт дифузії води через пори, м2/с;
– коефіцієнт дифузії води через пори, м2/с;
ε – пористість| мембрани, долі;
δ – товщина мембрани, м;
ρ – щільність води, кг/м3;
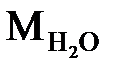 – маса 1 моля води, кг.
– маса 1 моля води, кг.
Технологія виготовлення зворотноосмотичних мембран така, що діаметри пір в них лежать в інтервалі 0 < dп < 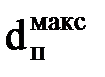 . При додаванні зовнішнього тиску з боку розчину швидкість перенесення води через пори розміром, рівним
. При додаванні зовнішнього тиску з боку розчину швидкість перенесення води через пори розміром, рівним 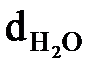 , буде рівна
, буде рівна
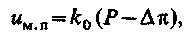
| (4.6) |
де Δπ викликає|спричиняє| протидію перенесенню|переносу| води і розчину у фільтрат.
Швидкість перенесення води через крупні пори (dп > 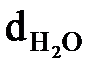 ) визначається відповідно до закону Пуазейля як
) визначається відповідно до закону Пуазейля як
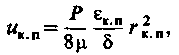
| (4.7) |
де Р – зовнішній тиск. Па;
μ – динамічна в'язкість води, Па·с;
εк.п – доля крупних пір;
rк.п – радіус крупної пори, м.
Тоді швидкість фільтрування розчину через мембрану
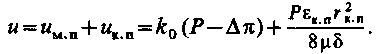
| (4.8) |
Питома продуктивність мембран, м3/(м2·с), пов'язана зі швидкістю фільтрування формулою q = 86,2·103u.
На практиці користуються поняттям «проникність мембрани», яка виражається кількістю фільтрату V, що одержується з одиниці поверхні мембрани F в одиницю часу τ:
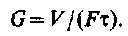
| (4.9) |
Проникність залежить від складу розчину, зовнішнього тиску і типу мембрани.
При експлуатації під впливом високого тиску води і засмічення мембран їх проникність знижується. Кращі свіжі мембрани мають проникність при тиску 5 МПа більше 15м3/(м2·с). Оскільки вартість мембран складає близько 20% вартості очищення води в процесі зворотного осмосу, питання про тривалість їх роботи є украй важливим. В наш час деякі типи мембран успішно експлуатуються 2 – 3 роки.
Селективність мембран в процесі розділення визначається виразом
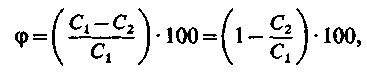
| (4.10) |
де С1і С2 – концентрація розчиненої речовини відповідно в початковій воді і фільтраті.
Відповідно до (4.8) селективність мембран можна інтерпретувати як
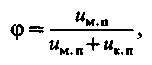
| (4.11) |
тобто селективність зростає із|із| збільшенням частини|долі| дрібних|мілких| пір в мембрані.
Селективність розділення залежить як від властивостей мембрани, так і від властивостей речовин, що розділяються, зокрема від діаметрів іонів в гідратованому стані. Вона збільшується із зростанням цих діаметрів. Встановлено також, що селективність мембрани покращується із збільшенням заряду іонів. Таким чином, утримання іонів мембранами може бути представлене рядами селективності (як при іонному обміні): для катіонів Ca2+ > Mg2+ >Na+, а для аніонів 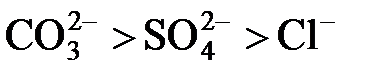 . Зазвичай селективність мембрани визначається по розчину NaCl, і її величина входить в марку мембрани (наприклад, МГА-80 – мембрана гіперфільтраційна, ацетатна з селективністю по NaCl не менше 80%). Селективність деяких типів мембран досягає 95 – 99%.
. Зазвичай селективність мембрани визначається по розчину NaCl, і її величина входить в марку мембрани (наприклад, МГА-80 – мембрана гіперфільтраційна, ацетатна з селективністю по NaCl не менше 80%). Селективність деяких типів мембран досягає 95 – 99%.
При русі розчину над мембраною відбувається безперервний відтік води через неї і концентрація домішок в потоці зростає. При цьому максимальна концентрація спостерігається біля поверхні мембрани. Підвищення концентрації солей біля поверхні мембрани (концентраційна поляризація) приводить до збільшення осмотичного тиску і можливості утворення осаду на мембрані. Строго кажучи, величина С1повинна відповідати концентрації речовини в примембранному шарі Сп.ш. Проте визначити її важко, і тому за Сп.ш приймають середню концентрацію речовини в концентраті Ск. У загальному вигляді таке явище можна відобразити, ввівши функцію Г = Сп.ш/Ск. Досягши насичення розчину в примембранному шарі максимальна швидкість протікання води через мембрану буде
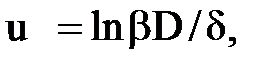
| (4.12) |
де D – коефіцієнт дифузії іонів від поверхні в глиб розчину;
δ – товщина прикордонного шару;
β = Снас/Сп.ш;
Сп.ш – концентрація іонів на кордоні прикордонного шару;
Снас – концентрація насичення.
Найбільшого поширення|розповсюдження| набули в нащ час|нині| пористі синтетичні полімерні мембрани, які отримуються введенням|вступом| в полімер добавок з|із| подальшою|наступною| операцією вимивання або видаленням|віддаленням| розчинників з|із| розчинів полімерів в умовах, що перешкоджають усадці каркасної| структури полімеру. Найбільш поширені анізотропні| ацетилцелюлозні| мембрани, що отримуються|одержують| коагуляційним методом. Хороші|добрі| властивості таких мембран пояснюються|тлумачать| високою здатністю ацетату целюлози до плівкоутворення, високою проникністю для води і низькою для більшості водорозчинних з'єднань|сполук|.
Технологія отримання|здобуття| таких мембран полягає в наступному|слідуючому|. Розчин, що містить|утримує| ацетат целюлози, розчинник (зазвичай|звично| ацетон), порообразователь| і воду, розливають тонким шаром на скляному листі|аркуші|, підсушують і потім|і тоді| занурюють в холодну| воду (0 – 25°|СС|із|С) для відмивання розчинника і відділення|відокремлення| мембрани від листа|аркуша|. Після|потім| цих операцій проводиться|виробляє| термообробка в гарячій воді (86 – 92°|С|із|С) для фіксації властивостей мембрани. Склад початкового|вихідного| розчину може бути вельми|дуже| різним. Зазвичай|звично| він містить|утримує| 17 – 22% ацетату целюлози, 66 – 69% ацетону, 1 –1,5% перхлорату| магнію (порообразователя|) і 12% води. Час підсушування складає 5 – 6 хв., час перебування в холодній| ванні при 0 – 2°|С – близько 1 год. і потім|і тоді| проводиться|виробляє| термообробка| протягом 5 – 10 хв. Отримані таким чином мембрани мають анізотропну структуру.
Анізотропна мембрана (рис. 4.2) складається з двох шарів: верхнього (активного) завтовшки до 0,25 мкм|, що представляє|уявляє| власне розділюючу| частину|частину| мембрани, і нижнього | грубозернистого |крупнозернистого| (100 – 200 мкм|) який є
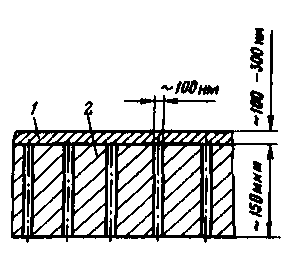
Рис. 4.2. Будова|споруда| анізотропної мембрани:
1 – активний шар; 2 – підтримуючий шар
|з'являється|підкладкою і забезпечує механічну міцність мембрани. Ацетилцелюлозні мембрани можуть використовуватися у відносно широкому| діапазоні тиску|тиснення| (1 – 8 МПа|), але|та| у вузькому інтервалі температур (273 – 303 К) і при рН| = 3 – 8. Термін роботи цих мембран різко скорочується при застосуванні вищого тиску|тиснення|, а відхилення від вказаних значень рН| приводить|наводить| до гідролізу ацетилцелюлози| з|із| відповідною зміною властивостей мембрани.
Слід підкреслити, що збільшення селективності мембрани| неминуче призводить до зниження її проникності (таблиця. 4.1), тому на практиці доводиться створювати марки мембран з|із| високою селективністю і малою проникністю і навпаки для різних умов проведення процесу зворотного осмосу.
Таблиця 4.1. Характеристики мембран для зворотного осмосу з ацетату целюлози
| Марка мембрани | Пористість, % | Селективність по NaCl, % | Проникність при тиску 5 МПа, 10–3 м3/(м2·с) |
| МГА-80 МГА-90 МГА-100 | 75±3 75±3 75±3 | 97,5 | 0,07 0,004 0,002 |
Для ультрафільтрації| застосовуються в основному поліелектролітні| мембрани. За структурою вони аналогічні ацетилцелюлозним| мембранам, але|та| мають відносно великий діаметр пір (>150 нм|).
Останнім часом в промисловості застосовуються наступні апарати для зворотного осмосу і ультрафільтрації|: з|із| плоскими мембранами (фільтр пресового типу|типу|); з|із| трубчатими| мембранами діаметром 10 – 60 мм, які вкладаються всередині|всередині| перфорованих трубок|люльок|; із|із| спіралевидними (рулонними) мембранами; з|із| мембранами у вигляді порожнистих волокон з|із| внутрішнім діаметром 24 – 80 мкм|. Різноманітність фільтрувальних елементів і апаратів пояснюється|тлумачить| перш за все|передусім| прагненням упакувати|пакувати| в одиницю об'єму|обсягу| апарату якомога більшу фільтруючу поверхню, щоб|аби| понизити|знизити| його габарити|, а також бажанням врахувати експлуатаційні можливості для проведення процесу зворотного осмосу.
Фільтр-пресовий апарат простий конструктивно, але незручний в збірці і має малу фільтруючу поверхню в одиниці об'єму. Цей апарат може працювати на воді, що містить значну кількість механічних домішок. Рулонний апарат компактний, зручний в збірці, але вимагає попереднього відділення з води механічних домішок. Найбільш ретельна підготовка води потрібна для апарату з порожнистими волокнами, але при цьому конструкція апарату проста, оскільки волокна самі витримують необхідний тиск. При плоских мембранах можна досягти щільності упаковки, рівної 700 м2/м3 об'єму апарату, і отримати питому продуктивність по воді, рівну 350 – 700 м3/м3 об'єму апарату. Використання порожнистих волокон дозволяє отримати щільність упаковки 35 000 м2/м3 об'єму апарату, але проникність порожнистих волокон на порядок нижче такої для плоских мембран, і тому питома продуктивність таких апаратів поки невелика (175 м3/м3 об'єму апарату).
У фільтр-пресовому| апараті мембрани разом з дренажними|, пристроями|устроями| набираються в пакети, які стискуються|стискають| потім між опорними пластинами. На рис. 4.3 представлена|уявляти| одна з модифікацій такого апарату. Початкова|вихідна| вода послідовно протікає уздовж|вздовж| поверхні мембран, частково фільтрується через них і у вигляді розсолу покидає апарат. Фільтрат виводиться з боку низького тиску|тиснення| з кожної мембрани.
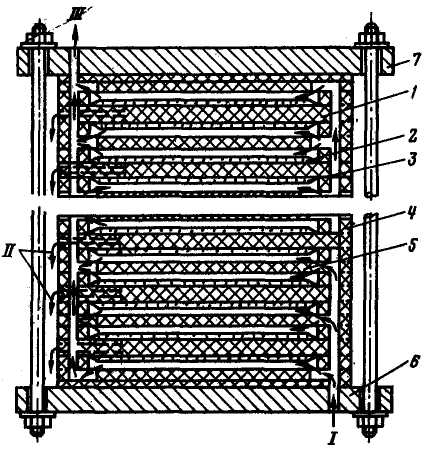
Рис. 4.3. Фільтр-прессовий зворотноосмотичний апарат конструкції ВНИИВодгео:
1 – опорна пориста пластина; 2 – мембрани; 3 – дренаж; 4 – рамка; 5 – пластина, що направляє; 6, 7 – фланцы; І – початкова вода; ІІ – фільтрат; III – конденсат
У апараті рулонного типу (рис. 4.4) мембрани розміщуються по межам шарів поропластов (рис. 4.5), один з яких 5 призначений для підведення початкової води до мембрани, а інший 4 – для відведення фільтрату. Кожен такий рулон утворює рулонний фільтруючий елемент (РФЕ). Такі РФЕ
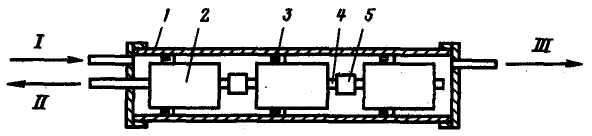
Рис. 4.4. Зворотноосмотичний апарат рулонного типу:
1 – корпус; 2 – рулонний фільтруючий елемент; 3 – уплотняющее кільце; 4 – водовідвідна трубка; 5 – муфта; І – початкова вода; ІІ – фільтрат; III – концентрат
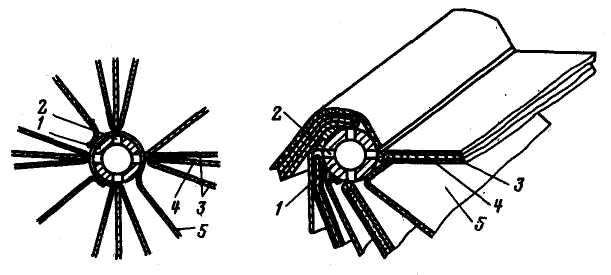
Рис. 4.5. Рулонний фільтрувальний елемент:
1 – водовідвідна трубка; 2 – щілина; 3 – мембрани; 4 – дренажний пристрій; 5 – турбулизатор-разделитель
розташовуються в кожусі, по осі якого встановлена|установлена| перфорована| трубка|люлька| для відведення води, і утворюють модуль. З|із| таких модулів можна зібрати|повизбирувати| апарат заданої продуктивності|. Початкова|вихідна| вода під тиском|тисненням| подається через розподільний пристрій|устрій| в кожусі до розділюючих шарів поропласту, проходить через мембрану і стікає| по внутрішньому шару поропласту (дренажу) до перфорованої| трубки|люльки|. Для того, щоб розчин не міг проникнути у фільтрат, кінці кожних двох мембран з|із| ув'язненим між ними дренажним пристроєм|устроєм| склеюють спеціальним клеєм.
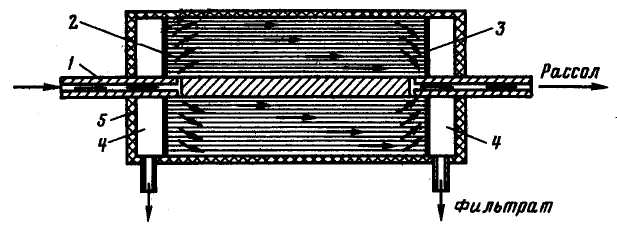
Рис. 4.6. Схема апарату ВИТАК:
1 – підведення початкової води; 2 – волокна; 3 – перегородка, в яку закладені кінці волокон; 4 – камери фільтрату; 5 – корпус
На рис. 4.6 представлена схема апарату ВИТАК з порожнистими волокнами, розробленого ВНИИВодгео. Початкова вода потрапляє в апарат через розподільну трубку, яка в середній частині перекрита, і подається до зовнішньої поверхні волокон, кінці яких закладені клеєм в трубних дошках. Частина початкової води фільтрується всередину волокон, через їх відкриті кінці потрапляє в камери фільтрату і відводиться з апарату. Концентрована частина початкової води (розсіл) також відводиться з апарату через праву частину розподільної трубки. Порожнисті волокна збирають також в окремі модулі. Так, модуль фірми «Дюпон» (США) (рис. 4.7) складається з корпусу
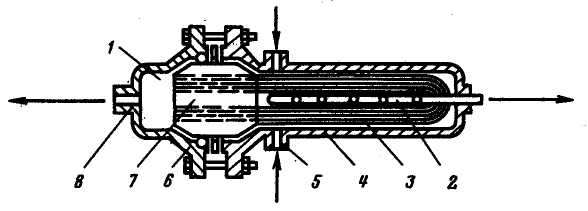
Рис. 4.7. Модуль з|із| U-образним| укладанням полого волокна:
1 – збірна камера; 2 – перфорована трубка; 3 – пучок порожнистих волокон; 4 – корпус; 5 – патрубок; 6 – фланець; 7 – кінцевий блок; 8 – патрубок
з розташованим в ньому пучком волокон, укладених U-образно. Кінці волокон відкриті, фільтрат потрапляє в збірну камеру і відводиться з модуля. Розсіл відводиться через перфоровану трубу. Один такий модуль діаметром 0,35 і довжиною 1 м містить до 9 · 105 волокон із загальною поверхнею фільтрування 1710 м2. Продуктивність такого модуля по знесоленій воді складає близько 0,1 кг/с, або 360 кг/год. Модулі збираються в один апарат необхідної продуктивності, при цьому на 1 м3 об'єму апарату досягається продуктивність, рівна 7,5 м3/год.
Продуктивність апаратів зворотного осмосу приймається по фільтрату з врахуванням|з урахуванням| селективності мембрани.
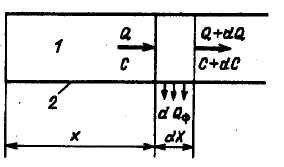
Рис. 4.8. Розрахункова схема концентрації розчину:
1 – напірний канал; 2 – мембрана
Представимо елементарний акт процесу зворотного осмосу на ділянці dx (рис. 4.8). Тоді рівняння балансу на цій ділянці можна записати як ???????
До останнього часом застосування прямотічних| систем| не викликало|спричиняло| особливих утруднень|, але|та| зростання|зріст| потужностей ТЕС і обмеженість дебіту води привели до того, що можливості|спроможності| їх застосування в наш час|нині| практично| вичерпані. Тому частина|доля| оборотних систем в подальшому зростатиме.
При оборотній системі охолоджування вода проходить через конденсатор багато разів. Охолоджування нагрітої води, що покидає конденсатор, здійснюється за рахунок її часткового випаровування. Для охолоджування можуть бути використані природні і штучні водосховища, ставки-охолоджувачі, басейни, що бризкають, і градирні. Економічно вигідніші природні водосховища, проте вони володіють тим недоліком, що у багатьох випадках в них не вдається створити нормальний тепловий режим.
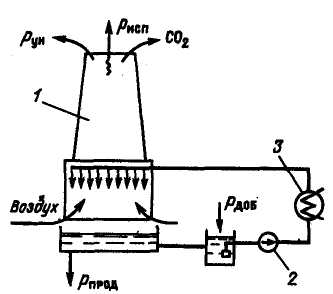
Рис. 5.1. Принципова схема оборотного охолоджування з градирнею:
1 – градирня; 2 – циркуляційний насос; 3 – конденсатор; рвип – втрата води на випаровування; рун – втрата води з віднесенням; рдоб – добавок свіжої води; рпрод – продувка оборотної води
Системи охолоджування з|із| градирнями| (рис. 5.1) найменш економічні, оскільки|тому що| вони мають температуру охолоджуючої води на вході в конденсатор у 1,4 – 1,5 раз вище, ніж в оборотних системах з|із| водосховищами. Проте|однак| при використанні градирень| можна різко понизити|знизити| скидання|скид| теплих вод у водоймища. Ці схеми єдино прийнятні в умовах обмеженого дебіту води.
Для запобігання утворенню мінеральних відкладень в конденсаторах в оборотних системах охолоджування застосовують продування системи, обробку води реагентами, обробку води в магнітному і акустичному полях. Для запобігання утворенню біологічних відкладень в обох видах охолоджуючих систем застосовують обробку води сильними окислювачами|.
У оборотній системі охолоджування внаслідок упарювання деякої частини води відбувається підвищення її солевмісту. Крім того, процес охолоджування води в градирнях супроводжується десорбцією СО2, що приводить до підвищення рН, часткової дисоціації іонів HCO3– і збагаченню води іонами СО32–. При відповідній концентрації іонів Са2+ в охолоджуючій воді створюються умови для утворення відкладень по тракту охолоджуючої води у формі СаСО3, тобто вода стає нестабільною за змістом карбонату кальцію. Для утворення СаСО3 необхідне деяке пересичення розчину. Проте в процесі утворення твердої фази СаСО3 надають інгібіруючу дію присутні у воді органічні речовини. Тому умови осадження СаСО3 в охолоджуючих системах у кожному конкретному випадку визначають експериментально. Зі сказаного вище виходить, що основним заходом для запобігання утворенню відкладення СаСО3 є стабілізація води.
Дата добавления: 2015-05-19; просмотров: 1237;
