Строение эритроцитов
Эритроциты у человека и млекопитающих в токе крови обычно (80%) имеют форму двояковогнутых дисков и называются дискоцитами. Такая форма эритроцитов создаёт наибольшую площадь поверхности по отношению к объёму, что обеспечивает максимальный газообмен, а также обеспечивает большую пластичность при прохождении эритроцитами мелких капилляров.
Диаметр эритроцитов у человека колеблется от 7,1 до 7,9 мкм, толщина эритроцитов в краевой зоне - 1,9 - 2,5 мкм, в центре - 1 мкм. В нормальной крови указанные размеры имеют 75% всех эритроцитов - нормоциты; большие размеры (свыше 8,0 мкм) - 12,5 % - макроциты. У остальных эритроцитов диаметр может быть 6 мкм и меньше - микроциты.
Поверхность отдельного эритроцита у человека приблизительно равна 125 мкм2, а объём (MCV) – 75-96 мкм3.
Эритроциты человека и млекопитающих представляют собой безъядерные клетки, утратившие в процессе фило- и онтогенеза ядро и большинство органелл, они имеют только цитоплазму и плазмолемму (клеточную мембрану), толщиной около 20 нм.
Химический состав эритроцитов
Плазмолемма эритроцитов
Плазмолемма эритроцитов состоит из примерно равного количества липидов и белков, а также небольшого количества углеводов.
Липиды. Бислой плазмолеммы образован глицерофосфолипидами, сфингофосфолипидами, гликолипидами и холестерином. Внешний слой содержит много фосфатидилхолина, сфингомиелина и около 5% (от общего количества липидов) гликолипидов, внутренний - много фосфатидилсерина и фосфатидилэтаноламина.
Белки. В плазмолемме эритроцита идентифицировано 15 главных белков с молекулярной массой 15-250 кДа. Большинство этих белков (спектрин, гликофорин, белок полосы 3, белок полосы 4.1, актин, анкирин) образуют с цитоплазматической стороны плазмалеммы цитоскелет, который придает эритроциту двояковогнутую форму и высокую механическую прочность.
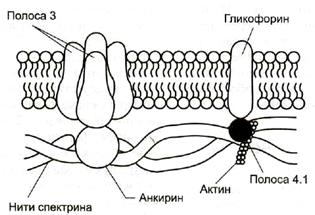
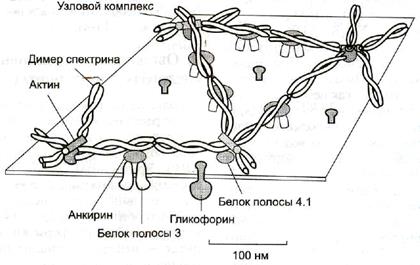
Самыми распространенными белками плазмолеммы (более 60% всех мембранных белков) являютсяспектрин, гликофорин и белок полосы 3.
Спектрин - основной белок цитоскелета эритроцитов (составляет 25% массы всех мембранных и примембранных белков), имеет вид фибриллы 100 нм, состоящей из двух антипаралельно перекрученных друг с другом цепей α-спектрина (240 кДа) и β-спектрина (220 кДа). Молекулы спектрина образуют сеть, которая фиксируется на цитоплазматической стороне плазмалеммы с помощью анкирина и белка полосы 3 или актина, белка полосы 4.1 и гликофорина.
Белок полосы 3 - трансмембранный гликопротеид (100 кДа), его полипептидная цепь которого много раз пересекает бислой липидов. Белок полосы 3 является компонентом цитоскелета и анионным каналом, который обеспечивает трансмембранный антипорт для ионов НСО3- и Сl-.
Гликофорин - трансмембранный гликопротеин (30 кДа), который пронизывает плазмолемму в виде одиночной спирали. С наружной поверхности эритроцита к нему присоединены 20 цепей олигосахаридов, которые несут отрицательные заряды. Гликофорины формируют цитоскелет и, через олигосахариды, выполняют рецепторные функции.
Na+,K+-АТФ-аза мембранный фермент, обеспечивает поддержание градиента концентраций Na+ и К+ по обе стороны мембраны. При снижении активности Na+K+-АТФ-азы концентрация Na+ в клетке повышается, что приводит к увеличению осмотического давления, увеличению поступления воды в эритроцит и к его гибели в результате гемолиза.
Са2+-АТФ-аза — мембранный фермент, осуществляющий выведение из эритроцитов ионов кальция и поддерживающий градиент концентрации этого иона по обе стороны мембраны.
Дата добавления: 2015-05-08; просмотров: 3203;
