Аллотропия веществ, состав, строение, свойства аллотропных модификаций.
Если какой-либо элемент может существовать в двух или нескольких твердых формах (кристаллических либо аморфных), то считается, что он проявляет аллотропию. Различные формы одного элемента называются аллотропами. Аллотропы существуют приблизительно у половины всех элементов.
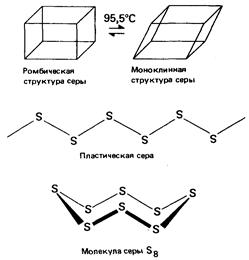
Например, углерод существует в виде алмаза либо графита. Сера существует в двух кристаллических формах - ромбической и моноклинной - в зависимости от температуры. Обе ее кристаллические формы являются примерами молекулярных кристаллов. Молекулы в них представляют собой гофрированные циклы, в каждом из которых содержится по восемь ковалентно связанных атомов серы. Твердая сера может существовать еще в третьей аллотропной форме как пластическая сера. Эта форма серы неустойчива. Она состоит из длинных цепочек атомов серы, которые при комнатной температуре разрушаются и снова образуют молекулы S8, кристаллизующиеся в ромбическую решетку.
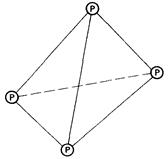
Фосфор может существовать в трех аллотропных формах. Наиболее устойчивая из них-красный фосфор. Красный фосфор имеет каркасную кристаллическую структуру, в которой каждый атом ковалентно связан с тремя другими атомами фосфора. Белый фосфор представляет собой молекулярный кристалл. Каждая его молекула содержит четыре атома фосфора, ковалентно связанных в тетраэдричес-кую структуру. Третий аллотроп - черный фосфор - образуется только при высоких давлениях. Он существует в виде макромолекулярной слоистой структуры.
Дата добавления: 2015-04-05; просмотров: 3679;
