Порядок виконання роботи. 1 Значення мас тіл, що використовуються в лабораторній роботі, їх питомі теплоємності вважаються відомими
1 Значення мас тіл, що використовуються в лабораторній роботі, їх питомі теплоємності вважаються відомими. Записати значення mт1, mт2, mт3, mт4, mт5, ст1, ст2, ст3, ст4, ст5 у табл. 3.3.1.
2 Опустити у нагрівач металеве тіло. Налийте в нагрівач води так, щоб металеве тіло було повністю покрите нею. Увімкнути нагрівач.
3 Використовуючи водомірну склянку, налити в калориметр 100 млводи. За допомогою термометра визначити початкову температуру води і калориметра Т0. Записати значення Т0 в табл. 3.3.2. Зверніть увагу, що в усіх експериментах початкова температура повинна бути однаковою. Це можна здійснити, якщо використовувати у всіх дослідах проточну воду.
Таблиця 3.3.1
| mт1 = < mт1> ± Δmт1 = |
| mт2 = < mт2> ± Δmт2 = |
| mт3 = < mт3> ± Δmт3 = |
| mт4 = < mт4> ± Δmт4 = |
| mт5 = < mт5> ± Δmт5 = |
| mт6 = < mт6> ± Δmт6 = |
| cт1 = < cт1> ± Δcт1 = |
| cт2 = < cт2> ± Δcт2 = |
| cт3 = < cт3> ± Δcт3 = |
| cт4 = < cт4> ± Δcт4 = |
| cт5 = < cт5> ± Δcт5 = |
| cт6 = < cт6> ± Δcт6 = |
Таблиця 3.3.2
| mт, кг | cт, Дж/(К·кг) | C, Дж/К | Tн, К | T0, К | Tр, К | DS,Дж/К | D(DS),Дж/К | |
4 Через 4 хвилини після того, як вода в нагрівачі закипить, вимкніть його, швидко перенесіть нагріте металеве тіло в калориметр. Закрийте калориметр кришкою. Температуру металевого тіла візьміть такою, що дорівнює температурі кипіння води, в якій розчинені солі, 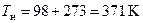 . Запишіть значення Тн у табл. 3.3.2.
. Запишіть значення Тн у табл. 3.3.2.
5 За допомогою термометра простежте за зростанням температури води в калориметрі. Запишіть у табл. 3.3.2 максимальне значення цієї температури Тр (температура рівноважного стану).
6 Вилийте воду з калориметра, остудіть його під струменем проточної води.
7 Дії пунктів 2 – 6 повторіть із кожним із шести металевих тіл.
8 Визначте теплоємність кожного із шести тіл за формулою 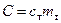 , результати розрахунків занесіть до табл. 3.3.2.
, результати розрахунків занесіть до табл. 3.3.2.
9 За формулою (3.3.9) знайдіть зміну ентропії 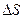 для кожного із шести тіл, результати розрахунків занести до табл. 3.3.2.
для кожного із шести тіл, результати розрахунків занести до табл. 3.3.2.
10 Обчисліть похибку зміни ентропії для шести дослідів, використовуючи формулу
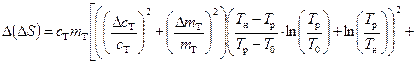
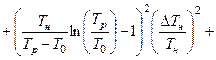
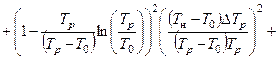
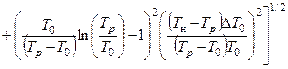 . (3.3.10)
. (3.3.10)
За похибку вимірювань температури взяти 1 градус ( 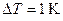 ). Результати обчислень запишіть у табл. 3.3.2.
). Результати обчислень запишіть у табл. 3.3.2.
11 Побудуйте залежність зміни ентропії від теплоємності металевого тіла ( 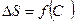 ). На графіку зобразіть похибки вимірювання зміни ентропії.
). На графіку зобразіть похибки вимірювання зміни ентропії.
12 Проведіть аналіз експериментальних результатів, зробіть висновки (чи виконується у вашому експерименті другий закон термодинаміки, як залежить зміна ентропії від теплоємності внесеного до калориметра металевого тіла).
Контрольні питання[8])
1 Будова та принцип дії теплової машини. Коефіцієнт корисної дії теплової машини.
2 Вічний двигун другого роду. Другий закон термодинаміки. Формулювання другого закону термодинаміки Томсона і Клаузіуса.
3 Оборотні й необоротні процеси. Цикл Карно. Перша і друга теореми Карно.
4 Рівність Клаузіуса. Ентропія. Закон зростання ентропії.
5 Ентропія ідеального газу.
6 Виходячи з означення ентропії, отримайте формулу для зміни ентропії ідеального газу для ізобаричного процесу.
7 Виходячи з означення ентропії, отримайте формулу для зміни ентропії ідеального газу для адіабатичного процесу.
8 Виходячи з означення ентропії, отримайте формулу для зміни ентропії ідеального газу для ізотермічного процесу.
9 Виходячи з означення ентропії, отримайте формулу для зміни ентропії ідеального газу для ізохоричного процесу.
10 Доведіть формулу (3.3.7).
11 Доведіть формулу (3.3.9).
12 Доведіть формулу для похибки зміни ентропії (3.3.10).
Дата добавления: 2015-05-05; просмотров: 789;
