Средняя доля гипофиза: меланотропин – меланоцитстимулирующий гормон (МСГ).
Существуют два типа гормонов α и β.
α-МСГ состоит из 13 аминокислот не имеет видовой спицифичности, соответствует фрагменту АКТГ.
β-МСГ имеет видовую специфичность состоит у животных из 18 аминокислот, у человека из 22 аминокислот.
Биологическое действие: стимулирует синтез меланина и образование меланоцитов, в коже, в волосах, радужке глаза, в шерсти.
Влияет на ЦНС, вызывает чувство страха.
Биохимия крови:кровь является одной из высоко специализированных тканей организма.
Функции крови:
1. дыхательная: кровь переносит кислород к тканям и углекислый газ к легким.
2. поддерживает постоянство внутренней среды организма (рН, осмотическое давление, ионный состав).
3. транспортная: питательная, экскриторная.
4. регуляторная: кровь переносит гормоны и в самой крови образуются биологическиактивные вещества (кинины, гистамин, серотонин).
5. поддержание водного баланса.
6. терморегуляторная.
7. защитная (иммуноглобулины).
8. обезвреживание (связывание токсических веществ с альбеминами, разведение концентрации токсических веществ в крови).
9. коммуникативная.
Кровь составляет 1/13 от массы тела, т.е. у взрослого человека содержится от 4-5,5л.
Кровь состоит из плазмы и форменных элементов (эритроциты, лейкоциты, тромбоциты). Клетки составоляют 45%., 83% в крови составляет вода.
Плазма крови:это жидкость после осаждения форменных элементов крови. Плазма без фибриногена называется сыворотка крови. В плазме крови содержится вода, различные электролиты (соли), питательные вещества, продукты обмена. Главную часть в плазме (85% сухого остатка) составляют белки. Их содержание в плазме в норме 65-85 г/л (6,5-8,5 %г/100 мл).
В плазме содержится более 100 белковых компонентов, которые выделяют электрофореза. При грубом делении белки плазмы крови делят на альбумины, глобулины и фибриноген.
Альбумины:содержание в норме 40-50 г/л, синтезируются в печени, молекулярная масса 67000-70000, t ½ = 7 суток.
Их функция: обеспечивают ¾ коллоидно-осмотического давления. При уменьшении одержания альбуминов в крови наблюдаются отеки.
– транспортная: альбумины имеют большое количество функциональных групп и поэтому могут переносить разные вещества (катионы – кальций, жирные кислоты, билирубин, лекарственные вещества, токсины).
– поддержание постоянства рН,
– резервная: при белковом голодании используются альбумины.
Глобулины:это гетерогенная смесь белков, содержание 20-30 г/л, молекулярная масса от 75000 и более.
При бумажном электрофорезе они делятся на фракции α1, α2, β, γ. Не растворимые в воде, растворимые в растворах солей.
Их функции: – участвуют в создании коллоидно-осмотического давления плазмы ¼.
– транспортная: более специализированные.
Fe – трансферрин ,
Сu – церулоплазмин.
Витамин В12 – транскоболамин,
ГК – транскортин,
Половые гормоны – тестостерон-эстрадиол связывающий белок.
Витамин А – ретинол связывающий белок,
Витамин Е – токоферол связывающий белок,
Витамин Д – кальциферол связывающий белок. И др…
– Поддержание постоянства рН.
– защитная: глобулины – это иммуноглобулины.
Синтезируются в печени, γ-глобулины в РЭС (ретикулоэндотелиальной системе).
Фебриноген:содержание 2-4 г/л участвуют в свертывании крови.
Безбелковые азотистые вещества:полипептиды, аминокислоты, мочевина, мочевая кислота, криатин и креатинин, пурины, перемидины.
Безазотистые вещества:к ним относятся продукты обмена углеводов и липидов: глюкоза, пируват, лактит, жирные кислоты, кетоновые тела, холестерин, триглицерины, фосфолипиды.
Плазма крови содержится минеральные вещества, соли кальция, натрия, калия, хлора, фосфора, серы, СО3-.
Белок эритроцитов (гемоглобин):хромопротеин с молекулярной массой 68000, состоит из белковой части глобина (96%) и простетической группы – гемма (4%).
Простетическая группа (гемм) представлена железом, протопорферином IX, протопорферин IX – это производное порферрина, который состоит из 4-ех пирольных колец, соединенных метиленовыми мостиками.
Протопорферин IX – это 1,3,5,8, тетраметил, 2,4, дивенил, 6,7, дипропионил-порфин.
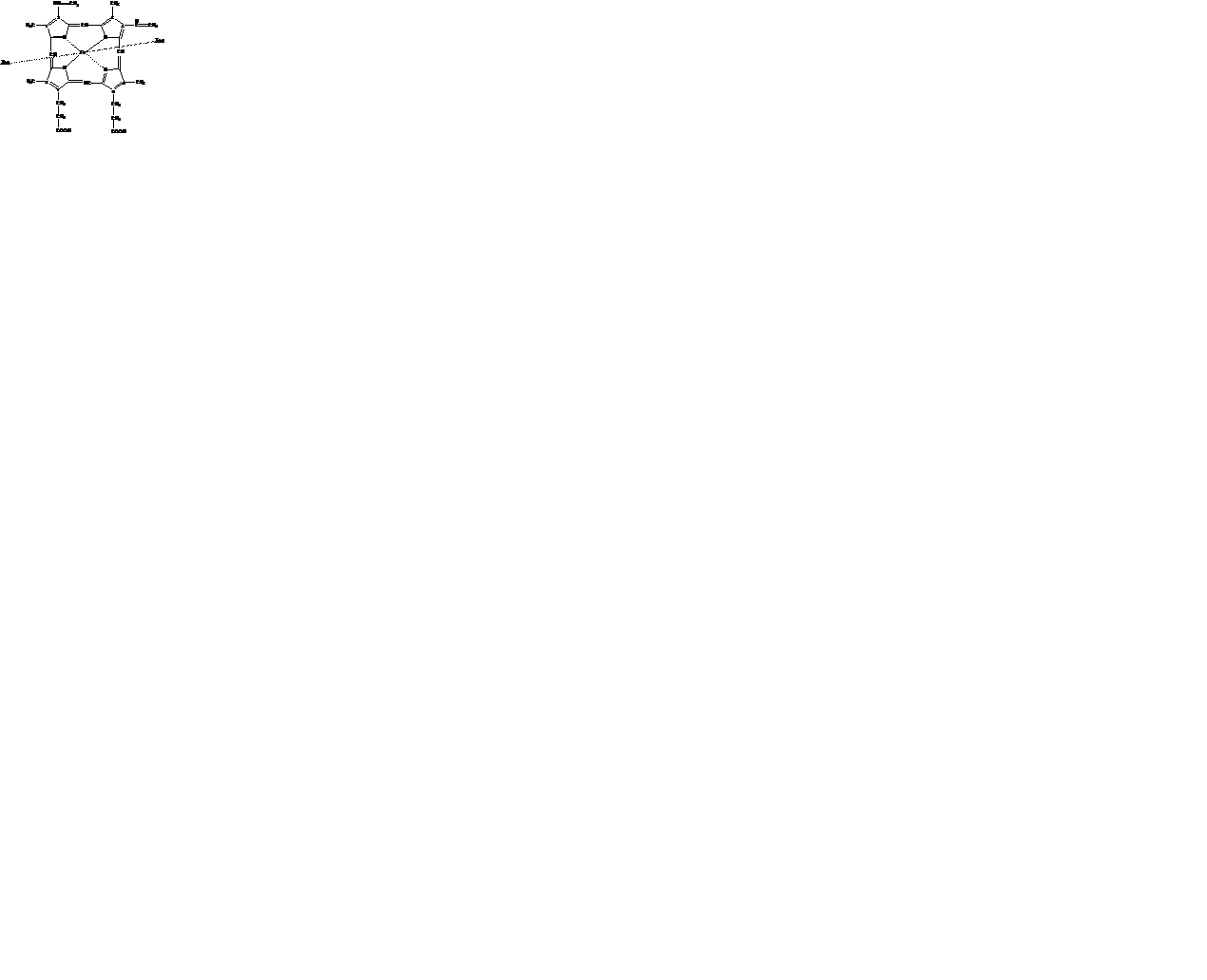
железо соединено двумя основаниями и двумя координационными связями с азотами пирольных колец. Железо, его содержание 0,335% в гемоглобине. Гемоглобин – белок четвертичной структуры, состоит из 4-ех субъединиц, с молекулярной массой = 17000, каждая субъединица состоит из гемма и полипептидной цепи. Всего в гемоглобине 574 аминокислоты. По количеству аминокислот, их последовательности цепи делят на α и β.
В молекуле гемоглобина 2 α и 2β (α – цепь содержит 141 аминокислоту, β – содержит 146, отличаются С-концевыми аминокислотами на N-конце одинакова Валин С-концевая у α – арг, у β – Гис.
Вторичная структура: в основном представлена α-спиралью. Молекула спирализована на 70-75%.
Третичная структура: представлена глобулой. Присоединение геан осуществляется 5 и 6 координационными связями железа с остатками гистидина (Гис).
4 глобулы плотно соединяются и образуют четвертичную структуру молекулы. Между одноименными субъединицами связь ионная, между разноименными субъединицами – гидрофобная.
Гемнаходится в особых гидрофобных карманах, образованных петлями полипептидных цепей. Гидрофобной частью погружен в карман, а гидрофильная наружу.
Производные гемоглобина: гемоглобин не связанный с кислородом называется дезоксигемоглобин или восстановленный гемоглобин (Fe3+), в присутствии кислорода одна из связей с гистидином разрывается и к ней присоединяется молекула кислорода, образуется оксигемоглобин (Fe2+) – это не истинное окисление, т.к. валентность железа не изменяется (это процесс называется оксигенация. Вместо кислорода к железу может присоединиться СО и такие производное называется карбоксигемоглобин (Fе2+). Но срадство гемоглобина к СО в 300 раз больше, чем к кислороду. К гемоглобину сможет присоединится СО2 и такие производное называется карбгемоглобин. Присоединение СО2 происходит не к железу, а остаткам лизина в глобине (Fе2+).
При действии сильных окислителей (К3Fe(CN)6, мителеновая синь) происходит окисление Fe2+ в Fe3+ и образуется производное метгемоглобин. Он не может присоединить кислород.
Гетерогенность гемоглобина: существует три вида:
1. эмбриональная,
2. связанная с наличием минорных компонентов.
3. генетическая.
1. эмбриональная гетерогенность:в крови эмбриона и плода имеется разный гемоглобин. В первой недели развития у эмбриона синтезируется гемоглобин Р. Приметивный, состоит из 4-ех цепей (ξξξξ эпсилон), называется говер I, когда эмбрион достигает 2,5 месяцев 2ξ цепи заменяется на α-цепи (ααξξ) говер II. В 3 месяца ξ-цепи заменяются на γ-цепи и образуется гемоглобин f – fetal – плодный (ααγγ).
γ-цепи отличаются от β-цепей 37 остаткамиаминокислот, но гемоглобин f имеет очень большое сродство к кислороду и поэтому он может забирать кислород из крови матери.
К моменту рождения у ребенка 70% составляет гемоглобин f, а 30% - гемоглобин А – adult – взрослый.
2. связанная с наличием минорных компонентов:95-96% в крови составляет гемоглобин А, кроме него имеются минорные гемоглобины (гемоглобин А2 – 2,5% (ααδδ), его роль не известна, δ-цепи отличаются 10 аминокислотами.
3. генетическая: связана с точечными мутациями в генах ДНК ответственных за синтез α, β, δ, γ цепи гемоглобина. Известно около 300 вариантов гемоглобина человека. Изменение аминокислотного состава приводит к изменению физико-химических свойств (растворимости, сродство к кислороду).
Такие гемоглобины называются анамальными и наиболее изучены из них гемоглобин S. У этого гемоглобина в β-цепях остаток глу в 6-ом положении замещен на остаток Валина. При деоксигенации такой гемоглобин выпадает в виде кристаллов в эритроцитах.
Эритроцит изменяет форму на форму серпа. Такой эритроцит застревает в капиллярах и погибает. Развивается серповидноклеточная анемия.
Гемоглобин S широко распространен у африканского населения.
Синтез гемоглобина: синтез белковой части идет в рибосомах, синтез происходит в печени, селезенке и костном мозге.
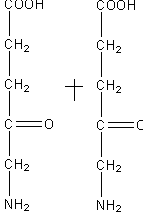
Синтез гемма осуществляется из глицина и сукцинилкофермента А в митохондриях.

δ-аминолевулиновая кислота
Две молекулы левулиновой кислоты соединяются ферментом порфобилиногенсинтаза и образуется порфобилиноген, 4 порфобилиногена образуют протопорферин.

Распад гемоглобина: продолжительность жизни эритроцитов 120 дней. Их распад происходит в печени, селезенке и красном костном мозге. При этом освобождается гемоглобин, который должен разрушаться в этих органах.
Гемоглобин
↓ оксидаза .
ведроглобин
↓ → Fe, глобин .
биливердин
↓ +2Н
билирубин (свободный непрямой) моно и ди пирролы
↓
| печень |
↓ + УДФ-глюкуронат мезобилиноген.
диглюкуронид
билирубина
(связанняй, прямой)
| Тонкий кишечник |
мезобилирубин
↓ +2Н v.porta
мезобилиноген ––––––––––––––––
(уробилиноген)
↓
| Толстый кишечник |
↓ + О2
стеркобилин → почки
↓
стеркобилиноген (моча)
1. распад начинается с разрыва метилового мостика между первым и вторым пирольными кольцами ферментом оксидазой с образованием пигмента зеленого цвета (вердоглобин).
2. от вердоглобина отщепляется железо и глобин и образуется биливердин. Железо транспортируется в депо, а глобин распадается.
3. в биливердине происходит восстановление метилового мостика между третим и четвертым пирольными кольцами и образуется билирубин. Этот билирубин называется свободным и он не растворим в воде и поэтому не дает реакцию с деазореактивом Эрлиха (реакция Ван-ден-Берга). Эта реакция идет после прибавления спирта и поэтому называется непрямая. Это билирубин адсорбируется на альбуминах плазмы крови и они доставляют его в печень.
4. в печени билирубин связывается с УДФ-глюкуроновой кислотой (после отщепления от альбумина), образуется диглюкуронид билирубина, который хорошо растворим в воде и дает прямую реакцию Ван-ден-Берга, поэтому этито билирубин называется связанный, прямой, т.к. деглюкуронидбилирубин хорошо растворим в воде он с желчью из печени поступает в тонкий кишечник.
5. здесь от билирубина отщепляется глюкуроновая кислота и происходит восстановление метилового мостика между первым и четвертым и вторым и третьим кольцами и образуется мезобилирубин.
6. в мезобилирубине происходит восстановление венильных радикалов и образуется мезобилиноген. Мезобилиноген называют иногда уробилиноген. Часть мезобилиногена по системе v/ porta всасывается из кишечника и переносится в печень, где распадается на моно и ди пирролы. Большая часть мезобилиногена поступает в толстый кишечник и восстанавливается в стеркобилиноген (двойные связи в кольцах). Основная часть стеркобилиногена выводится с содержимым кишечника, окисляется кислородом воздуха в стеркобилин. Он обуславливает окраску содержимого кишечника. Небольшая часть стеркобилдиногена всасывается и по геморроидальным венам доставляется в почки и выводится с мочой (окрашивает мочу).
Определение прямого и непрямого билирубина в крови имеет важное значение в диагностике заболеваний печени – желтуха.
Различают три вида желтух:
1. гемолитическая в следствии усиленного гемолиза эритроцитов в крови содержится большое количество непрямого билирубина. Печень усиленно его перерабатывает и с мочой выводится повышенное количество стеркобилиногена, а с калом – стеркобилин (это надпочечная желтуха).
2. паренхиматозная – инфекционный гепатит, печеночная желтуха. В печени вирусом повреждены гепатоциты и поэтому происходит соединение кровеносной системы с системой желчных капилляров. Поэтому в кровь поступают желчные пигменты и повышается содержание прямого билирубина, т.к. гепатоциты повреждены, онине успевают конъюгировать свободный билирубин с глюкуроновой кислотой ион потупает в кровь. Вмочу фильтруется растворимый в воде прямой билирубин и мезобилиноген, поэтому моча интенсивно окрашена (цвет пива). Т.к. в кишечник из печени поступает мало пигментов кал слабо окрашен или белый.
3. обтурационная: закупорка желчного протока камнем (или рак панкреас). Нарушается выведение желчи из желчного пузыря и печени. В кровь поступает прямой билирубин и не прямой билирубин, т.к. в следствии застоя желчив печени нарушается коньюгирование непрямого билирубина. Прямой билирубин фильтруется в мочу и она сильно окрашена. В укишечник не поступает пигмент – ахолия и кал белого цвета. Это подпеченочная желтуха (тоже появляется моча цвета пива).
Общего билирубина 8,55 – 20,5 мкмоль/л.
| гемолитическая | паренхиматозная | Обтурационная | |
| кровь | Увеличение непрямого билирубина | Увеличение прямого билирубина, увеличение непрямого билирубина, мезобилиноген | Увеличение прямого билирубина, увеличение не прямого билирубина |
| моча | Увеличение стеркобилиногена | Увеличение билирубина, мезобилиногена | Увеличение прямого билирубина |
| кал | Увеличение стеркобилина | Уменьшение стеркобилина, уменьшение стеркобилиногена | Ахолия, уменьшение стеркобилиногена |
Обмен железа:всего в организме взрослого человека содержится от 3-5г железа, в основном все связано с белками. эти железо содержашие белки делят на 2 группы:
1. гемосодержащий – гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза.
2. не содержащие гемма – трансферрин, ферритин, железосерные белки.
Основное количество железасодержится в гемоглобине (1,5-3г) и 1-1,5 г в ферритине. С пищей к нам поступает трех валентное железо, а всасывается двух валентное железо. В желудке в кислой среде происходит восстановление железа с помощью витамина С или SH-группы. Всасывание двухвалентного железа происходит в двенадцатиперстной кишке в клетках слизистой. Здесь имеется белок похожий на трансферрин крови. Он присоединяет два атома железа и передает трансферрину плазмы крови. Трансферрин плазмы крови синтезируется в печени.
Молекулярная масса около 86000. связывает 2 атома трехвалентного железа и и транспортирует их их к органам где железо депонируется, т.е. в печень. Селезенку и красный костный мозг.
В этих тканях трансферрин отдает железо белку ферритину. Белковая часть его называется аппоферритин. Ферритин – крупный белок с молекулярной массой 450000. состоит из протомеров, которые образуют шар. В полость шара ведут 6 каналов. По которым атомы железа проходят внутрь и откладывается там от 2500 до 45000 атомов железа. Поэтому белок и эти органы имеют ржаво-красный цвет. При передаче атомов железа с белка на белок каждый раз происходит восстановление трехвалентного железа в двухвалентное для его освобождения. Выделяется железо с содержимым кишечника (с желчью через печень приблизительно 1 мг в сутки). При распаде гемоглобина и других белков железо не выводится, а связывается с белками плазмы крови гаптоглобинами и снова депонируются в ферритине, в печени, селезенке, костном мозге. Железо поступает в организм с яблоками, печенью, гречкой, фасолью.
Смуточная потребность: 1 мг. Но чтобы он 1 мг всасался нужно поступление 13-15 мг.
Обмен меди:всего в организме взрослого человека содержится приблизительно 100 мг меди.
Суточная потребность: 2 мг содержится в печни, мясе, овощах, орехах, морских продуктах.
Обычно поступает достаточное количество меди всасывается в тонком кишечнике. Ворганизме содержится во всех органах и в основном связано с белками: гемокупренил содержится в эритроцитах, гепатокупренил содержится в печени (депонирукет медь).
Транспорт в крови осуществляется белком церрулоплазмином.
Биологическая роль:
1. активатор ферментов.
2. составная часть ферментов: цитохром оксидаза, тирозиназа, лизилоксидаза, т.е. в окислительных ферментах.
3. содержится в пигментированных волосах и коже.
Обмен цинка:в организме здорового человека содержится около 0,5 г. Содержится во всех органах, особенно много в гипофизе, панкреас, печени, мужчких половых железах, мышечной ткани.
Транспортируется глобулинами плазмы крови (с α1 связан прочно. А с β не прояно).
Суточная потребность: у взрослого 12-16 мг, у детей 4-6 мг.
Роль: является актватором ферментов и входит в состав карбоангидразы, карбоксипептидазы, глютамат ДГ, инсулин.
Выделяется через кишечник и в небольшом количестве с мочой.
Обмен воды:вода самое распростаненное соединение в организмах. Выделяют ряд важных функций благодаря ее физико-химическим свойствам: (большая теплопроводность, большая удельная теплоемкость, большая теплота испарения, большое поверхностное натяжение).
Молекула воды представляет собой диполь, у которой положительный и отрицательный заряд в пространстве разделены, поэтому между ними могут возникать водородные связи. Эти связи слабые, но их много и поэтому вода является устойчивой жидкостью. t = ½ этих связей маленький очень = 1*10-9 сек и поэтому вода подвижная жидкость. А не вязкая. На разрыв этих связей надо потратить большое количество энергии, поэтому у воды высокая температура кипения, большое поверхностное натяжение. Большая теплота испарения.
Функции воды:
1. вода растворитель кристаллических солей, органических веществ.
2. структурная: вода способствует образованию липидного бислоя мембран.
3. вода способствует созданию внутриклеточного давления и формы клеток.
4. терморегуляторная: вода поддерживает постоянную температуру тела благодаря большой удельной теплоемкости (в 4 раза больше, чем воздуха), теплота испарения воды предохраняет организм от перегревания, тюк. На испарения 1 мл воды с поверхности тела нудно 2,26 кДж. Вода имеет большую теплопроводность (в 2-4 раза больше, чем у других жидкостей)., поэтому не происходит местных перегревов тканей.
5. транспортная: благодаря большой текучести воды, поэтому в организме быстро перемешиваются разные вещества.
6. смачивающая: т.е. вода смачивает трущиеся поверхности и способствует их скольжению.
7. метаболическая: вода является средой, где происходят химические реакцтт и сама учасивует в реакциях гидролизаЮ, гидротации, дегидротации, реакциях синтеза, является конечным продуктов дыхательной цепи.
Классификация воды: всего в организме животных и человека вода составляет 65-70% от массы тела.
По локализации она делится на внутриклеточную. Внеклеточную. Внеклеточная вода делится на внутрисосудистую и интерстициальную.
Вода (65-70%
Внутриклеточная (45-50%) внеклеточная (20-25%)
внутрисосудистая (5-6%) интерстициальная жидкость
это плазма крови (15-20%)
межклеточная, лимфа,
спинномозговая жидкость,
жидкость суставов.
Кроме этого вода делится по подвижности в зависимости от способности перемещаться, на свободную и иммобилизированную (связанную). Свободная вода – это свободно перемещающаяся в организме (плазма крови, лимфа. Спинномозговая жидкость, пищеварительные соки. Моча, пот). Эта вода поддерживает гемостаз.
Иммибилизованная вода: не может свободно двигаться в организме, т.к. связана с молекулами полимеров (белки, гликонен, ДНК, РНК) или в мембранах – это гидротация.
Вода обеспечивает форму тканей (тургор).
Имеются возрастные различия в содержании воды: у детей воды больше. Это связано с гидратациооной способностью белков. 100 г белков могут связать 50 г воды. С возрастам такие способности уменьшаются и ткани сморщиваются.
Органное различие: разные ткани содержат разное количество воды:
Серое вещество мозга 84%
Почки 81%
Сердце 78%
Печень и мышцы 75%
Костная ткань 20-40%
Жировая ткань 25%
Половые различия: содержание воды у мужчина на 10 % больше, чем у женщин.
Суточная потребность: 2-2,5 л (40г на кг).
Выделение воды: ежедневно 1,5-2 л из них 0,5-1,5 л с мочой, приблизительно 0,4 л с воздухом, приблизительно 0,6 л с потом.
Поступившая в организм вода находится 9-10 суток.
Регуляция объема внеклеточной жидкости:объем внеклеточной жидкости зависит от осмотического давления и главным образом от содержание натрия хлорида в организме.
В регуляции обмена участвует:
1. вазопрессин: при повышении осмотического давления в крови более чем на 2% раздражаются осморецепторы в сосудах, импульсы с осморецепторов поступают в гипоталамус, где вырабатывается вазопрессин. Он поступает в заднюю долю гипофиза и секретируется в кровь. Мишенью для него является почечные канальцы. По аденилатциклазному механизму он вызывает фосфорелирование белков мембраны почечных канальцев и активацию гиалуронидазы. Увеличивается проницаемость мембран почечных канальцев и происходит реабсорбция воды. Объем увеличивается внеклеточной воды и снижается осмотическое давление, осморецепторы тормозятся.
2. минералькортикоиды, в основном альдостерон: секретируется в ответ на снижение концентрации натрия, хлора в крови, что вызывает снижение осмотического давления. Снижение обмена внеклеточной воды и следовательно снижение АД.
Снижение АД воспринимается клетками югстогломерулярного аппарата – это гладкомышечные клетки, которые окружают приносящую артериолу. Эти клетки являются анализаторами давления крови на стенку артериолы.
При уменьшении давления клетки ЮГА выделяют в кровь протолитический фермент ренин, который расщепляет белок ангиотензиноген (синтезируется в печени) от ангиотензиногена отщепляется с N-конца декапептид и образуется ангиотенин I. На него действует ангиотензин превращающийфермент, который с С-конца отщепляет две аминокислоты и образуется ангиотензин II – самое сильное сосудосуживающее редство в организме.
Ангиотензин II действует на гладкие мышцы сосудов. Они сокращаются, повышается АД и тормозятся клетки ЮГА.
Под действием фермента аминопептидазы с N-конца от ангиотензина II отщепляется 1 аминокислота и образуется ангиотензин III.
Ангиотензин II и IIIвырабатываются с соотношением 5:1.
Эти вещества действуют на рецепторы клубочковой зоны коры надпочечников, которая вырабатывает альдостерон. Он усиливает реабсорбцию натрия, хлора, HCO3- и способствует выведению калия и протонов, увеличивается осмотическое давление.
Ангиотензин II стимулирует также секрецию вазопрессина, который задерживает воду. Увеличивается объем внеклеточной воды. Увеличение объема и осмотического давления тормозят клетки ЮГА.
Сам альдостерон так же тормозит клетки ЮГА.
Ангиотензин II и III разрушаются ангиотензиназой до аминокислот.
3. увеличение объема внеклеточной воды (плазма крови) раздражаются клетки предсердия, которые вырабатывают атриальный натрийуретический фактор – это пептид действующий по гуанилатциклазному механизму. В почечных канальцах тормозит реабсорбцию натрия, хлора и воды. Т.е. способтвует их выведению.
Минеральный обмен:это совокупность процессов всасывания, распределения, превращения и выведения веществ, которые в организме находятся в основном в форме неорганических соединений. К минеральным веществам относятся вода, разные катионы и анионы неорганических кислот.
76 из 106 элементов найдены в живых организмах, но содержаться в разных количествах.
Na,K,Ca,P,Mg,Cl,S – содержаться в больших количествах (макроэлементы) от 3 до 1200г (10-2%) другие элементы Со, Мn,F,Br,Cu,J в меньших колочествах (от 10-2 до 10-3)и их называют микроэлементами.
Их функции:
1) структурная: построение костной ткани, образование комплексов металлов с макромолекулами.
2) Регуляция физико-химических процессов (создание осмотического давления во всех жидкостях, поддержание постоянства рН в крови и тканях).
3) Регуляция проницаемости мембран.
4) Участие в ферментативном катализе и регуляции активности ферментов.
5) Биоэлектрическая: образование разности потенциалов на клеточной мембране.
Таким образом, основное значение их кроме структурной функции заключается в регуляции физико-химических процессов.
Обмен кальция и фосфора:общее содержание кальция 1000-1200г.
Фосфора – 500-900г.
Содержание кальция в крови 2,05-2,8 ммоль/л.
Фосфора 0,8-2 ммоль/л
Суточная потребность: кальция для взрослого человека 800 мг, для детей, подростков, беременных женщин 1200мг, фосфора 1500 мг.
Источники: кальция – молочные продукты, орехи, зерна злаков, фасоль, горох, бобы, соя. Фосфора: молочные продукты, рыба.
Кальций в основном поступает в виде фосфорно-кислых солей и на всасывание кальция влияет: 1) соотношение кальция и фосфора в пище. Она болжна быть 1:2. такое соотношение есть в молоке.
2) наличие жирной пищи, т.к. кальций с жирными кислотами образует нерастворимые соли (кальциевое мыло).
Функция кальция: 1) формирование костного скелета.
2) регуляция активности ферментов.
3) участие в свертывании крови.
4) участие в мышечном сокращении.
5) регуляция проницаемости мембран.
6) посредник в действии гормонов на проницаемость в клетку.
7) стимуляция секреции экзокринных эндокринных желез.
8) Участие в контактном узнавании клеток.
Выведение кальция: через кишечник 500-800 мг, с мочой 100-300 мг.
Функция фосфора: 1) формирование костного скелета.
2) структурный компонент органических содинений ( нуклеиновыен кисолты, фосфолипиды, кофактор ферментов,
3) образование буферной системы)
4) участие в регуляции активности ферментов путем фосфорелирования – дефосфорелирования.
5) энергетическая – образование макроэргическх соединений.
Регуляция фосфорно-кальциевого обмена осуществляется 3 ферментами:
1 – паратгормон.
2 – кальцитонин.
3 – кальцитриол.
Обмен натрия и калия:общее содержание натрия в организме приблизительно 105 г, калия приблизительно 245 г.
Суточная потребность натрия 4,5-5 г, калия 2-6г.
Источники натрия – соль (8-10г).
Калия – картофель, помидоры, томатный сок, бананы, сухофрукты, лимоны.
Содержаниен атрия в крови 135-150 ммоль/л. Натрий – это катион внеклеточной жидкости, а калий внутриклеточный катион.
Депонируется натрий в коже, подкожной клетчатке, хрящах, калий в мышечной ткани.
Их функции:
1. электрическая активность клетки в результате разности концентрация натрия и калия по сторонам мембраны.
2. поддержание рН (бикарбонатно-фосфорная буфермена система).
3. создание осматического давления в клетках и внеклеток.
Обмен натрия, калия тесно связан с обменом воды, регулируется вазопрессином, альдостероном, натрийуретическим фактором.
Прри недостатке калия: отсутствие аппетита, мышечная слабость, дегенеративное изменение миокарда, нарушение функции почек.
Обмен магния:в организме человека приблизительно 25 г. Большая часть которого в костях.
Суточная потребность приблизитольно равна 700 мг (– 10 мг на кг массы тела).
Откладыватся в костной и мышечной ткани.
Его функции:
1 активатор ферментов, входит в АТФ-азу, входит в состав фосфотаз, холинэстеразы, активирует пируваткарбоксилазу, входит в состав хлорофилла. Парат гормон способствует поступлению магния в кость уменьшая его содержание в крови.
При длительном введении магния усиливается выведение кальция.
Дата добавления: 2015-04-19; просмотров: 1466;
