Диаграмма состояния для сплавов, компоненты которых неограниченно растворимы в твердом состоянии (II рода) (неограниченный твердый раствор).
Оба компонента сплава (А и В) неограниченно растворимы в жидком (L) и твердом состояниях и не образуют химических соединений. Диаграмма состояния имеет простой вид и показана на рис. 1.18,а где линия AmB – ликвидус, AnB – солидус.
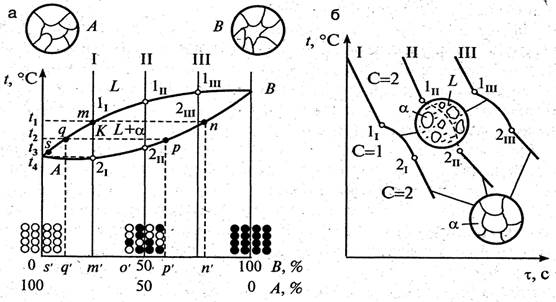
Рис.1.18 Диаграмма состояния II рода (а), кривые охлаждения сплавов I, II, III и схемы их структур (б).
Структура всех этих сплавов однофазная и состоит из зерен, которые представляют собой твердый раствор одного компонента в другом (рис.1.18,б). Из кривых охлаждения видно, что до точки 1 происходит охлаждение жидкого сплава, на участке 1-2 – кристаллизация твердого раствора, а ниже точки 2 – охлаждение уже твердого вещества.
Рассмотрим процесс затвердевания одного из сплавов этой системы. Кристаллизация сплава I начинается при температуре t1 . Из жидкой фазы состава m выделяются кристаллы твердого раствора состава n (т.е. раствора в котором концентрация В составляет n’ по оси концентраций, а концентрация А составляет 100% - n’), обогащенные компонентом В.
При дальнейшем охлаждении до температуры t2 в жидко-твердом растворе имеется (находится в равновесии) жидкий сплав с концентрация ми компонентов q (q’) и твердый раствор с концентрация ми компонентов р (p’). Т.е. при кристаллизации сплава I состав жидкой фазы непрерывно меняется по лини ms, а твердого вещества – по линии n21. В результате медленного охлаждения в равновесных условиях успевает произойти диффузионное перераспределение компонентов между жидкой и твердой фазами. Поэтому к моменту окончания процесса кристаллизации при температуре t2 все зерна твердого раствора будут иметь одинаковый состав (если бы этого не было, то тогда раствор состоял бы из зерен с концентрациями компонентов начиная от n’ до 2I – т.е. с зернами сначала богатыми компонентом В, а потом зернами богатыми компонентом А).
В соответствии с правилом отрезков в точке К количество жидкости равно соотношению Kp/qp, количество твердой фазы - qK/qp. Состав жидкости: q’ – концентрация В, %, (1- q’) – концентрация А. Состав твердой фазы: n’ - концентрация В, %, (1- n’) – концентрация А.
В реальных условиях охлаждения состав кристаллов получается неоднородным. Это происходит потому, что скорость кристаллизации больше скорости диффузии и у кристаллов, образующихся при температуре выше t4, не успевает произойти диффузионное перераспределение компонентов. Внутренние участки кристалла обогащаются тугоплавким компонентом В (т.е. тем компонентом, который лежит ближе к точке n или n’), а наружные - компонентом А (т.е. тем компонентом, который лежит ближе к точке 2I , как выше и сказано). Такая неоднородность химического состава называется внутрикристаллической, или дендритной, ликвацией. Ликвация чаще всего играет отрицательную роль, т.к. ухудшает технологические и механические свойства сплавов.
Диаграммы такого типа имеют системы Ni – Cu, Ag – Au, Mo – V, Mo – W и др.
Дата добавления: 2015-04-15; просмотров: 1836;
