Из: Hunter T. Cooperation between oncogenes. Cell, 64: 249, 1991
Регуляторный ген (р53), предотвращающий излишнюю пролиферацию клеток, служит супрессивным геном для опухолевых клеток. Характерно, что активация супрессорных генов происходит в два этапа. В ядре клетки существует по две копии любого гена. Супрессивные гены обладают так называемым "доминирующим" действием, когда для супрессии пролиферации клеток достаточно лишь одной полной копии гена. Теория супрессорных генов согласуется с теорией наследственной предрасположенности к возникновению рака. Инактивация одной из двух аллелей может быть фенотипически "немой" (т. е. не происходит развития злокачественного фенотипа), если достаточно одной (второй) аллели для сохранения незлокачественного фенотипа клеток. Но у таких людей особенно высок риск развития рака, т. к. при одной лишь мутации супрессорных генов клетки трансформируются в раковые. В таблице 10-2 приведены наиболее важные гены тканевой супрессии (TSGs).
Образование запретных клонов. Большинство генетических исследований подтверждают, что опухоль развивается из одной клетки. Принятая в настоящее время теория многоступенчатого канцерогенеза гласит, что эпителий желудочно-кишечного тракта подвергается воздействию вредных факторов окружающей среды. Вследствие этого происходит постепенное повреждение ДНК с накоплением генетических мутаций. При этом мутации обычно возникают в участках ДНК, ответственных за выживаемость и рост клетки. Многие из них способны ингибировать процессы, необходимые для жизнедеятельности клетки, и тем самым привести ее к гибели. Некоторые мутации могут усиливать рост и выживаемость мутированных клеток, позволяя им размножаться быстрее, чем окружающие их клетки. В конце концов мутированные клетки начинают составлять большую часть органа или ткани. Часть мутированных клеток теряет способность исправлять повреждения ДНК, и, следовательно, из поколения в поколение происходит накопление мутаций. Этот пул клеток также подвержен дополнительным мутациям.
Периодически отдельные клетки мутантного клона подвергаются дополнительной мутации, повышающей их выживаемость и способность к росту. Такие клетки постепенно вытесняют из популяции родительские клетки. Увеличение клона мутированных клеток обычно происходит при появлении новых мутаций, которые увеличивают выживаемость клетки. При наблюдении за развитием опухоли на ранней стадии в клетках выявляется определенное количество мутаций, число которых возрастает с течением времени. На Рис. 10-1 показана прогрессия опухоли на фоне появления клонов с новыми характеристиками.
Таблица 10-2. примеры генов, подавляющих рост опухоли У человека
| Соматические мутации | Врожденные мутации | ||||||
| Ген-супрессор опухоли | Локус хромосомы | Локализация/ предположительная функция | Основные типы | Примеры опухолей | Синдром | Количество гетерозигот на 105новорожденных | Типичные опухоли |
| р53 | 17р13.1 | Ядро/фактор транскрипции | Отсутствует | Большинство типов рака у человека | Синдром Ли-Фраумени | ~2 | Карциномы груди, коры надпочечников, саркомы, лейкемия, опухоли мозга |
| RB1 | 13q14 | Ядро/модификатор транскрипции | Делеция и незначимая мутация | Ретинобластома, остеосаркома, карцинома молочной железы, простаты, мочевого пузыря, легкого | Ретинобластома | ~2 | Ретинобластома, остеосаркома |
| АРС | 5q21 | Цитоплазма/ неизвестно | Делеция и незначимая мутация | Карцинома толстой кишки, желудка, поджелудочной железы | Наследственный аденоматозный полипоз толстой кишки | -10 | Карциномы толстой кишки, щитовидной железы, желудка |
| WT1 | 11р13 | Ядро/фактор | Отсутствует | Опухоль Вильмса | Опухоль Вильмса | -0.5-1 | Опухоль Вильмса |
| NF1 | 17q11 | транскрипцииЦитоплазма/ГТФ активирующий | Делеция | Шванномы | Нейрофиброматоз (тип 1) | -30 | Нейрональные опухоли |
| NF2 | 22q | факторЦитоплазма/ мембранные свя | Делеция и незначимая мутация | Шванномы и менингиомы | Нейрофиброматоз (тип 2) | -3 | Центральные шванномы и менингиомы |
| VHL | Зр25 | зи цитоскелета Неизвестно | Делеция | Неизвестно | Болезнь ван Хип-пель-Ландау | -3 | Гемангиобластома, почечно-клеточная карцинома |
Многоступенчатый канцерогенез. Концепция генетической основы развития рака толстой кишки была разработана Vogelstein с соавторами. Согласно этой концепции процесс протекает медленно, и в него вовлечено множество генов.
Количество генетических повреждений опухолей постепенно увеличивается по мере роста. Часть повреждений появляется только на ранних стадиях, часть — только на поздних. Еще до конца не ясна последовательность появления опреде-
Рис. 10-1. Опухолевый рост. На данной схеме представлена типичная последовательность канцерогенеза. На первой стадии показано действие канцерогена. После накопления критической массы мутировапных генов (единой точки зрения на их количество и локализацию нет) клетка превращается в опухолевую. На второй стадии происходит разрастание клона мутировавших клеток с формированием доброкачественной опухоли. Без каких-либо дополнительных воздействий доброкачественная опухоль способна сохранять свою доброкачественность. Но при дополнительном воздействии она трансформируется в злокачественную и приобретает способность к инвазивному росту и метастазированию (стадия 3). Не существует единой точки зрения на природу этого воздействия. Злокачественная опухоль склонна к инвазивному росту с повреждением органов хозяина. Генотип злокачественных клеток очень нестабилен, поэтому их клон оказывается гетерогенным (стадии 4 и 5). Клинически такая гетерогенность приводит к формированию отдаленных метастазов. (Но: Yamada Т., Alpers D. H., Owyang С., Роwell D. W., Silverstein F. E., cds. Textbook of Gastroenterology, 2nded. Philadelphia: J. B. Lippincott, 1995:586.)
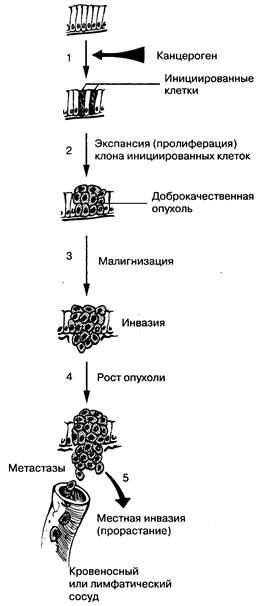
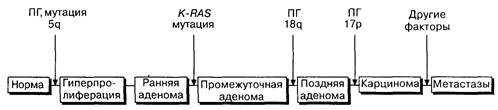
Рис.10-2. Схема последовательных генетических изменений в многоступенчатом канцерогенезе при раке толстой кишки с дополнениями по Fearon, Vogelstcin. Сверху над схемой показаны мутации, ведущие к потере гетерозиготности (П1), лежащие в основе развития колоректального рака
ленных повреждений в опухолевых клетках, но уже выяснено, что при различных типах рака возможны разные мутации и хромосомные делеции. Для выявления потери участков хромосом используются лабораторные методы, а процесс утраты генетической информации был назван "потерей гетерозиготности".
В ходе своего развития опухолевая клетка кишечника человека претерпевает определенные изменения (рис. 10-2). Гипометилирование ДНК происходит на ранних стадиях возникновения канцерогенеза в аденомах. В клетках небольших аденом могут происходить как мутации, так и выпадения участков хромосом, например изменения на 5q хромосоме при аденоматозном полипозе кишки. Обнаруживаемые в крупных аденоматозных полипах мутации генов K-RASvip53 играют заметную роль в поддержании опухолевого роста. Делеции генов супрессоров опухолевого роста на 18q (встречается при раке толстой кишки) и 17р (локус гена р53) происходят на поздних стадиях и означают малигнизацию процесса. Несмотря на наличие сходства канцерогенеза в толстой кишке и в других отделах желудочно-кишечного тракта, последовательность изменений, а также вовлеченные в процесс гены различны. Детали этих процессов только начинают исследоваться.
Механизмы, замедляющие опухолевую прогрессию. В происхождении опухолей толстой кишки, помимо выпадения супрессорных генов, задействованы и другие механизмы генетических изменений. Микросателлиты — участки ДНК, используемые для картирования генов хромосом. Обычно микросателлиты полностью копируются при репликации клеток, но в некоторых опухолевых клетках отмечается незначительное изменение их длины. Микросателлиты в геноме могут иметь до 103 копий. Было замечено, что в некоторых случаях рака толстой кишки эти микросателлиты копируются не полностью. Наличие "нестабильных" микросателлитов в геноме опухолевых клеток говорит об утрате ими способности адекватно копировать гены. Такое нарушение процессов исправления мутаций считается еще одним механизмом канцерогенеза. Примерная схема этого механизма приведена на Рис. 10-3.
Дата добавления: 2015-02-23; просмотров: 1017;
