СЕПТИЧЕСКИЙ ШОК
Сепсис, являясь первостепенной медицинской проблемой и на сегодняшний день, продолжает оставаться одной из ведущих причин смертности, несмотря на различные открытия в патогенезе этого заболевания и применение новых принципов лечения. Тяжелым осложнением сепсиса является септический шок.
Септический шок — сложный патофизиологический процесс, возникающий в результате действия экстремального фактора, связанного с прорывом в кровоток возбудителей или их токсинов, что вызывает наряду с повреждением тканей и органов чрезмерное неадекватное напряжение неспецифических механизмов адаптации и сопровождается гипоксией, гипоперфузией тканей, глубокими расстройствами обмена.
В литературе септический шок принято обозначать как инфекционно-токсический, бактериотоксический или эндотоксический шок. Тем самым подчеркивается, что данный вид шока развивается только при генерализованных инфекциях, протекающих с массивной бактериемией, интенсивным распадом бактериальных клеток и высвобождением эндотоксинов, нарушающих регуляцию объема сосудистого русла. Септический шок может развиваться не только при бактериальных, но и при вирусных инфекциях, инвазиях простейшими, грибковом сепсисе и др.
В общеклинической практике проблема септического шока сейчас приобрела особую актуальность в связи с повсеместным ростом септических заболеваний. Число больных сепсисом за последние годы возросло в 4—6 раз [Gomez J. et al., 1995]. Этому способствовало широкое, часто нерациональное применение антибиотиков, подавляющих конкурентную флору и создающих условия для селекции нечувствительных к ним возбудителей, а также использование глюкокортикостероидов и иммунодепрессантов, угнетающих защитные механизмы. Немаловажную роль играют увеличение среднего возраста больных, а также преобладание в этиологии сепсиса «госпитальной» флоры, резистентной к антибиотикам.
Развитие внутрибольничного сепсиса и септического шока может быть обусловлено различными факторами. Вероятность инфицирования и риск развития септического шока несут с собой некоторые диагностические и лечебные процедуры, загрязнение внутривенных сред. Большой процент септических состояний связан с послеоперационными осложнениями. Повышенной вероятности развития сепсиса могут способствовать некоторые неотложные состояния, например панкреатит, жировая эмболия, геморрагический шок, ишемия и различные формы травм, сопровождающиеся повреждением тканей. Хронические заболевания, осложненные изменениями в иммунной системе, могут увеличить риск возникновения генерализованной инфекции.
В этиологии септического шока чаще всего преобладает грамотрицательная инфекция (65—70 % случаев), но он может развиться и при сепсисе, вызванном грамположительными бактериями.
Достижения в области молекулярной биологии и иммунологии предоставили возможность понять многие патогенетические механизмы развития септического шока. В настоящее время доказано, что инфекция сама по себе не является непосредственной причиной многочисленных патологических сдвигов, характерных для сепсиса. Скорее всего они возникают как результат ответной реакции организма на инфекцию и некоторые другие факторы. Этот ответ обусловлен усилением действия различных эндогенных молекулярных веществ, которые запускают патогенез сепсиса. Если при нормальном состоянии подобные молекулярные реакции можно расценить как реакции приспособления или адаптации, то во время сепсиса их чрезмерная активация носит повреждающий характер. Известно, что некоторые из этих активных молекул могут высвобождаться непосредственно на эндотелиальной мембране органа-мишени, приводя к поражению эндотелия, и вызывать дисфункцию органа.
Некоторые известные медиаторы повреждения эндотелия, вовлекаемые в септические реакции:
• туморнекротизирующий фактор (TNF);
• интерлейкины (ИЛ-1, ИЛ-4, ИЛ-6, ИЛ-8);
• фактор активации тромбоцитов (PAF);
• лейкотриены (В4, С4, D4, Е4);
• тромбоксан А2;
• простагландины (Е2, Е12);
• простациклин;
• гамма-интерферон.
Наряду с вышеперечисленными медиаторами повреждения эндотелия в патогенез сепсиса и септического шока вовлекается много других эндогенных и экзогенных медиаторов, которые становятся слагаемыми воспалительного ответа.
Потенциальные медиаторы септического воспалительного ответа:
• эндотоксин;
• экзотоксин, части клеточной стенки грамотрицательной бактерии;
• комплемент, продукты метаболизма арахидоновой кислоты;
• полиморфно-ядерные лейкоциты, моноциты, макрофаги, тромбоциты;
• гистамин, клеточные адгезивные молекулы;
• каскад коагуляции, фибринолитическая система;
• токсические метаболиты кислорода и другие свободные радикалы;
• калликреин-кининовая система, катехоламины, стрессовые гормоны.
Развитие септического процесса осложняется тем, что медиаторы сепсиса могут взаимодействовать между собой, активируя друг друга. Следовательно, в развитии септического шока в отличие от других видов шока важную роль играет взаимодействие эндотоксина с медиаторными системами организма. Общепризнанно, что септический шок, как и анафилактический, является иммунопатологическим состоянием, когда в ответ на «прорыв инфекта» нарушается или снижается фагоцитоз, в крови появляются блокирующие субстанции и развивается вторичный иммунный дефицит. Эндотоксин также выполняет роль индуктора макрофагов и каскадных систем, персистирующего и после нарушений гомеостаза. В развитии этих изменений ведущее значение принадлежит TNF, интерлейкинам (ИЛ-1, ИЛ-6, ИЛ-8) и т.д. Кроме того, микробная инвазия и токсемия быстро приводят к глубоким метаболическим, эндокринным и циркуляторным расстройствам.
Нарушения гемодинамики и транспорта кислорода при септическом шоке занимают одно из центральных мест и отличаются большой сложностью. Некоторые исследователи утверждают, что одновременное и разнонаправленное действие этиологических и патогенетических факторов при септическом шоке приводит к нарушению распределения кровотока и органной перфузии даже на фоне нормального АД и высокого СВ. На первый план при шоке выступают именно нарушения микроциркуляции, а артериальная гипотензия является поздним симптомом септического шока.
Выделяют два основных синдрома расстройств кровообращения, которые характеризуют стадии развития септического шока, — гипердинамический и гиподинамический. Для ранней стадии септического шока, сопровождающейся циркуляторной гипердинамией, как правило, характерно снижение общего сосудистого сопротивления с рефлекторно обусловленным (с барорецепторов) увеличением СВ и работы сердца. Это, возможно, связано с прямым влиянием быстро накапливающейся бактериальной флоры и эндотоксинов на сердечно-сосудистую систему и клеточный метаболизм. Причинами снижения периферической сосудистой резистентности являются открытие низкорезистентных артериовенозных шунтов и непосредственный сброс крови через них. При этом значительно увеличиваются потребление кислорода и индекс его доставки, в то время как экстракция кислорода находится в пределах нормы. Дальнейшая манифестация септического шока также характеризуется значительными изменениями в симпатико-адреналовой, гипофизарно-надпочечниковой, калликреин-кининовой и других системах регуляции гомеостаза. Для следующей стадии септического шока характерны гипердинамический режим кровообращения и нарушения транспорта кислорода. В этой стадии шока сохраняется повышенная производительность сердца: существенно увеличена работа левого желудочка, однако СИ лишь незначительно превышает норму. В результате преобладания активности норадреналина, альфа-адреномиметическое действие которого способствует вазоконстрикции, повышается общее периферическое сосудистое сопротивление. Неизбежным следствием этого является развивающаяся тканевая гипоксия. Снижаются потребление кислорода и индекс его доставки тканям, существенно увеличивается экстракция кислорода. Развивается блокада утилизации кислорода на субклеточном уровне с накоплением лактата.
В поздних стадиях развития септического шока, несмотря на продолжительную вазоконстрикцию и перераспределение крови на периферии, наблюдается снижение преднагрузки, объясняемое опустошением капиллярного функционирующего русла и, главное, жидкостной экстравазацией. Этим и определяется развитие вторичного гиповолемического синдрома. Вместе с миокардиодепрессией гиповолемия формирует гиподинамический синдром. Стадия гиподинамического режима кровообращения характеризуется низкими показателями СВ, доставки и потребления кислорода на фоне повышенной экстракции последнего. Экстракция кислорода резко падает в терминальной стадии шока. Значительное повышение экстракции кислорода на фоне сниженной его доставки и потребления обусловлено не только перфузионной недостаточностью и гипоксемией, но и значительным нарушением клеточного метаболизма и утилизации кислорода [Gutierrez G., 1991]. Компенсаторная вазоконстрикция с повышением общего сосудистого сопротивления может наблюдаться также и в гиподинамической фазе септического шока. Значительное повышение легочного сосудистого сопротивления и легочная гипертензия становятся дополнительными факторами прогрессирования миокардиальной недостаточности.
Установлено, что детерминирующим фактором в специфике нарушений гемодинамики при септическом шоке являются не особенности микрофлоры, а системная реакция организма больного, в которой большую роль играет повреждение иммунной системы [Shapiro L. et al., 1993]. Гипер- и гиподинамические синдромы как при грамположительной, так и при грамотрицательной бактериемии наблюдаются практически с одинаковой частотой.
Следует подчеркнуть, что при септическом шоке раньше всего повреждается главный орган-мишень — легкие. Основная причина дисфункции легких обусловлена повреждением эндотелия медиаторами и факторами воспаления, что увеличивает проницаемость кровеносных сосудов, приводит к их микроэмболизации и капиллярной дилатации [Shapiro L. et al., 1993]. Изменения проницаемости клеточной мембраны могут вести к трансмембранному потоку низкомолекулярных веществ и макроионов, что сопровождается нарушением функции клеток. Таким образом развивается интерстициальный отек легких.
Как только возникает повреждение эндотелия, в органах и тканях, являющихся мишенью, увеличивается вероятность развития полиорганной недостаточности. За дисфункцией легких могут последовать сначала печеночная, затем почечная недостаточность, что и формирует синдром полиорганной недостаточности (СПОН) [Gates D.M., 1994]. По мере развития СПОН каждый из органов оказывается не в состоянии адекватно функционировать, что приводит к появлению новых факторов повреждающего воздействия на другие органы и системы организма.
В патогенезе септического шока важнейшим звеном являются расстройства микроциркуляции. Они обусловлены не только вазоконстрикцией, но и значительным ухудшением агрегатного состояния крови с нарушением ее реологических свойств и развитием синдрома диссеминированного внутрисосудистого свертывания (ДВС) крови или тромбогеморрагического синдрома. Септический шок приводит к расстройствам всех метаболических систем. Нарушаются углеводный, белковый и жировой обмен, резко угнетается утилизация нормальных источников энергии — глюкозы и жирных кислот. При этом возникает резко выраженный катаболизм мышечного белка. В целом обмен веществ сдвигается на анаэробный путь.
Таким образом, в основе патогенеза септического шока лежат глубокие и прогрессирующие расстройства гуморальной регуляции, метаболизма, гемодинамики и транспорта кислорода. Взаимосвязь этих нарушений может привести к формированию порочного круга с полным истощением адаптационных возможностей организма. Предотвращение развития этого порочного круга и является основной задачей интенсивной терапии больных с септическим шоком.
Клиническая картина. Изменения функций жизненно важных органов под влиянием повреждающих факторов септического шока формируют динамический патологический процесс, клинические признаки которого выявляются в виде нарушений функцийЦНС, легочного газообмена, периферического и центрального кровообращения, а в последующем и в виде органных повреждений.
Прорыв инфекта из очага воспаления или поступление эндотоксина в кровоток запускают первичный механизм септического шока, в котором проявляется пирогенное действие инфекта и прежде всего эндотоксина. Гипертермия выше 38—39 °С, потрясающий озноб являются ключевыми признаками в диагностике септического шока. Очень часто постепенно прогрессирующую лихорадку гектического или неправильного типа, достигающую предельных величин и нехарактерную для данного возраста (40—41 °С у пожилых больных), а также полипноэ и умеренные нарушения кровообращения, главным образом тахикардию (ЧСС более 90 в минуту), считают реакцией на травму и операцию. Иногда такие симптомы служат основанием для диагноза местной инфекции. Однако эта фаза септического шока носит название «теплой нормотензии» и часто не диагностируется. При исследовании центральной гемодинамики определяется гипердинамический режим кровообращения (СИ более 5 л/мин/м2) без нарушения транспорта кислорода (РТК 800 мл/мин/м2 и более), что характерно для ранней стадии септического шока.
При прогрессировании процесса данную клиническую фазу септического шока сменяет фаза «теплой гипотензии», для которой характерны максимальное повышение температуры тела, ознобы, изменения психического состояния больного (возбуждение, беспокойство, неадекватность поведения, иногда психоз). При осмотре больного кожа теплая, сухая, гиперемированная или розовая. Нарушения дыхания выражены по типу гипервентиляции, которая в дальнейшем приводит к дыхательному алкалозу и утомлению дыхательной мускулатуры. Отмечается тахикардия до 120 ударов и более в минуту, которая сочетается с хорошим наполнением пульса и гипотензией (Адсист < 100 мм рт.ст.). Гипотензия скорее умеренная и обычно не привлекает внимание врачей. Уже в этой стадии септического шока выявляются признаки неспособности системы кровообращения обеспечить потребность тканей в кислороде и питательных веществах, а также создать возможность детоксикации и удаления токсичных метаболитов. Для того чтобы поддержать адекватность перфузии тканей и избежать анаэробного окисления, больным необходим более высокий уровень DO2 (15 мл/мин/кг вместо 8—10 мл/мин/кг в норме). Однако в этой стадии септического шока даже повышенный СВ (СИ 4,3—4,6 л/мин/м2) не обеспечивает должной потребности в кислороде.
Нередко гемодинамические и дыхательные изменения сочетаются с отчетливыми нарушениями деятельности пищеварительного тракта: диспепсические расстройства, боли (особенно в верхней части живот), понос, которые можно объяснить особенностями метаболизма серотонина, начальными изменениями кровотока в зоне чревных сосудов и активацией центральных механизмов тошноты и рвоты. В этой фазе септического шока отмечается снижение диуреза, иногда достигающее уровня олигурии (мочеотделение менее 25 мл/ч).
Клиническая картина поздней стадии септического шока характеризуется нарушениями сознания, выраженными расстройствами легочного газообмена, периферической и центральной циркуляторной недостаточностью, органной патологией с признаками печеночной и почечной недостаточности. Внешние проявления этой стадии септического шока получили название «холодной гипотензии». При осмотре больного обращают на себя внимание затемнение сознания, вплоть до развития коматозного состояния; бледность кожных покровов; акроцианоз, иногда значительный; олигоанурия. Выраженное тахипноэ (более 40 дыханий в 1 мин) сочетается с ощущением нехватки воздуха, которое не уменьшается даже на фоне оксигенотерапии; вдыхании, как правило, участвуют вспомогательные мышцы.
Озноб и гипертермия сменяются снижением температуры тела, нередко с ее критическим падением до субнормальных цифр. Кожная температура дистальных отделов конечностей даже на ощупь значительно ниже обычной. Снижение температуры тела сочетается с отчетливой вегетативной реакцией в виде проливных потов. Холодные, бледно-цианотичные, влажные кисти и стопы — это один из патогномоничных симптомов неблагоприятного течения генерализованной инфекции. Одновременно выявляются относительные признаки уменьшения венозного возврата в виде запустевания периферической венозной подкожной сети. Частый, 130—160 в минуту, слабого наполнения, иногда аритмичный, пульс сочетается с критическим снижением системного АД, нередко с малой пульсовой амплитудой.
Наиболее ранним и четким признаком органного поражения является прогрессирующее нарушение функций почек с такими тяжелыми симптомами, как азотемия и нарастающая олигоанурия (диурез менее 10 мл/ч).
Поражения желудочно-кишечного тракта проявляются в виде динамической кишечной непроходимости и желудочно-кишечных кровотечений, которые в клинической картине септического шока могут превалировать даже в тех случаях, когда он не перитонеального генеза. Поражение печени характеризуется появлением желтухи и гипербилирубинемией.
Принято считать, что снабжение организма кислородом бывает достаточно адекватным при концентрации гемоглобина >100 г/л, SаO2 > 90 % и СИ>2,2 л/мин/м2. Тем не менее у больных с выраженным перераспределением периферического кровотока и периферическим шунтированием кислородное снабжение даже при этих показателях может быть неадекватным, в результате чего развивается гипоксия с высоким кислородным долгом, что характерно для гиподинамической стадии септического шока. Высокое потребление тканями кислорода в сочетании с низким транспортом последнего свидетельствует о возможности неблагоприятного исхода, тогда как повышенное потребление кислорода в сочетании с повышением его транспорта является признаком, благоприятным практически для всех вариантов шока.
Большинство клиницистов считают, что основными объективными диагностическими критериями сепсиса являются изменения периферической крови и метаболические расстройства.
Наиболее характерные изменения крови: лейкоцитоз (12 x 109/л) с нейтрофильным сдвигом, резкое «омоложение» лейкоцитарной формулы и токсическая зернистость лейкоцитов. В то же время следует помнить о неспецифичности нарушений отдельных показателей периферической крови, их зависимости от циркуляторного гомеостаза, постоянно меняющейся клинической картины заболевания и влияния лечебных факторов. Принято считать, что для септического шока характерными объективными критериями могут быть лейкоцитоз с нарастанием лейкоцитарного индекса интоксикации (ЛИИ>10) и тромбоцитопения. Иногда динамика лейкоцитарной реакции имеет волнообразный характер: начальный лейкоцитоз сменяется лейкопенией, совпадающей по времени с психическими и диспепсическими расстройствами, появлением полипноэ, а затем вновь наблюдается быстрое нарастание лейкоцитоза. Но даже и в этих случаях величина ЛИИ прогрессивно увеличивается. Этот показатель рассчитывают по формуле [Кальф-Калиф Я.Я., 1943]:
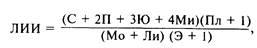
где С — сегментоядерные нейтрофилы, П — палочкоядерные, Ю — юные, Ми — миелоциты, Пл — плазматические клетки, Мо — моноциты. Ли — лимфоциты, Э —эозинофилы.
Нормальная величина индекса колеблется около 1. Повышение ЛИИ до 4—9 свидетельствует о значительном бактериальном компоненте эндогенной интоксикации, тогда как умеренное повышение индекса до 2—3 указывает на ограничение инфекционного процесса или преимущественный тканевый распад. Лейкопения с высоким ЛИИ является всегда тревожным симптомом септического шока.
В поздней стадии септического шока при гематологических исследованиях, как правило, выявляются умеренная анемия (Нb 90—100 г/л), гиперлейкоцитоз до 40x109/л и выше с предельным возрастанием ЛИИ до 20 и более. Иногда увеличивается количество эозинофилов, что уменьшает ЛИИ, несмотря на отчетливый сдвиг лейкоцитарной формулы в сторону незрелых форм нейтрофилов. Может наблюдаться лейкопения с отсутствием нейтрофильного сдвига. При оценке лейкоцитарной реакции необходимо обращать внимание на снижение абсолютной концентрации лимфоцитов, которое может быть в 10 раз и более ниже нормальной величины.
Среди данных стандартного лабораторного контроля заслуживают внимание показатели, характеризующие состояние метаболического гомеостаза. Наиболее распространена диагностика метаболических расстройств на основании контроля сдвигов КОС, газов крови и оценки концентрации лактата в крови. Как правило, характер и форма расстройств КОС, а также уровень лактата зависят от тяжести и стадии развития шока. Достаточно выражена корреляция между концентрациями лактата и эндотоксина в крови, особенно при септическом шоке.
При исследовании КОС крови на ранних стадиях септического шока нередко определяется компенсированный или субкомпенсированный метаболический ацидоз на фоне гипокапнии и высокого уровня лактата, концентрация которого достигает 1,5—2 ммоль/л и более. В ранней стадии септицемии наиболее характерен временный респираторный алкалоз. У некоторых больных отмечается метаболический алкалоз. В поздних стадиях развития септического шока метаболический ацидоз становится некомпенсированным и по дефициту оснований нередко превышает 10 ммоль/л. Уровень лактат-ацидемии достигает 3—4 ммоль/л и более и является критерием обратимости септического шока. Как правило, определяется существенное снижение РаО2, SaO2 и, следовательно, уменьшение кислородной емкости крови. Следует подчеркнуть, что выраженность ацидоза в значительной степени коррелирует с прогнозом.
В диагностике и лечении септического шока становится все более и более необходимым динамическое определение показателей центральной гемодинамики (МОС, УО, СИ, ОПСС и др.) и транспорта кислорода (a-V — разница по кислороду, СаО2, РаО2, SaО2), которые позволяют оценить и определить стадию шока и компенсаторные резервы организма. СИ в сочетании с другими факторами, характеризующими особенности транспорта кислорода в организме и тканевый обмен служат критериями не только эффективности кислородного обеспечения, но и ориентировки в прогнозе септического шока и выборе основного направления интенсивной терапии расстройств кровообращения при внешне одинаковых проявлениях этого патологического процесса — гипотензии и низком темпе диуреза.
Кроме функционального исследования, диагностика включает выявление этиологического фактора — определение возбудителя и изучение его чувствительности к антибактериальным препаратам. Проводят бактериологическое исследование крови, мочи, раневого экссудата и т.д. С помощью биологических тестов исследуют выраженность эндотоксинемии. В клиниках проводится диагностика иммунной недостаточности на основании общих тестов: Т- и В-лимфоциты, бласттрансформация, уровень иммуноглобулинов в сыворотке крови.
Диагностические критерии септического шока:
• наличие гипертермии (температура тела >38—39 °С) и ознобов. У пациентов пожилого возраста парадоксальная гипотермия (температура тела <36 °С);
• нейропсихические расстройства (дезориентация, эйфория, возбуждение, сопор);
• гипер- или гиподинамический синдром нарушения кровообращения. Клинические проявления: тахикардия (ЧСС =100—120 в минуту), Адсист< 90 мм рт.ст. или его снижение на 40 мм рт.ст. и более от среднего в отсутствие других причин гипотензии;
• расстройства микроциркуляции (холодные, бледные, иногда слегка или интенсивно желтушные кожные покровы);
• тахипноэ и гипоксемия (ЧСС>20 в минуту или PaCO2<32 мм рт.ст., акроцианоз);
• олигоанурия, мочеотделение — менее 30 мл/ч (или необходимость применения диуретиков для поддержания достаточного диуреза);
• рвота, понос;
• число лейкоцитов >12,0•109/л, 4,0•109/л или незрелые формы >10 %, ЛИИ >9-10;
• уровень лактата >2 ммоль/л.
Некоторые клиницисты выделяют триаду симптомов, которая служит продромой септического шока:нарушение сознания (изменение поведения и дезориентация);гипервентиляцию, определяемую на глаз, иналичие очага инфекции в организме.
В последние годы находит широкое применение балльная шкала оценки органной недостаточности, связанной с сепсисом и шоком (шкала SOFA — Sepsis-related Organ Failure Assessment) (табл. 17.1). Полагают, что данная шкала, принятая Европейским обществом интенсивной терапии, является объективной, доступной и простой в оценке дисфункции органов и систем при прогрессировании и развитии септического шока.
Таблица 17.1.
Шкала SOFA [Vincent J.L. et al., 1996]
| Оценка | Показатель | ||||
| Оксигенация | PaO2/FiO2, мм рт.ст. | <400 | <300 | <200 | <100 |
| Коагуляция | Тромбоциты | <150•109/л | <100•109/л | <50•109/л | <20•109/л |
| Печень | Билирубин, мг/дл, мкмоль/л | 1,2-1,9 (20-32) | 2,0-5,9 (33-101) | 6,0-11,9 (102-204) | >12 (>204) |
| Сердечнососудистая система | Гипотензия или степень инотропной поддержки | САД<70 мм рт.ст. | Допамин < 5 или добута-мин (любая доза) | Допамин >5* или адреналин <0,1* или норадре-налин < 0,1* | Допамин >15* или адреналин >0,1* норадреналин >0,1* |
| ЦНС | Показатель по шкале комы Glasgow, в баллах | 13-14 | 10-12 | 6-9 | <6 |
| Почки | Креатинин, мг/дл, мкмоль/л. Возможна олигурия | 1,2-1,9 (110-170) | 2,0-3,4 (171-299) | 3,5-4,9 (300-440) или <500 мл мочи/сут | > 5,0 (> 440) или <200 мл мочи/сут |
Доза кардиотоников в мг на 1 кг массы тела в 1 мин в течение не менее
Дисфункция каждого органа (системы) оценивается отдельно, в динамике, ежедневно, на фоне интенсивной терапии.
Лечение. Сложность патогенеза септического шока определяет многокомпонентный подход к его интенсивной терапии, так как лечение недостаточности только одного органа нереально. Только при комплексном подходе к лечению можно надеяться на относительный успех.
Интенсивное лечение должно осуществляться в трех принципиальных направлениях. Первое по времени и по значимости — надежное устранение основного этиологического фактора или заболевания, запустившего и поддерживающего патологический процесс. При неустраненном очаге инфекции любая современная терапия будет безрезультатной. Второе — лечение септического шока невозможно без коррекции общих для большинства критических состояний расстройств: гемодинамики, газообмена, геморео-логических нарушений, гемокоагуляции, водно-электролитных сдвигов, метаболической недостаточности и т.д. Третье — непосредственное воздействие на функцию пораженного органа, вплоть до временного протезирования, следует начинать рано, до развития необратимых изменений.
Антибактериальная терапия, иммунокоррекция и адекватное хирургическое лечение септического шока в борьбе с инфекцией имеют важное значение. Необходимо начинать раннее лечение антибиотиками до выделения и идентификации культуры. Это имеет особенное значение у пациентов с нарушенным иммунитетом, когда задержка лечения свыше 24 ч может закончиться неблагоприятным исходом. При септическом шоке рекомендуется немедленное применение антибиотиков широкого спектра действия парентерально. Выбор антибиотиков обычно определяется следующими факторами: вероятный возбудитель и его чувствительность к антибиотикам; заболевание, лежащее в основе; иммунный статус пациента и фармакокинетика антибиотиков. Как правило, применяют комбинацию антибиотиков, что обеспечивает их высокую активность против широкого спектра микроорганизмов до того, как станут известны результаты микробиологического исследования. Часто используются комбинации цефалоспоринов 3—4-го поколения (лонгацеф, роцефин и др.) с аминогликозидами (гентамицин или амикацин). Доза гентамицина при парентеральном введении составляет 5 мг/кг/сут, амикацина — 10—15 мг/кг массы тела. Лонгацеф имеет большой период полураспада, поэтому может применяться 1 раз в сутки до 4 г, роцефин — до 2 г 1 раз в сутки. Антибиотики, которые имеют короткий период полураспада, должны назначаться в больших суточных дозах. Широко применяются клафоран (150—200 мг/кг/сут), цефтазидим (до 6 г/сут) и цефалоспорин (160 мг/кг/сут). При лечении больных с септическим очагом в пределах брюшной полости или малого таза можно прибегнуть к комбинации гентамицина и ампициллина (50 мг/кг в сутки) или линкомицина. При подозрении на грамположительную инфекцию часто используется ванкомицин (ванкоцин) до 2 г/сут. При определении чувствительности к антибиотикам терапия может быть изменена. В случаях, когда удалось идентифицировать микрофлору, выбор антимикробного препарата становится прямым. Возможно использование монотерапии с помощью антибиотиков, имеющих узкий спектр действия.
В некоторых случаях наряду с антибиотиками в антибактериальную комбинацию препаратов могут быть включены и мощные антисептики: диоксидин до 0,7 г/сут, метронидазол (флагил) до 1,5 г/сут, солафур (фурагин) до 0,3—0,5 г/сут. Такие комбинации предпочтительно использовать в тех случаях, когда трудно ожидать достаточной эффективности от обычных антибиотиков, например при предшествующей длительной антибактериальной терапии.
Важным звеном в лечении септического шока является применение средств, усиливающих иммунные свойства организма. Больным вводят гамма-глобулин или полиглобулин, специфические антитоксические сыворотки (антистафилококковые, антисинегнойная).
Мощная интенсивная терапия не будет иметь успеха, если не устранить очаги инфекции хирургическим путем. Неотложное хирургическое вмешательство может иметь существенное значение на любой стадии. Обязательны дренирование и удаление очага воспаления. Оперативное вмешательство должно быть малотравматичным, простым и достаточно надежным для обеспечения первичного и последующего удаления из очага микроорганизмов, токсинов и продуктов тканевого распада. Необходимо постоянно следить за появлением новых метастатических очагов и устранять их.
В интересах оптимальной коррекции гомеостаза клиницист должен одновременно обеспечивать коррекцию различных патологических изменений. Считают, что для адекватного уровня потребления кислорода необходимо поддерживать СИ не менее 4,5 л/мин/м2, при этом уровень DO2 должен быть более 550 мл/мин/м2. Тканевое перфузионное давление можно считать восстановленным при условии, когда среднее АД не менее 80 мм рт.ст., а ОПСС около 1200 дин•с/(см5•м2). В то же время необходимо избегать чрезмерной вазоконстрикции, которая неизбежно ведет к снижению перфузии тканей.
Проведение терапии, корригирующей гипотензию и поддерживающей кровообращение, имеет при септическом шоке очень большое значение, так как нарушение кровообращения является одним из ведущих симптомов шока. Первым средством в этой ситуации является восстановление адекватного сосудистого объема. В начале терапии внутривенно может быть введена жидкость из расчета 7 мл/кг массы тела за 20—30 мин. Улучшение гемодинамики наблюдается по мере восстановления нормального давления наполнения желудочков и среднего АД. Необходимо переливать коллоидные растворы, так как они более эффективно восстанавливают как объем, так и онкотическое давление.
Несомненный интерес представляет применение гипертонических растворов, так как они способны быстро восстанавливать объем плазмы благодаря извлечению ее из интерстиция. Восстановление внутрисосудистого объема одними кристаллоидами требует увеличения инфузии в 2—3 раза. В то же время, учитывая порозность капилляров, чрезмерная гидратация интерстициального пространства способствует формированию отека легких. Кровь переливают с таким расчетом, чтобы поддерживать уровень гемоглобина в пределах 100—120 г/л или гематокрита 30—35 %. Общий объем инфузионной терапии составляет 30—45 мл/кг массы тела с учетом клинических (САД, ЦВД, диурез) и лабораторных показателей.
Решающее значение для улучшения показателей доставки кислорода к тканям имеет адекватное восполнение объема жидкости. Этот показатель можно легко изменять с помощью оптимизации СВ и уровня гемоглобина. При проведении инфузионной терапии диурез должен быть не менее 50 мл/ч. Если после восполнения объема жидкости давление продолжает оставаться низким, для увеличения СВ применяют допамин в дозе 10—15 мкг/кг/мин или добутамин в дозе 0,5—5 мкг/(кг-мин). Если гипотензия сохраняется, можно провести коррекцию адреналином в дозе 0,1—1 мкг/кг/мин. Адренергический вазопрессорный эффект адреналина может потребоваться у пациентов с упорной гипотензией на фоне применения допамина или у тех, кто реагирует только на его высокие дозы. В связи с опасностью ухудшения транспорта кислорода и его потребления можно сочетать адреналин с вазодилататорами (нитроглицерин 0,5— 20 мкг/кг/мин, нанипрусс 0,5—10 мкг/кг/мин). В лечении выраженной вазодилатации, наблюдаемой при септическом шоке, должны использоваться мощные сосудосуживающие препараты, например норадреналин от 1 до 5 мкг/кг/мин или допамин в дозе более 20 мкг/кг/мин.
Вазоконстрикторы могут давать вредные эффекты и должны использоваться для восстановления ОПСС до нормальных пределов 1100— 1200 дин• с/см5м2 только после оптимизации ОЦК. Дигоксин, глюкагон, кальций, антагонисты кальциевых каналов должны использоваться строго индивидуально.
Пациентам с септическим шоком показана респираторная терапия. Поддержка дыхания облегчает нагрузку на систему DO2 и снижает кислородную цену дыхания. Газообмен улучшается при хорошей оксигенации крови, поэтому всегда требуются проведение оксигенотерапии, обеспечение проходимости дыхательных путей и улучшение дренажной функции трахеобронхиального дерева. Необходимо поддерживать РаОз на уровне не менее 60 мм рт.ст., а сатурацию гемоглобина не менее 90 %. Выбор метода лечения ОДН при септическом шоке зависит от степени нарушения газообмена в легких, механизмов его развития и признаков избыточной нагрузки на аппарат дыхания. При прогрессировании дыхательной недостаточности методом выбора является ИВЛ в режиме ПДКВ.
Особое внимание при лечении септического шока придается улучшению гемоциркуляции и оптимизации микроциркуляции. Для этого применяют реологические инфузионные среды (реополиглюкин, плазмастерил, HAES-стерил, реоглюман), а также курантил, компламин, трентал и др.
Метаболический ацидоз можно скорригировать, если рН будет ниже 7,2. однако это положение остается дискуссионным, так как бикарбонат натрия может усугубить ацидоз (сдвиг КДО влево, ионная асимметрия и др.).
В процессе интенсивной терапии должны быть устранены нарушения коагуляции, так как септический шок всегда сопровождается ДВС-синдромом.
Наиболее перспективными представляются лечебные мероприятия,
направленные на пусковые, начальные, каскады септического шока. В качестве протекторов повреждения клеточных структур целесообразно использовать антиоксиданты (токоферол, убихинон), а для ингибирования протеаз крови — антиферментные препараты (гордокс — 300 000—500 000 ЕД, контрикал - 80 000—150 000 ЕД, трасилол - 125 000-200 000 ЕД). Также необходимо применение средств, ослабляющих действие гуморальных факторов септического шока, — антигистаминных препаратов (супрастин, тавегил) в максимальной дозе.
Использование глюкокортикоидов при септическом шоке является одним из спорных вопросов терапии этого состояния. Многие исследователи считают, что необходимо назначать большие дозы кортикостероидов, но только однократно. В каждом случае требуется индивидуальный подход с учетом иммунологического статуса пациента, стадии шока и тяжести состояния. Мы считаем, что оправданным может быть применение стероидов высокой активности и продолжительности действия, у которых менее выражены побочные эффекты. К таким препаратам относятся кортикостероиды дексаметазон и бетаметазон.
В условиях инфузионной терапии наряду с задачей поддержания водно-электролитного равновесия обязательно решаются вопросы энергетического и пластического обеспечения. Энергетическое питание должно составлять не менее 200—300 г глюкозы (с инсулином) в день. Общая калорийность парентерального питания — 40—50 ккал/кг массы тела в сутки. Многокомпонентное парентеральное питание можно начинать только после выведения пациента из септического шока.
К. Мартин и соавт. (1992) разработали схему коррекции гемодинамики при септическом шоке, которая обеспечивает эффективную терапию нарушений кровообращения и транспорта кислорода и может быть использована в практической деятельности.
Рациональная коррекция гемодинамики. Необходимо выполнить в течение 24—48 ч следующие принципиальные терапевтические задачи.
Обязательно:
• СИ не менее 4,5 л/(мин-м2);
• уровеньDO2 не менее 500 мл/(мин-м2);
• среднее АД не менее 80 мм рт.ст.;
• ОПСС в пределах 1100-1200 дин-сДсм^м2).
По возможности:
• уровень потребления кислорода не менее 150 мл/(мин-м2);
• диурез не менее 0,7 мл/(кг'ч).
Для этого требуется:
1) восполнить ОЦК до нормальных величин, обеспечить Ра02 в артериальной крови не менее 60 мм рт.ст., сатурацию — не менее 90 %, а уровень гемоглобина — 100—120 г/л;
2) если СИ не менее 4,5 л/(мин-м2), можно ограничиться монотера-пией норадреналином в дозе 0,5—5 мкг/кг/мин. Если уровень СИ ниже 4,5 л/(мин-м2), вводят дополнительно добутамин;
3) если СИ исходно меньше 4,5 л/(мин-м2), необходимо начать лечение с добутамина в дозе 0,5—5 мкг/(кг-мин). Норадреналин добавляется в том случае, когда среднее АД остается менее 80 мм рт.ст.;
4) в сомнительных ситуациях целесообразно начать с норадреналина, а при необходимости дополнить терапию добутамином;
5) адреналин, изопротеренол или инодилататоры можно сочетать с добутамином для управления уровнем СВ; для коррекции ОПСС допа-мин или адреналин можно сочетать с норадреналином;
6) в случае олигурии используют фуросемид или небольшие дозы допа-мина (1—3 мкг/кг-мин);
7) каждые 4—6 ч необходимо контролировать параметры транспорта кислорода, а также корригировать лечение в соответствии с конечными целями терапии;
8) отмену сосудистой поддержки можно начинать через 24—36 ч пе риода стабилизации состояния. В некоторых случаях может потребоваться несколько дней для полной отмены сосудистых средств, особенно норадреналина. В первые дни пациент, помимо суточной физиологической потребности, должен получить 1000—1500 мл жидкости в качестве компенсации возникающей после отмены а-агонистов вазодилатации.
Авторы утверждают, что данная схема терапии септического шока и полиорганной недостаточности эффективна в 80—90 % случаев.
Таким образом, септический шок — достаточно сложный патофизиологический процесс, требующий как в диагностике, так и в лечении ос мысленного, а не шаблонного подхода. Сложность и взаимосвязанность патологических процессов, разнообразие медиаторов при септическом шоке создают множество проблем в выборе адекватной терапии этого грозного осложнения многих заболеваний.
Поданным J. Gomez и соавт. (1995), смертность при септическом шоке. несмотря на рациональную интенсивную терапию, составляет 40—80 %.
Появление перспективных методов иммунотерапии и диагностики открывает новые возможности лечения, улучшающие исходы септического шока. Обнадеживающие результаты получены при использовании моно-клональных антител к ядру эндотоксина и к фактору опухолевого некроза.
Дата добавления: 2015-02-23; просмотров: 1515;
