Определение йодного числа жира (методом Гануса)
Йодное число характеризует наличие в составе жира непредельных (ненасыщенных) жирных кислот. Его выражают массой йода (в г), которая может быть связана 100 г жира. По величине йодного числа судят о натуральности жира и изменениях, которые могут происходить при его хранении.
Йодное число определяют на основе реакции присоединения йода по месту двойных связей:
… - СН = СН - … + J2 = … - CHJ – CHJ - ….
При комнатной температуре йод реагирует с кислотами, входящими в состав жира, очень медленно; при нагревании присоединение йода идет неравномерно. Более интенсивно реагируют с непредельными кислотами жира соединения йода с другими галоидами (хлором, бромом). Поэтому были предложены методы определения йодного числа, в которых йод заменили его соединениями с галоидами. Гюбль предложил для определения йодного числа готовить раствор йода с сулемой (HgCl2 + 2J2 = HgJ2 + 2JCl), Ганус применил раствор бромистого йода.
Полное насыщение двойных связей происходит только в том случае, если масса галоида на 60-100 % выше теоретической.
Йодные числа некоторых жиров и масел имеют следующие величины: Молочный жир – 24¸45, говяжий – 32¸47, свиной – 46¸66, китовый 108¸130, жир печени трески – 118¸186, кокосовое масло – 8¸12, хлопковое – 100¸116, подсолнечное – 119¸136, льняное – 175¸201, бараний - 31÷46,
конский - 71÷86.
Жир выдерживают с избытком раствора бромистого йода в ледяной уксусной кислоте (раствор Гануса). При этом происходит присоединение йода по месту двойных связей жирных кислот:
 … - СН = СН - … + BrJ … - CHBr – CHJ - ….
… - СН = СН - … + BrJ … - CHBr – CHJ - ….
После выдерживания избыток бромистого йода разлагают водным раствором йодида калия:
 BrJ + KJ KBr + J2 ,
BrJ + KJ KBr + J2 ,
выделившийся йод оттитровывают раствором тиосульфата натрия:
 J2 + 2Na2S2 О3 2NaJ + Na2S4O6
J2 + 2Na2S2 О3 2NaJ + Na2S4O6
ХОД РАБОТЫ. В колбу вместимостью 300-500 мл с притертой стеклянной пробкой вносят 0,4-0,5 г жира (0,1 г растительного масла, китового или рыбьего жира) и растворяют его в 10 мл хлороформа или четыреххлористого углерода (опытная проба). В другую такую же колбу вносят 10 мл того же растворителя, но без жира (контрольная проба). В обе колбы из бюретки приливают по 25 мл раствора Гануса, перемешивают, закрывают пробками и ставят в темное место на 30 мин, периодически встряхивая.
По истечении указанного времени в обе колбы добавляют по 10 мл раствора с массовой концентрацией йодида калия 15 г/100 мл, содержимое перемешивают и приливают к нему по 100 мл свежепрокипяченной охлажденной дистиллированной воды, ополаскивая ею пробку. Выделившийся йод титруют раствором с концентрацией тиосульфата натрия 0,1 моль/л до слабо-желтого цвета. Затем вносят 1 мл раствора с массовой долей оклейстеренного крахмала 1 % и продолжают титрование по каплям до исчезновения синей окраски. Колбу закрывают пробкой и интенсивно встряхивают до извлечения йода, оставшегося в растворителе. При появлении синей окраски титрование продолжают до обесцвечивания.
Объем раствора тиосульфата натрия, израсходованный на все этапы титрования каждой пробы, записывают. Йодное число (Й.ч.) рассчитывают по формуле:
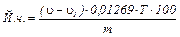 ,
,
где (u-u1) – разность между объемами раствора с концентрацией тиосульфата натрия 0,1 моль/л, израсходованными на титрование опытной (u1) и контрольной (u) проб, мл;
0,01269 - масса йода в граммах, соответствующая 1 мл раствора с концентрацией тиосульфата натрия 0,1 моль/л;
Т - титр раствора тиосульфата натрия;
m – масса жира, г.
РЕАКТИВЫ. Жир животный или растительный (фильтрованный); хлороформ или четыреххлористый углерод, раствор с концентрацией тиосульфата натрия 0,1 моль/л; раствор йодида калия (15 г йодида калия вносят в мерную колбу вместимостью 100 мл и, растворяя, объем доводят до метки водой); вода дистиллированная; раствор о массовой долей оклейстеренного крахмала 1 %; раствор Гануса (в 825 мл ледяной уксусной кислоты растворяют при нагревании 13,8 г йода. Охлаждают и 25 мл этого раствора титруют раствором с концентрацией тиосульфата натрия 0,1 моль/л. находят объем раствора тиосульфата, пошедший на титрование 1 мл приготовленного раствора йода (1-е титрование). Отмеривают 200 мл ледяной уксусной кислоты и приливают к ней 3 мл брома, содержимое перемешивают.
К 5 мл полученного раствора брома добавляют 10 мл раствора с массовой концентрацией йодида калия 15 г на 100 мл и титруют раствором тиосульфата натрия – 0,1 моль/л. Находят объем раствора тиосульфата, пошедшего на титрование 1 мл приготовленного раствора брома (2-е титрование) При первом и втором титрованиях в качестве индикатора используют раствор оклейстеренного крахмала. После титрований рассчитывают объем раствора брома, который нужно прилить для удвоения содержания галоида в оставшихся 800 мл раствора йода по формуле: А = В/С, где А - требуемый объем раствора брома, мл; В – находят умножением 800 на объем тиосульфата в мл, пошедший на титрование 1 мл раствора йода (1-е титрование); С – объем тиосульфата в мл, пошедший на титрование 1 мл раствора брома (2-е титрование). После смешивания в 1000 мл полученного раствора Гануса должно содержаться 13,2 г йода. Если окончательный раствор слишком крепкий, его разбавляют ледяной уксусной кислотой.
КОНТРОЛЬНЫЕ ВОПРОСЫ.
1. Строение и общая формула нейтральных жиров.
2. Номенклатура нейтральных жиров.
3. Чем характеризуются жирные кислоты, входящие в состав природных ацилглицеролов?
4. Какое состояние может иметь жир при комнатной температуре, и чем оно обусловлено?
5. Какие показатели используются для определения природы и качества жира?
6. Назовите физические и химические константы жиров.
7. Какие числа жира Вы знаете?
8. Методика подготовки жира к исследованию.
9. Что характеризует йодное число жира?
10. Что положено в основу определения йодного числа жира? Напишите уравнение.
11. Какие соединения и растворы используются для определения йодного числа и почему?
12. Назовите йодные числа некоторых жиров.
13. Химизм реакции раствора Гануса с жирными кислотами.
14. Химизм титрования йода раствором тиосульфата натрия.
Дата добавления: 2015-02-13; просмотров: 7031;
