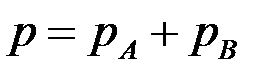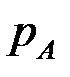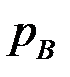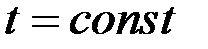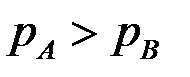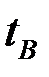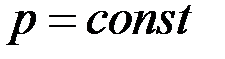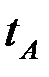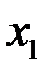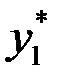Общие понятия о перегонке. Законы Рауля и Дальтона. Первый закон Коновалова
Перегонка (дистилляция и ректификация) – это частичное испарение жидкой смеси и последующая конденсация паров, осуществляемые однократно или многократно.
Перегонка основана на различной летучести компонентов жидкой смеси при одинаковой температуре. В процессе перегонки жидкая смесь обедняется низкокипящим компонентом (НК), а паровая фаза обогащается им.
Неиспарившаяся часть жидкой смеси – кубовый остаток, конденсат паровой фазы – дистиллят (ректификат).
Кубовый остаток обогащается высококипящим компонентом (ВК).
Простая дистилляция применяется лишь для грубого разделения смеси с высокой относительной летучестью компонентов. Относительная летучесть α – отношение летучестей компонентов:
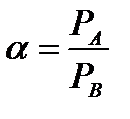 , где РА и РВ – давление насыщенных паров чистых компонентов.
, где РА и РВ – давление насыщенных паров чистых компонентов.
Идеальные растворы подчиняются законам Рауля и Дальтона. По закону Рауля парциальное давление компонента А в паре рА пропорционально мольной доле этого компонента хА в растворе:
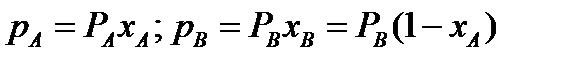 .
.
По закону Дальтона общее давление пара над раствором Р равно сумме парциальных давлений его компонентов:
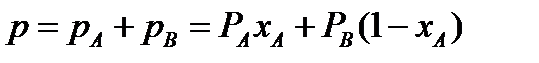 .
.
Графически эти законы – диаграммой р-х (давление-состав):
Зависимость общего давления Р и парциальных давлений от мольной доли хА (НК) – диаграмма р-х.
В расчетах обычно используют диаграммы T-x,y (P = const) и y-x (P = const).
Диаграмма T-x,y – зависимость температур кипения и конденсации от мольной доли НК в жидкой фазе хА и в паровой фазе уА.
Диаграмма у-х отображает зависимость между равновесными концентрациями НК в жидкой фазе хА и паровой уА* фазах. Равновесная линия – выше диагонали, т.к. на осях координат – мольные доли НК. По первому закону Коновалова пар обогащается НК. При х = 0,5; у*≈0,6.
Дата добавления: 2015-01-19; просмотров: 3448;
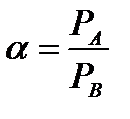 , где РА и РВ – давление насыщенных паров чистых компонентов.
, где РА и РВ – давление насыщенных паров чистых компонентов.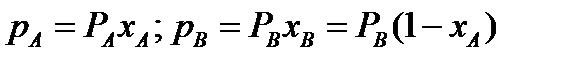 .
.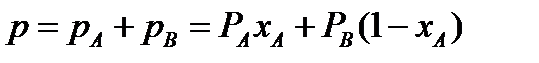 .
.