ОБМЕН ЖИРОВ
При декомпенсированном диабете часто повышается содержание в плазме СЖК, триглицеридов и холестерина. Распространенность гиперлипидемии при ювенильном диабете может достигать 50% [134]. Увеличение концентрации СЖК является следствием их усиленного высвобождения из жировых депо, так как скорость образования новых жирных кислот у больных диабетом снижена. Таким образом, при диабете увеличен приток СЖК из жировых депо в печень и другие ткани. Усиление липолиза происходит в результате выпадения нормального тормозного влияния инсулина на гормончувствительную липазу в жировой ткани. Кроме того, снижение утилизации глюкозы приводит к уменьшению содержания глицерин-3-фосфата, необходимого для реэстерификапии жирных кислот в самой жировой клетке.
Механизм гипертриглицеридемии при диабете более сложен [135]. В норме богатые триглицеридами липопротеины попадают в плазму либо в виде хиломикронов, образующихся из жира, содержащегося в пище, либо в виде липопротеинов очень низкой плотности (ЛПОНП), синтезируемых в печени и кишечнике. Высвобождение жирных кислот из триглицеридов обоих видов и их поглощение жировой тканью зависят от дгипрпротеиновой липазы, содержащейся в эндотелии капилляров и активирующейся инсулином. При нелеченом или недостаточно компенсированном диабете снижение активности липопротеиновой липазы обусловливает повышение уровня триглицеридов в плазме, что влияет на содержание хиломикронов, ЛПОНП или чаще обоих классов липопротеинов. В повышении синтеза триглицеридов может играть роль и увеличенная доставка жирных кислот в печень, поскольку в этом органе образование эфиров между жирными кислотами и глицерином при диабете не нарушается. В результате у больного декомпенсированным диабетом, несмотря на практически полное прекращение синтеза жирных кислот, может увеличиваться перегруженная жирами печень и повышаться уровень триглицеридов в крови. Гипертриглицеридемия наблюдается также при легком инсулинонезависимом диабете, особенно при ожирении. У больных в этих случаях гиперинсулинемия может стимулировать печеночную продукцию ЛПОНП [135].
Как частота, так и механизм повышения уровня холестерина при диабете остаются невыясненными [136]. По данным различных исследований, распространенность гиперхолестеринемии при инсулинозависимом диабете колеблется от <3 до >50%. Закономерная зависимость между контролем гликемии и уровнем холестерина в сыворотке отсутствует. Кроме того, при некомпенсированном диабете общий синтез стеролов повышается не всегда. Непостоянство связи нарушений холестеринового обмена с другими метаболическими показателями при диабете может определяться тем фактом, что инсулин стимулирует синтез холестерина в кишечнике, но подавляет холестериногенез в печени. В любом случае гиперхолестеринемия является, вероятно, одним из факторов, обусловливающих ускорение развития атеросклероза при диабете.
При резко выраженной недостаточности инсулина изменения жирового обмена в жировой ткани, печени и мышцах обусловливают накопление кетоновых тел (бета-оксибутират, ацетоацетат и ацетон). Как уже отмечалось, нормальный «сдерживающий» эффект инсулина на кетонемию обусловливается его способностью тормозить липолиз, снижать окисление жирных кислот до кетоновых тел в печени и стимулировать утилизацию последних мышцами. При тяжелой инсулиновой недостаточности увеличивается
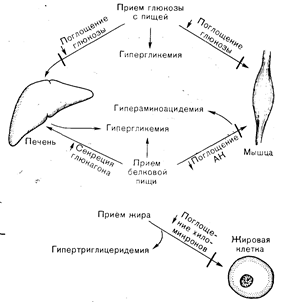
Рис.10—35. Патологическая физиология метаболических нарушений в состоянии сытости у больных диабетом. Снижение поглощения глюкозы печенью и мышцами приводит к гипергликемии после приема углеводной пищи. После потребления белковой пищи развивается гипераминоацидемия из-за снижения поглощения аминокислот (АК) мышцей; гипергликемия обусловливается не встречающим противодействия эффектом чрезмерного повышения уровня глюкагона в плазме. После приема жирной пищи сниженная активность липопротеиновой липазы определяет уменьшение клиренса хиломикронов и снижение поглощения свободных жирных кислот (СЖК) жировой тканью, что приводит к гипертриглицеридемии. Может наблюдаться и увеличение продукции триглицеридов печенью вследствие повышенной доставки СЖК в этот орган. как доставка жирных кислот в печень, так и активность фермента, ограничивающего скорость окисления жирных кислот в данном органе (ацилкарнитинтрансфераза). Изменения активности этого фермента в печени опосредуются повышением содержания карнитина и снижением уровня малонил-СоА (первый промежуточный продукт синтеза жирных кислот), который в норме ингибирует ацилкарнитинтрансферазу [15]. Дополнительную роль в механизме гиперкетонемии играет снижение утилизации кетоновых тел мышцами.
РЕЗЮМЕ
Слегка или умеренно выраженный дефицит инсулина характеризуется невозможностью восстановления или увеличения запасов энергетических веществ в организме при потреблении пищи (рис. 10—35). при потреблении пищи, содержащей глюкозу, отсутствие поглощения ее печенью и в меньшей мере мышцами обусловливает гипергликемию. Пpи поступлении белка дефицит инсулина приводит к снижению поглощения аминокислот мышцами и развитию гипераминоацидемии. Гиперсекреция глюкагона в ответ на :белковое питание вызывает гипергликемию. При потреблении пищи, содержащей жир, появляется гипертриглицеридемия после еды, обусловленная недостаточной элиминацией
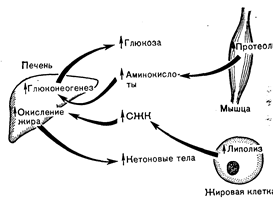
Рис.10—36. Патологическая физиология метаболических нарушений в состоянии натощак у больных инсулинозависимым диабетом. Гипер-гликемия определяется повышением глюконеогенеза, стимулируемого отчасти ускоренным протеолизом и высвобождением аминокислот из мышцы, что лежит и в основе гипераминацидемии. Повышенный липолиз приводит к увеличению уровня свободных жирных кислот (СЖК) в плазме. Гиперкетонемия является результатом повышенной доставки СЖК в печень, равно как и усиленной стимуляции b-окисления в печени (см. рис.10—9).
жирных кислот из циркулирующих хиломикронов вследствие снижения активности липопротеиновой липазы.
При более выраженном дефиците инсулина наблюдается повышение уровня в крови всех этих энергетических веществ: глюкозы, аминокислот, жирных кислот, а также кетоновых тел не только в состоянии сытости, но и натощак (рис. 10—36). Повышение содержания субстратов в крови происходит вследствие ускоренного опустошения запасов энергетических веществ в организме (повышенный протеолиз и липолиз), а также чрезмерной продукции глюкозы и кетоновых тел из соответствующих предшественников (аминокислот и жирных кислот), в избытке поступающих в кровоток.
Дата добавления: 2015-01-19; просмотров: 1195;
