СЕКРЕЦИЯ ГЛЮКАГОНА
Unger постулировал, что метаболические расстройства при диабете определяются не только дефицитом инсулина, а что диабет представляет собой бигормональное нарушение, при котором важное значение имеет относительная или абсолютная гиперглюкагонемия [88]. Доказательства важности изменения секреции глюкагона в патогенезе диабета были получены в различных исследованиях. У больных диабетом глюкоза не подавляет секрецию глюкагона, а введение белка или аминокислот вызывает гиперсекрецию его [24] (рис. 10—34). В отличие от этого реакция глюкагона на гипогликемию у больных диабетом I типа снижена, что указывает на дефект рецепторов глюкозы на поверхности а-клеток [128]. Кроме того, у экспериментальных животных диабет, вызываемый панкреатэктомией, сопровождается чрезмерной продукцией внепанкреатического глюкагона [88]. Далее, снижение уровня глюкагона в плазме, вызываемое соматостатином, приводит к уменьшению степени диабетической гипергликемии [52].
Несмотря на привлекательность бигормональной теории, некоторые данные вызывают серьезные сомнения в значимости глюкагона или первичного нарушения функции а-клеток при спонтанном диабете у человека [84, 89]. Повышение уровня глюкагона в плазме (вызываемое инфузией этого гормона) до его уровня при диабете или других состояниях, сопровождающихся гиперглюкагонемией, не нарушает толерантности к глюкозе у здоровых лиц и не снижает степени компенсации гликемии у больных диабетом, пока они получают инсулин [129]. У лиц с удаленной поджелудочной железой внепанкреатический глюкагон не образуется, однако гипергликемия и кетоз все же развиваются [81]. Подобно этому, длительное подавление секреции глюкагона и инсулина с помощью соматостатина вызывает транзиторную гипогликемию, сменяющуюся гипергликемией натощак и избыточной продукцией глюкозы (т. е. диабетическое состояние), несмотря на продолжающееся подавление секреции глюкагона [89]. У больных с инсулинозависимым диабетом, у которых соматостатин существенно снижает уровень глюкозы после еды, этот эффект определяется в основном торможением всасывания углеводов и белков, а не повышением утилизации углеводов [53]. Наконец, лечение инсулином приводит к ликвидации гиперглюкагонемии при диабете у человека и к восстановлению функции а-клеток при экспериментальном диабете [85].
Таким образом, основная роль глюкагона при диабете заключается в том, что он усиливает последствия дефицита инсулина. Согласно этому, вызываемая приемом пищи секреция глюкагона у больного при некомпенсированном диабете увеличивает степень гипергликемии после еды. Кроме того, гиперглюкагонемия при диабетическом кетоацидозе усиливает кетогенез в печени [15].
Первичную роль в развитии гипергликемии глюкагон играет у больных с синдромом глюкагономы (см. далее).
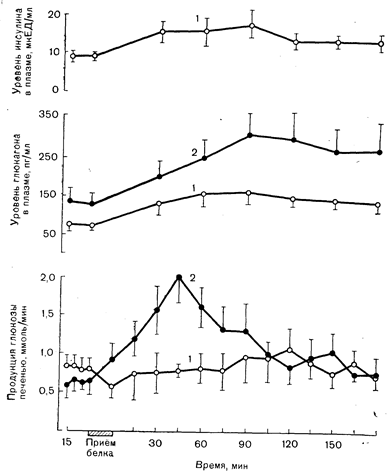
Рис. 10—34. Влияние белковой пищи на уровень глюкагона в плазме и продукцию глюкозы органами брюшной полости (печенью) у здоровых лиц (1) и больных инсулинозависимым (I тип) диабетом (2). Содержание инсулина в плазме больных не определяли, поскольку они предварительно получали его. Белковая пища обусловила выраженное повышение продукции глюкозы у больных диабетом, но не у здоровых лиц. Это различие было следствием чрезмерного повышения уровня глюкагона в плазме на фоне абсолютного дефицита инсулина (по данным Wharen J., Felig P., Hagenfeldt L., J. Clin. Invest., 1976, 57, 987).
Дата добавления: 2015-01-19; просмотров: 1596;
