І. Реакції приєднання
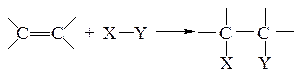
1. Приєднання водню (+Н2) – гідрування з утворенням алканів:
Pt
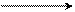 СН2=СН2 + Н2 CН3−СН3
СН2=СН2 + Н2 CН3−СН3
Етен або Ni,150˚С Етан
2. Приєднання галогенів (+ F2, Cl2, Br2, I2) – галогенування з утворенням дигалогеналканів:
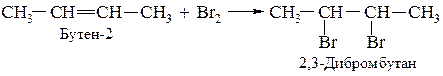
Бромна вода (розчин Br2 у воді) має жовтий колір. При взаємодії з алкенами вона обезбарвлюється, тому реакція з бромною водою використовується для ідентифікації алкенів (якісна реакція на алкени).
3. Приєднання галогеноводнів (+НHal) – гідрогалогенування, утворюються моногалогеналкани:
СН2 = СН2 + НCl → CH3− CH2Cl
Етен Хлоретан
Приєднання галогеноводнів до несиметричних алкенів відбувається за правилом В.В. Марковнікова.
Правило Марковнікова.При приєднанні речовин типу НХ (Х = Hal, ОН і т.п.) до несиметричних алкенів атом водню приєднується до атома вуглецю з кратним зв’язком, зв’язаним з більшим числом атомів водню:
Наприклад:
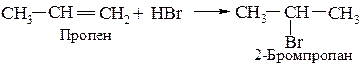
Орієнтація приєднання пояснюється поляризацією молекули несиметричного алкена в результаті дії індуктивного ефекта алкільних груп:
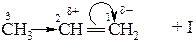
Метильна група відштовхує електрони σ–зв’язку СН3−С−, що призводить до поляризації π–зв’язку. Електрони π–зв’язку є дуже рухливими, тобто легко зміщуються до атому С (1). Це зміщення показують зігнутою стрілкою( 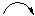 ). В результаті на атомі С (1) виникає частковий негативний заряд δ‾, а на атомі С (2) частковий позитивний заряд δ+. При приєднанні галогеноводню протон Н+ приєднується до атома С (1), який несе частковий негативний заряд.
). В результаті на атомі С (1) виникає частковий негативний заряд δ‾, а на атомі С (2) частковий позитивний заряд δ+. При приєднанні галогеноводню протон Н+ приєднується до атома С (1), який несе частковий негативний заряд.
При наявності в молекулах ненасичених вуглеводнів замісників, які проявляють значний електронно акцепторний ефект, реакція приєднання Н−Х іде проти правила Марковнікова: СН2=СН−Х (Х= CN, CF3, NO2,COOH)
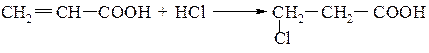
4. Приєднання води (+Н2О) – гідратація з утворенням насичених одноатомних спиртів (алканоли СnH2n+1OH)
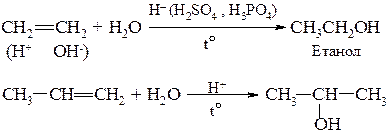
Дата добавления: 2015-03-23; просмотров: 1510;
