Физиология и регуляция функции яичек
Яички состоят из системы сперматогенных канальцев, где образуются и транспортируются сперматозоиды, и скоплений интерстициальных клеток, или клеток Лейдига, которые вырабатывают андрогенные стероиды.
Клетки Лейдига
Синтез тестостерона. Биохимические реакции превращения стерина, содержащего 27 углеродных стероатомов, — холестерина — в андрогены и эстрогены показаны на рис. 330-1. Холестерин в клетке Лейдига может либо синтезироваться de novo, либо поступать в нее из липопротеидов плазмы. Холестерин превращается в тестостерон под воздействием пяти ферментов или ферментных комплексов. При этом боковая цепь холестерина отщепляется в два этапа, что приводит к уменьшению размера молекулы (с 27 углеродных атомов до 19), а кольцо А стероида приобретает 4-З-кето-конфигурацию. Упомянутыми пятью ферментами являются 20,22-десмолаза, комплекс З-гидроксистероиддегидрогеназа-4,5-изомераза, 17-гидроксилаза, 17,20-десмолазаи 17 -гидроксистероиддегидрогеназа. Первые четыре фермента содержатся и в надпочечниках.
Реакция, ограничивающая скорость синтеза тестостерона, — это превращение холестерина в прегненолон под действием 20,22-десмолазы. Лютеинизирующий гормон (ЛГ) гипофиза регулирует активность этого фермента, а также других, участвующих в биосинтезе тестостерона. В клетке Лейдига синтезируются в небольших количествах и другие стероиды, включая эстрадиол.
Секреция и транспорт тестостерона. В норме в семенниках содержится лишь около 0,02 мг тестостерона. Поэтому, чтобы обеспечить суточную секрецию в плазму в среднем 5—6 мг гормона (что характерно для здорового молодого мужчины), это количество должно полностью обновляться примерно 200 раз в сутки (рис. 330-2). Тестостерон в плазме транспортируют связывающие белки, главным образом альбумин и специфический транспортный белок — тестостеронсвязывающий глобулин (ТеСГ). Связанная и несвязанная фракции гормона в плазме находятся в динамическом равновесии, причем на долю свободной фракции приходится примерно 1—3% общего количества гормона. Та доля присутствующего в крови тестостерона, которая может поступать в ткани, приблизительно равна сумме свободной и связанной с альбумином фракций, т. е. у здорового человека — около 40—45% общего содержания тестостерона в плазме.
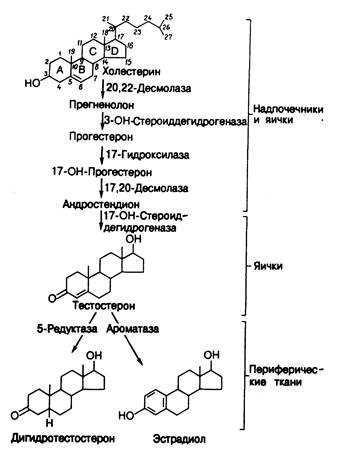
Рис. 330-1. Пути образования андрогенов в яичках и превращения андрогенов в другие активные гормоны в периферических тканях.
Периферический метаболизм андрогенов. Тестостерон—это циркулирующий в крови предшественник (или прогормон), служащий для образования двух других активных метаболитов, которые опосредуют многие физиологические процессы, лежащие в основе эффекта андрогенов (см. рис. 330-1). С одной стороны, тестостерон может восстанавливаться в 5-положении с образованием дигидротестостерона, который и обусловливает многие дифференцировочные, ростовые и функциональные сдвиги, характерные для развития особей по мужскому типу и для вирилизации. У особей обоего пола присутствующие в крови андрогены могут также превращаться в периферических тканях в эстрогены. Таким образом, физиологические эффекты тестостерона отражают сочетанное влияние самого тестостерона и активных андрогенных и эстрогенных его метаболитов. Кроме того, у здоровых мужчин небольшие количества эстрадиола и дигидротестостерона секретируются семенниками, а также образуются из слабого надпочечникового андрогена — андростендиона.
Количественные соотношения между циркулирующими в крови андрогенами и образующимися эстрогенами у здорового молодого мужчины показаны схематически на рис. 330-2. Скорость продукции тестостерона и андростендиона в среднем составляет соответственно 6 и 3 мг/сут. Всю продукцию эстрона (в среднем 66 мкг/сут) можно отнести за счет
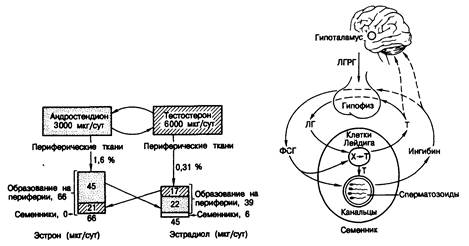
Рис. 330-2. Продукция андрогенов и эстрогенов у здорового молодого мужчины.
В верхних квадратах указана средняя продукция андростендиона и тестостерона, а в нижних — средняя суточная продукция эстрона и эстрадиола. Эстрогены образуются путем ароматизации (квадратные скобки) вне железы или непосредственно секретируются яичками. Вертикальные стрелки отражают скорости ароматизации андрогенов вне железы, а горизонтальные — взаимопревращение андрогенов и эстрогенов под действием 17-гидроксистероиддегидрогеназы. Таким образом, эстрадиол образуется из тестостерона плазмы, из эстрона и в результате прямой секреции яичками. (Из Р. С. MacDonald et al.)
Рис. 330-3. Регуляция образования тестостерона и сперматозоидов лютеинизирующим (ЛГ) и фолликулостимулирующим гормоном (ФСГ). Обозначения: Х — холестерин, Т — тестостерон.
его образования из циркулирующих в крови предшественников. Средняя скорость продукции эстрадиола — примерно 45 мкг/сут; около 35% этого количества образуется из тестостерона крови, 50% — из слабого эстрогена эстрона и 15%) непосредственно секретируется в кровь семенниками. При повышении уровня гонадотропинов количество эстрадиола, секретируемого семенниками, увеличивается.
Восстановленные в 5-положении и эстрогенные метаболиты могут оказывать местное (паракринное) действие в тех тканях, где они образуются, или попадать в кровь и действовать как гормоны на другие ткани. Дигидротестостерон крови образуется главным образом в тканях-мишенях для андрогенов, тогда как эстрогены образуются во многих тканях, особенно в жировой. Общая скорость образования эстрогенов вне эндокринных желез возрастает с увеличением массы жировой ткани и с возрастом.
Содержащиеся в плазме тестостерон и его активные метаболиты инактивируются в печени и выводятся из организма преимущественно с мочой; примерно половина их количества, обновляющегося в течение суток, экскретируется в составе 17-кетостероидов мочи (в основном в виде андростерона и этиохоланолона), а остальная часть выводится в виде полярных соединений (диолы, триолы и конъюгаты).
Гонадотропная регуляция и секреция тестостерона. Секреция тестостерона регулируется гипофизарным ЛГ (рис. 330-3). (Подробности функции гипофиза см. в гл. 321.) Секрецию тестостерона может повышать также фолликулостимулирующий гормон (ФСГ), стимулируя, вероятно, созревание клеток Лейдига. В свою очередь тестостерон регулирует чувствительность гипофиза к гипоталамическому либерину — рилизинг-гормону лютеинизирующего гормона (ЛГРГ). Хотя в гипофизе тестостерон может превращаться в дигидротестостерон и эстрогены, но главным регулятором секреции гонадотропинов служит все же сам тестостерон. Он влияет также на центральную нервную систему, замедляя образование или секрецию ЛГРГ и уменьшая частоту импульсов его секреции. В обычных условиях процесс секреции ЛГ очень чувствителен к влиянию тестостерона по механизму обратной связи: полное подавление секреции ЛГ происходит при введении уже таких количеств экзогенного андрогена, которые примерно равны его суточной продукции (около 6 мг). Однако при длительном повышении уровня ЛГ в плазме (как это наблюдается при тестикулярной недостаточности) понижается чувствительность гипофиза к регулирующему действию экзогенного андрогена по механизму отрицательной обратной связи.
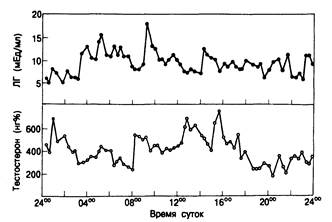
Рис, 330-4. Суточный профиль концентрации Л Г и тестостерона в плазме крови здорового мужчины (отбор проб каждые 20 мин). (Из Griffin a. Wilson, 1980.)
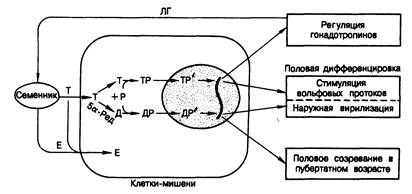
Рис. 330-5. Современные представления о действии андрогенов.
Обозначения: Т — тестостерон, Д — дигидротестостерон, Е — эстрадиол, Р — рецепторный белок, Р' — трансформированный рецепторный белок, Л Г — лютеинизирующий гормон, 5а-Ред — 5и-редуктаза.
Ни концентрация тестостерона, ни уровень ЛГ в плазме не остаются постоянными; для них характерны импульсные колебания, что отражает изменения скорости секреции этих гормонов (рис. 330-4). Резкие выбросы Л Г и тестостерона во сне свидетельствуют о начале полового созревания у мальчиков. У пожилых мужчин суточные колебания амплитуды секреторных импульсов ЛГ и тестостерона сглаживаются; максимальная концентрация этих гормонов по утрам лишь на 10—15% превышает их уровень в остальное время суток.
Действие андрогенов. Основные функции андрогенов заключаются в регуляции секреции гонадотропинов, формировании мужского фенотипа в процессе половой дифференцировки и индукции полового созревания с последующим поддержанием деятельности половых органов. Клеточные механизмы, посредством которых осуществляются эти функции андрогенов, схематически представлены на рис. 330-5. Тестостерон (Т) проникает в клетку путем пассивной диффузии. Внутри клетки он может превращаться в дигидротестостерон (Д) под действием фермента 5-редуктазы. Затем Т или Д связываются с цитозольным белком — рецептором андрогенов (Р). Гормонрецепторный комплекс (ТР или ДР) трансформируется таким образом, что приобретает способность связываться с ДНК (ТР' или ДР') и транслоцируется в ядро, где и прикрепляется к специфическим участкам хромосом. В результате образуется новая информационная РНК и в цитоплазме клетки появляется новый белок.
Хотя тестостерон и дигидротестостерон взаимодействуют с одними и теми же рецепторами, физиологическая роль их неодинакова. Комплекс тестостерон—рецептор регулирует секрецию гонадотропинов, а также обусловливает фазу стимуляции вольфовых протоков в процессе половой дифференцировки (см. гл. 333). Комплекс же дигидротестостерон— рецептор определяет внешнюю вирилизацию во время эмбриогенеза и основную часть андрогенного действия при половом созревании и половой жизни взрослого мужчины, включая инициацию и поддержание сперматогенеза. Механизм разграничения этих функций тестостерона и дигидротестостерона неизвестен. Неизвестны также механизмы, посредством которых эстрогены усиливают или блокируют влияния андрогенов. Предполагают, что действие эстрадиола опосредуется механизмом, аналогичным таковому для андрогенов, но с привлечением своего собственного рецепторного белка (см. гл. 331).
Семенные канальцы и сперматогенез
Нормальная функция семенных канальцев зависит как от влияния гипофиза, так и от активности прилежащих клеток Лейдига; для запуска и поддержания нормального сперматогенеза необходимы и ФСГ, и андрогены (см. рис. 330-3). ФСГ действует в основном на клетки Сертоли в семенных канальцах. Последние содержат также специфические рецепторы андрогенов. Андрогены, по-видимому, требуются для начальной стадии сперматогенеза, тогда как ФСГ — для конечных стадий развития сперматид. У здорового взрослого мужчины этот механизм обеспечивает образование более 200 млн сперматозоидов в сутки.
Клетка Сертоли не способна синтезировать стероидные гормоны de novo, и ее активность определяется тестостероном, диффундирующим в нее из соседних клеток Лейдига. В сертолиевых клетках, однако, тестостерон превращается в эстрадиол и дигидротестостерон. Семенные канальцы вырабатывают также пептидный гормон ингибин, который регулирует секрецию ФСГ гипоталамо-гипофизарной системой (см. рис. 330-3). Неясно, является ли ингибин главным физиологическим регулятором ФСГ; тестостерон и эстрадиол также могут ингибировать секрецию ФСГ, а изменив частоту импульсов ЛГРГ, можно избирательно повысить секрецию ФСГ.
Сложная система, в которой функцию семенников регулируют два гормона гипофиза, создает очень точный механизм двойного контроля, где уровень тестостерона в плазме и образование сперматозоидов оказывают обратное влияние на гипоталамо-гипофизарную систему, регулируя скорости собственной продукции (см. рис. 330-3).
Дата добавления: 2015-03-17; просмотров: 1037;
