Реакция на острую травму
Реакция организма при острой травме включает в себя сложное взаимодействие множества гомеостатических процессов. Хотя общую реакцию на травму легче всего представить, рассматривая отдельные компоненты нейроэндокринной, метаболической и иммунной систем, важно понимать, что многие молекулярные, клеточные, гуморальные и физиологические механизмы и каскады развиваются интерактивно.
Конечная способность пострадавшего пациента оправиться от инсульта зависит от динамической взаимосвязи между реакцией организма и своевременным медицинским или хирургическим вмешательством (рис. 1).
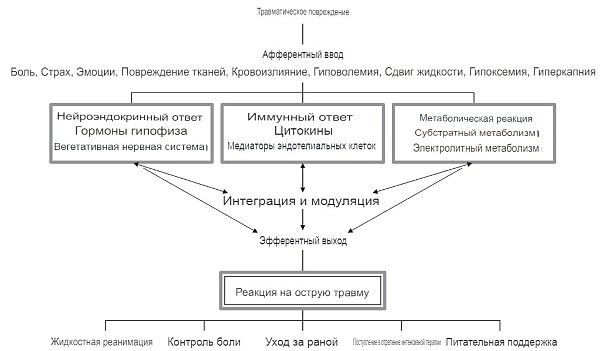
Рисунок 1. Принципиальная схема, отображающая взаимодействие нейроэндокринной, иммунной и метаболической систем после травматического повреждения. Обработка и интеграция многочисленных раздражителей, а также модуляция посредством взаимодействия различных медиаторов формируют общую биологическую реакцию. Модификация этой реакции с помощью терапевтических вмешательств способствует достижению и поддержанию гомеостаза
Нейроэндокринная реакция на травму. Классический нейроэндокринный рефлекс включает в себя афферентные стимулы, интеграцию и модуляцию центральной нервной системы, а также эфферентную отдачу.
После травматического повреждения специальные датчики обнаруживают множественные дискретные химические и физиологические нарушения. После локальной трансдукции раздражителей эти сигналы передаются в центральную нервную систему по определенным нервным путям и направляются в высокоспециализированные клеточные ядра для обработки и интеграции с другими сигналами.
Результирующим эфферентным эффектом является секреция различных гормональных веществ отдельными системами органов. На интенсивность и характер выделения этих гормонов влияют короткие рефлекторные дуги и длинные регуляторные петли обратной связи, как стимулирующие, так и тормозящие.
Афферентный вход. После тяжелой травмы разрушение тканей и кровоизлияние, по-видимому, являются двумя наиболее важными ранними изменениями. Периферические сенсорные рецепторы первичных ноцицептивных афферентных нейронов обнаруживают механическую деформацию и температурные изменения в месте повреждения. Поврежденные клетки выделяют химические вещества, такие как гистамин, калий, серотонин, тромбин и другие, которые также обеспечивают ноцицептивный эффект.
Клеточные тела этих нейронов находятся в спинномозговых корешковых ганглиях и передают сигналы в спинномозговой рог, где вторичные нейроны и коллатеральные пути соединяются с третичными нейронами в стволе головного мозга и таламусе.
Гиповолемия является наиболее распространенной причиной сердечно-сосудистого шока после травмы. Значительная потеря крови приводит к снижению эффективного объема циркулирующей крови и артериального давления. Повреждение тканей и задержка жидкости могут способствовать развитию гиповолемии.
Эти изменения ощущаются барорецепторами, чувствительными к давлению в аорте и сонных артериях, и рецепторами, чувствительными к растяжению в предсердиях и полой вене. Волокна от этих первичных нейронов поднимаются по блуждающему нерву к ядру одиночного тракта. Вторичные нейроны проецируются на медуллярную ретикулярную формацию и сердечно-сосудистые прессорные и депрессорные области ствола мозга.
Многие другие изменения, включая страх и тревожность, а также изменения концентрации кислорода, температуры и энергетических субстратов, обеспечивают афферентный вход в нейроэндокринную систему. Восприятие опасности или угрозы травмы стимулирует центральную лимбическую систему, волокна которой проецируются на гипоталамус. Оптическая, обонятельная или слуховая информация может давать существенные сигналы.
Травмы, которые влияют на дыхательные пути, дыхание или кровообращение, могут привести к гипоксии, гиперкарбии или ацидозу. Хеморецепторы, расположенные в сонных артериях и аорте, а также в центральной нервной системе, обнаруживают снижение концентрации кислорода в плазме крови и повышение концентрации углекислого газа или ионов водорода.
Волокна от этих нейронов проходят как к сердечно-сосудистому, так и к дыхательному центрам продолговатого мозга. Кровоизлияние и воздействие после травмы, приводящие к переохлаждению и изменению внутренней температуры, ощущаются в преоптической области гипоталамуса.
Интеграция и модуляция. Множественные сигналы, поступающие от разных проводящих путей, модулируются на нескольких уровнях. Первичный сигнал зависит от характера, интенсивности и продолжительности стимула. На реакцию влияют последовательная или повторяющаяся стимуляция, а также состояние и отзывчивость рецептора.
Сенсорный сигнал поступает в мозговой центр для интеграции с другими восходящими сигналами, интернейронами и нисходящими тормозными сигналами. Различные сигналы от ноцицепторов, барорецепторов, хеморецепторов, соматосенсорных афферентов и лимбической системы передаются от ядер ствола головного мозга к гипоталамусу.
Эфферентный выход. Регуляция гипофизом. Существует два основных компонента эфферентной части нейроэндокринной реакции: гормоны, контролирующие гипоталамо-гипофизарную систему, и гормоны, контролирующие вегетативную нервную систему. Гипоталамо-гипофизарно-надпочечниковая система (ГПА) была тщательно изучена и представляет собой модель нейроэндокринной системы реагирования на стресс.
Хотя кортикотропин-рилизинг-гормон (КРГ), адренокортикотропный гормон (АКТГ) и кортизол секретируются последовательно, точный контроль над системой достигается за счет нейронной интеграции, регуляции по контуру обратной связи и промежуточных веществ. Множество входов объединяются в паравентрикулярном ядре гипоталамуса (ПВН) для создания эфферентной дуги.
CRH является основным стимулятором синтеза и секреции АКТГ кортикотропинами передней доли гипофиза. АКТГ высвобождается в виде продукта расщепления проопиомеланокортина и впоследствии стимулирует синтез и высвобождение глюкокортикоидов из коры надпочечников.
Кортизол является основным глюкокортикоидом в ответ на стресс и оказывает широкое влияние на метаболизм организма. Среди его многочисленных метаболических эффектов - усиление выработки глюкагона и адреналина, приводящее к гипергликемии, стимуляция глюконеогенеза в печени, стимуляция высвобождения аминокислот в скелетных мышцах, приводящая к протеолизу, а также увеличение липолиза и высвобождения жирных кислот. Кортизол также играет важную роль в компенсаторной гиперосмолярной реакции, необходимой для полного восстановления объема циркулирующей крови. Степень повреждения влияет на интенсивность реакции CRH-АКТГ-кортизол.
В то время как более раннее кровоизлияние усиливает реакцию на АКТГ, циркадные факторы могут маскировать этот эффект. Наряду с повышением уровня кортизола в плазме крови теряются нормальные суточные колебания. Этот измененный паттерн секреции кортизола надпочечниками связан с аналогичной потерей суточных колебаний как секреции АКТГ, так и чувствительности коры надпочечников к стимуляции АКТГ.
При чистой гиповолемии уровень кортизола в плазме крови быстро нормализуется после восстановления объема циркулирующей крови. Устойчиво повышенный уровень кортизола свидетельствует о продолжающейся стимуляции в результате гипоксии тканей или последующей инфекции и связан со снижением выживаемости.
Гипоталамический тиреотропин-рилизинг-гормон (ТРГ) стимулирует высвобождение тиреотропного гормона (ТТГ) из передней доли гипофиза. ТТГ отвечает в первую очередь за высвобождение тироксина (Т4) из щитовидной железы, который периферически преобразуется в трийодтиронин (Т3).
Гормоны щитовидной железы также оказывают множество метаболических эффектов, наиболее важными из которых являются увеличение потребления кислорода и теплопродукции. После травмы периферическое преобразование Т4 в Т3 нарушается, и компенсаторного повышения уровня ТТГ не происходит.
Роль эндогенных опиоидов после травм и кровоизлияний является предметом активного изучения. Опиоиды, включая эндорфины и энкефалины, секретируются клетками центральной нервной системы, стенками кишечника и мозговым веществом надпочечников. Они воздействуют на различные рецепторы, вызывая различные эффекты. В центральной нервной системе опиоидные пептиды действуют как нейромедиаторы, которые ослабляют боль, подавляя ноцицепцию.
Избыточное высвобождение эндогенных опиоидных пептидов связано с сердечно-сосудистым коллапсом при шоке. Одним из предполагаемых механизмов опиоидной гипотензии после острого кровоизлияния является снижение симпатического оттока, опосредованное серотонинергическими путями. Было показано, что после геморрагического или септического шока введение антагониста опиатных рецепторов налоксона улучшает сердечно-сосудистую функцию, системное артериальное давление и продолжительность жизни.
Гормон роста (ГР), гонадотропины и пролактин - это другие гормоны передней доли гипофиза, участвующие в нейроэндокринной реакции. ГР способствует синтезу белка и повышается после травмы. Гонадотропин-рилизинг-гормон (ГнРГ) стимулирует выработку фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ), которые подавляются после травмы. Хотя гипоталамус оказывает тонизирующее действие на высвобождение пролактина гипофизом, сообщалось о повышении его уровня после травмы у взрослых.
Аргинин-вазопрессин (АВП), или антидиуретический гормон, синтезируется в гипоталамусе и транспортируется в заднюю долю гипофиза для хранения. Секреция АВП увеличивается сразу после травмы. Стимулами для высвобождения АВП являются повышение осмоляльности плазмы и изменение эффективного объема циркулирующей крови. Действие АВП включает реабсорбцию свободной воды в дистальных почечных канальцах и собирательных протоках, сужение периферических и селезеночных сосудов, а также гликогенолиз и глюконеогенез в печени.
Вегетативная регуляция. Катехоламины являются важными компонентами физиологической реакции на травму. Норадреналин в первую очередь высвобождается из окончаний аксонов постганглионарных нейронов с последующим попаданием в плазму. Скорость высвобождения норадреналина коррелирует с интенсивностью активности симпатической нервной системы.
Адреналин непосредственно выделяется в кровоток в результате стимуляции мозгового вещества надпочечников. Как и другие гормоны, катехоламины оказывают как гемодинамическое, так и метаболическое действие, включая усиление сердечно-сосудистой функции, сужение сосудов, печеночный гликогенолиз и глюконеогенез, а также периферический липолиз.
Система ренин-ангиотензин-альдостерон служит для поддержания внутрисосудистого объема крови. Ренин катализирует превращение ангиотензиногена в ангиотензин I в почках, который, в свою очередь, превращается в ангиотензин II в малом круге кровообращения. Ангиотензин II и АКТГ являются стимуляторами секреции альдостерона корой надпочечников. Основным действием альдостерона является усиление активности фермента Na+/K+-АТФазы в дистальных извитых канальцах почек и собирательных протоках, что приводит к увеличению реабсорбции натрия и выведению калия.
Инсулин и глюкагон играют противоположные роли в поддержании гомеостаза субстратов. Инсулин является основным анаболическим гормоном и способствует накоплению углеводов, белков и липидов. После травмы активность симпатической нервной системы подавляет секрецию инсулина бета-островковыми клетками поджелудочной железы, а кортизол подавляет усвоение глюкозы, что в конечном итоге приводит к гипергликемии и катаболизму. Глюкагон синтезируется в альфа-островковых клетках поджелудочной железы и усиливает катаболизм белков и липидов за счет усиления гликогенолиза и глюконеогенеза в печени.
Дата добавления: 2024-07-17; просмотров: 2119;
