Второе начало термодинамики (устанавливает определённое направление течения процессов в природе – стрела времени).
В процессе эксплуатации месторождений в пластах непрерывно изменяются давление, количественное соотношение газа и нефти, а иногда и температура. Это сопровождается непрерывными изменениями состава газовой и жидкой фаз и переходом различных углеводородов из одной фазы в другую. Особо интенсивные процессы таких превращений происходят при движении нефти по стволу скважины от забоя к устью. Вследствие быстрого падения давления из нефти выделяется значительное количество газа и около устья поток
Термодинамические функции.
Наряду с энтропией можно пользоваться можно пользоваться множеством других, связанных с ней функций состояния.
Предлагаемый вашему вниманию курс лекций неразрывно связан с решением проблемы извлечения углеводородов сложного состава из плотных низкопроницаемых коллекторов, составляющих, как сейчас принято говорить, трудноизвлекаемые запасы углеводородов (сокращённо ТРИЗ).
Почему возникла именно эта проблема?
Обеспечение высокого уровня добычи углеводородного сырья, в настоящее время, невозможно без вовлечения в разработку новых месторождений.
Если ранее, на протяжении многих десятилетий углеводородные залежи разрабатывались по большей части без использования различных методов воздействия, то сейчас ситуация кардинально меняется.
Как показывает практика, во вновь открываемых залежах углеводородов растёт доля ТРИЗ. Что же это такое ТРИЗ?
К ТРИЗ мы относим ту часть запасов жидких углеводородов, извлечение которой требует применения активных методов разработки (в отличие от пассивного режима истощения).
Необходимо подчеркнуть, что разработка залежей ТРИЗ не эффективна на режиме истощения и предполагает использование различных методов воздействияна продуктивный пласт (применение тепловых методов воздействия, закачка растворителей и т.д.), которые в свою очередь требуют серьёзную научную проработку.
Прежде всего, к ТРИЗ мы относим ретроградный конденсат.
Кроме ретроградного конденсата к ТРИЗ относятся:
- дегазированная нефть тонких, как правило, нефтяных оторочек;
- углеводороды, приуроченные к слабо дренируемым зонам пласта (с ухудшенными ФЁС и с проявлением эффекта НГД);
- углеводороды в тонких пропластках коллекторов в толще неколлекторов;
- рассеянные жидкие углеводороды (РЖУ) - связанная нефть;
- сорбированная пористой средой часть углеводородов.
Если ранее удерживать высокие годовые отборы углеводородов удавалось игнорируя трудноизвлекаемые запасы, то далее уже невозможно будет ограничиваться только малоэнергоёмкой добычей.
Доля ТРИЗ увеличивается. Добыча этих ресурсов предполагает привлечение внешней (сверх пластовой) энергии.
Рентабельная разработка ТРИЗ может осуществляться только с применением методов и технологий, требующих повышенных капиталовложений и эксплуатационных затрат по сравнению с традиционно используемыми способами.
Как я уже подчёркивал ранее, говоря о моделировании процесса разработки, я буду стараться отражать классические представления на проблему, с одной стороны, и, с другой стороны, постараюсь донести до вас новые подходы к решению проблемы, разрабатываемые во ВНИИГАЗе.
Например, ещё в школе вас учили, что основным состоянием, которым занимается наука, является равновесное состояние. А неравновесное состояние является переходным, временным.
Относительно неравновесности можно сказать: «Давайте подождём, пока система не придёт в равновесие, а потом будем её изучать».
Однако, если оглянуться вокруг, то мы увидим, что весь окружающий нас мир – неравновесен. И венцом неравновесности является живая материя и человек. Поэтому, почему бы не изучать то состояние, в котором мы находимся.
Анализ экспериментальных данных приводит нас к заключению, что при создании современных методов моделирования процессов разработки месторождений, содержащих ТРИЗ, необходимо исходить из того, что разрабатываемая залежь представляет собой открытую термогидродинамическую систему.
Флюидальная система (ФС), как составная часть пластовой фильтрационной системы (ПФС), являясь открытой, - крайне неравновесна. Как следствие, имеющие место в процессе разработки залежи фазовые переходы с понижением числа сосуществующих фаз также неравновесны, о чём свидетельствуют представленные ниже результаты некоторых экспериментальных исследований.
1. Процесс испарения ретроградного конденсата. Представляет собой фазовый переход двухфазная система (жидкость - пар) 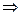 однофазная система (газ).
однофазная система (газ).
Полученные в лабораторных условиях данные свидетельствуют, что на размере образца 1 см3 характерные времена релаксации к равновесному состоянию (выравнивание разности концентраций неравновесных фаз в 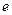 раз в результате диффузии компонентов) составляют несколько суток.
раз в результате диффузии компонентов) составляют несколько суток.
Можно полагать, что на размере залежи, протяжённостью несколько сотен и тысяч метров времена релаксации системы к равновесному состоянию могут достигать десятков и даже сотен лет.
2. Фазовые переходы в двухфазной системе рассеянные жидкие углеводороды (РЖУ), представляющие собой связанную нефть – углеводородный (УВ) газ.
Характерные времена релаксации РЖУ – УВ газ значительно превышают характерные времена релаксации к равновесному состоянию в случае испарения ретроградного конденсата (пример 1). Это обусловлено тем, что РЖУ содержат компоненты с большей молекулярной массой и меньшей диффузионной способностью, чем ретроградный конденсат.
3. Сорбционно-десорбционные процессы в системе сорбировая (связанная) углеводородная фаза – мобильная часть флюидальной системы.
Неравновесность процесса десорбции обусловлена тем, что сорбированная фаза обогащена высокомолекулярными компонентами с пониженной диффузионной способностью.
Трудноизвлекаемость углеводородов обусловлена двумя глобальными причинами.
Во-первых – результатами деятельности человека (техногенные причины).
Во-вторых – природными особенностями, как коллектора, так и насыщающего его флюида.
Анализировать причины трудноизвлекаемости углеводородов удобно на двух масштабах:
- на макроскопическом масштабе, соответствующем масштабу залежи, если мы рассматриваем месторождение, либо масштабу модели, в случае лабораторных исследований (от долей метра до тысяч метров);
- на микроскопическом масштабе, соответствующем масштабу отдельной поры (от долей микрона до сотен микрон).
На макроскопическом уровне причины трудноизвлекаемости углеводородов неразрывно связаны с макроскопической неоднородностью: высокой неоднородностью распределения проницаемости и пористости по коллектору, напластованием, малой толщиной пропластков, большой глубиной залегания залежи и т.д.
Как результат традиционных методов разработки месторождений на истощение мы имеем:
- выпадение конденсата, парафинов, резин и асфальтенов в коллекторе;
- селективное внедрение подошвенной воды в залежь и защемление углеводородов за фронтом внедрения;
- защемление углеводородов вследствие высокой пространственной неоднородности резервуара и напластования и т.д.
На микроскопическом уровне причины трудноизвлекаемости углеводородов обусловлены:
- процессами и явлениями вследствие влияния обширной поверхности коллектора;
- формированием немобильных граничных фаз;
- трансформации свойств потока флюида и т.д.
В своих лекциях я не буду останавливаться на техногенных причинах. Упомяну только такие из них, как выбор неправильной системы разработки газоконденсатных месторождений, ведущий к выпадению жидких углеводородов в пласте, с последующей безвозвратной потерей значительной их части. Вообще-то техногенных причин, обусловленных неряшливой деятельностью человека, масса.
Мои лекции посвящены второй группе причин трудноизвлекаемости УВ, обусловленных природными факторами. Природные факторы охватывают всё многообразие особенностей строения пористых сред, особенностей фазового поведения, реологических свойств углеводородных флюидов и воды, насыщающих эти пористые среды.
Решение проблемы извлечения углеводородов сложного состава из плотных низкопроницаемых коллекторов, представляющих собой пористую среду с большой удельной поверхностью, невозможно без знания фазового поведения углеводородов, насыщающих эти коллектора. Экспериментально известно, что свойства жидких и газообразных углеводородов в пористой среде отличаются от их объёмных свойств. Это связано с взаимодействием флюида с поверхностью пористой среды и зависит как от состава флюида, так и от свойств поверхности. В результате этого взаимодействия, в частности, может возникнуть переход смачивания (на поверхности возникает макроскопический слой, обогащенный одной из компонент жидкости) или в поверхностном слое жидкости может образоваться гомеотропная или планарная структуры (молекулы жидкости ориентируются по отношению к поверхности перпендикулярно или параллельно). Это существенным образом изменяет фильтрационные свойства среды. Адекватное описание динамики движения многофазного флюида предполагает знание реологии отдельных фаз и механизма их взаимодействия с твердой стенкой скелета горной породы.
Однако современные представления о фильтрации флюидов основываются на том, что при одинаковых термобарических условиях фазовое поведение исследуемой системы в пористой среде остается таким же, как и в свободном объеме.
С точки зрения классической теории фильтрации значение твердого скелета пористой среды, прежде всего геометрическое, он ограничивает ту область пространства, в которой движется жидкость. Обычно силовое взаимодействие между скелетом и прилегающими к нему слоями жидкости не учитывается. Поэтому свойства пористой среды в теории фильтрации описываются некоторым набором геометрических средних характеристик. Теория фильтрации строится на представлении о том, что пористая среда и заполняющая её жидкость образуют сплошную среду. Для объёма, в котором заключено большое число пор и зёрен, достаточно представительны вводимые осреднённые характеристики. В применении к меньшим объёмам выводы теории фильтрации теряют силу.
Основные исследования поведения жидкостей и газов в пористых средах направлены на решение следующих вопросов:
- в какой степени понятие объемного фазового равновесия применимо для ограниченных систем? Например, имеют ли место конденсация или кристаллизация в очень узких порах? Существует ли некий критический размер пор, начиная с которого сосуществование фаз становится невозможным?
- какова структура поверхностных слоев флюида и как она зависит от геометрии пор и свойств каркаса?
- каковы реологические свойства поверхностных слоев, генерируемых скелетом горной породы?
- какое воздействие необходимо оказать на систему пористая среда - многофазный, многокомпонентный флюид (включая поверхностные слои), чтобы сместить границу раздела фаз в ту или иную сторону?
Чтобы ответить хотя бы на некоторые из этих вопросов, необходимы тщательные эксперименты, которых в настоящее время крайне мало.
Как я уже отмечал, отличительной особенностью плотных низкопроницаемых коллекторов является высокая удельная поверхность. Процессы и явления, затрудняющие извлечение углеводородов из таких коллекторов, проявляются в необычном фазовом поведении и режимах фильтрации углеводородов вследствие влияния обширной поверхности. Чем больше удельная поверхность пористой среды, тем значительнее трансформация фазового поведения флюида, заключенного в ней.
Необходимо различать особенности процессов, имеющих место при разработке чисто газовых месторождений и разработке нефтегазоконденсатных месторождений.
Разработка газовых месторождений осложнена поверхностными фазовыми переходами и явлениями в поровом пространстве на границе поверхность порового коллектора – сорбированный газ, поверхность порового коллектора – пленочная вода – газ.
Разработка нефтегазоконденсатных месторождений осложняется новыми явлениями вследствие особенностей состава флюида. На границе под воздействием влияния пористой среды молекулы конденсата и парафинов образуют гомеотропно ориентированные квазижидкокристаллические структуры. Молекулярная ориентация этих структур по отношению к стенке пористой среды предопределяет природу течения углеводородного флюида в целом.
Важным фактором, осложняющим извлечение углеводородов из пласта, является присутствие неуглеводородных компонентов и, в частности - воды. Реологические свойства воды, как и углеводородного флюида, резко изменяются вследствие влияния обширной поверхности. Вода, занимающая значительную часть пустот, сильно влияет на режим течения УВ флюида. Частичная насыщенность порового пространства низкопроницаемого коллектора водой ухудшает фильтрацию газа вследствие проявления эффекта первоначального градиента давления.
Нередко бывает, что скорость изменения внутреннего параметра 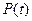 пропорциональна его отклонению от равновесного значения
пропорциональна его отклонению от равновесного значения 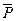 ; в этом случае
; в этом случае
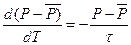 , (2)
, (2)
где 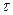 - постоянный множитель, называемый временем релаксации.
- постоянный множитель, называемый временем релаксации.
Интегрируя это выражение, получим
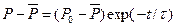 (3)
(3)
Здесь 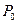 - неравновесное значение параметра
- неравновесное значение параметра 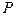 в начальный момент времени
в начальный момент времени 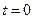 .
.
Из соотношения (3) видно, что 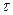 - время, в течение которого отклонение параметра от его равновесного значения уменьшается в
- время, в течение которого отклонение параметра от его равновесного значения уменьшается в 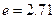 раза. Время релаксации
раза. Время релаксации 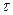 зависит не только от природы внутреннего параметра
зависит не только от природы внутреннего параметра 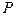 , но и от характера нарушения его равновесного значения. Например, если
, но и от характера нарушения его равновесного значения. Например, если 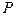 давление в данной точке внутри газа, то
давление в данной точке внутри газа, то 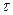 , связанное с нарушением равновесной концентрации молекул газа, будет одно, а
, связанное с нарушением равновесной концентрации молекул газа, будет одно, а 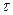 , связанное с нарушением равновесного распределения молекул по скоростям, - другое.
, связанное с нарушением равновесного распределения молекул по скоростям, - другое.
В силу этого зависимость 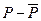 от времени может быть более сложной, чем (3); так, например,
от времени может быть более сложной, чем (3); так, например, 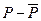 может равняться сумме экспоненциальных членов с разными временами релаксации
может равняться сумме экспоненциальных членов с разными временами релаксации 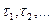 . Возможен и такой случай, когда зависимость
. Возможен и такой случай, когда зависимость 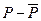 от времени имеет характер затухающих колебаний.
от времени имеет характер затухающих колебаний.
Если в системе реализуется термодинамическое равновесие только в отношении части переменных, описывающих систему, то говорят о неполном термодинамическом равновесии.
Величина времени релаксации может меняться в очень широких пределах.
Современные уравнения состояния, описывающие фазовое поведение как углеводородных, так и неуглеводородных смесей, были получены на основе анализа результатов исследований на установках фазового равновесия и не учитывают особенностей кинетики процессов фазовых переходов, ведущих к общей неравновесности системы.
Реальный фазовый переход всегда сопровождается отклонением системы от равновесия, он происходит с участием метастабильной фазы.
Например, интенсивный теплообмен при кипении приводит к большим локальным перегревам жидкости.
Процесс превращения метастабильной фазы в стабильную фазу следует изучать. Прежде всего, необходимо исследовать процессы релаксации основных термодинамических параметров системы из метастабильного состояния в стабильное.
Современные уравнения состояния устанавливают связь давления – температура – плотность. Эти параметры связаны с термодинамическими функциями (Гиббса, Гельмгольца и т.д.).
В общем случае функция распределения скоростей выражается рядом
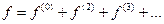 ,
,
где 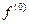 - максвелл - больцмановское распределение скоростей, а
- максвелл - больцмановское распределение скоростей, а 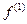 ,
, 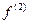 ,… - последующие приближения, зависящие от степени неравновесности системы
,… - последующие приближения, зависящие от степени неравновесности системы
Строго говоря, термодинамические функции могут быть точно определены только при термостатическом равновесии, когда 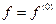 .
.
Неравновесность флюидальной системы обусловливает невозможность использования при её описании классических уравнений состояния (Пенга-Робинсона, Редлиха-Квонга, Соаве и т.д.), являющихся продуктом равновесной термодинамики (термостатики), изучающей только обратимые процессы.
Для описания неравновесных систем нужно использовать методы неравновесной термодинамики.
Второе начало термодинамики (устанавливает определённое направление течения процессов в природе – стрела времени).
Первая часть: Каждая термодинамическая система обладает функцией состояния, называемой энтропией (энтропия – изменение). Энтропия вычисляется следующим образом. Система переводится из произвольно выбранного начального состояния через последовательность состояний равновесия, вычисляются все подводимые при этом к системе порции тепла 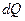 , делится каждая на соответствующую ей абсолютную температуру
, делится каждая на соответствующую ей абсолютную температуру 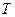 , и все полученные таким образом значения суммируются.
, и все полученные таким образом значения суммируются.
Вторая часть: При реальных (неидеальных) процессах энтропия изолированной системы возрастает 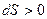 .
.
Если обозначить энтропию через 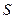 , то
, то
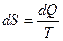 (2)
(2)
и получим соотношение Гиббса:
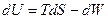 (3)
(3)
Это фундаментальное уравнение, объединяющее первое и второе начала, и в нём по существу заключена вся равновесная термодинамика.
Второе начало термодинамики позволяет судить о направлении процесса и имеет различные формулировки.
Томсона: «Невозможно построить периодически действующую машину, единственным результатом которой было бы поднятие груза за счёт охлаждения теплового резервуара».
Клаузиуса: «Теплота не может самопроизвольно переходить от тела менее нагретого к телу более нагретому».
Из второго постулата следует:
- существование энтропии как функции состояния системы;
- принцип возрастания энтропии.
В гигантской фабрике естественных процессов принцип энтропии занимает место директора, который предписывает вид и течение всех сделок. Закон сохранения энергии играет лишь роль бухгалтера, который приводит в равновесие дебет и кредит.
Третье начало термодинамики (тепловая теорема Нернста)
При абсолютном нуле температуры энтропия принимает значение 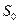 , не зависящее от давления, агрегатного состояния и других характеристик вещества. Эту величину можно положить равной рулю.
, не зависящее от давления, агрегатного состояния и других характеристик вещества. Эту величину можно положить равной рулю.
Теорема Нернста не вытекает из первых двух начал, поэтому в силу своей общности может рассматриваться как новый закон природы - третье начало термодинамики.
В отличие от нулевого, первого и второго начал теоремы Нернста не вводит в термодинамику новой функции состояния, однако именно она делает функции состояния численно определёнными и практически полезными.
Содержание тепловой теоремы Нернста сводится к двум утверждениям.
Первое утверждение состоит в том, что при приближении к абсолютному нулю энтропия стремится к определённому конечному пределу. Поэтому имеет смысл говорить об энтропии тела при абсолютном нуле температур. То есть интеграл
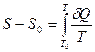
сходится.
Вторая часть теоремы Нернста утверждает, что все процессы при абсолютном нуле температур, переводящие систему из одного равновесного состояния в другое равновесное состояние, происходят без изменения энтропии.
В 1906 году немецкий физикохимик В.Г.Нернст сформулировал свою знаменитую тепловую теорему, ставшую третьим началом термодинамики. Тем самым было завершено аксиоматическое построение классической термодинамики.
Этот этап термодинамики сыграл выдающуюся роль в истории науки.
Логическая стройность равновесной термодинамики, основанной на четырёх началах, породила мнение, что термодинамика уже доведена до своего окончательного завершения. Эту точку зрения целиком поддерживал Нернст, считавший, что развитие термодинамики закончилось.
Такой взгляд не выдержал испытания временем. История науки свидетельствует, что всякая глубокая научная идея не может быть исчерпана до конца. Более того, сама идея развивается и обогащается по мере углубления наших знаний. Именно так обстоит дело с термодинамикой.
Теорема Нернста подвела итог развитию классической равновесной термодинамики.
Классическая термодинамика – это область физики, которая занимается изучением общих свойств макроскопических систем в равновесии, а также общих закономерностей при установлении равновесия.
Из всего многообразия макроскопических объектов, которые нас окружают или которые мы используем в повседневной жизни или работе, термодинамика изучает объекты только в состоянии термодинамического равновесия.
Под состоянием термодинамического равновесия подразумевается состояние, в которое с течением времени рано или поздно приходит система, находящаяся при определённых внешних условиях и определённой постоянной температуре окружающих тел.
При достижении термодинамического равновесия система забывает свою предысторию.
Она помнит только то, что сохраняется в силу законов сохранения (в изолированной системе это суммарные энергия, импульс и масса).
С этой точки зрения окружающий нас мир: мир животных, мир растений, мир неживой природы – представляют собой системы, не находящиеся в состоянии термодинамического равновесия.
Термодинамическое равновесие есть некая абстракция. По отношению к окружающему нас миру это упрощённая модель. Тем не менее, в огромном большинстве практически важных случаев она приводит к правильным результатам.
Термодинамика, как уже говорилось, изучает свойства равновесных состояний. А для равновесных состояний понятия времени не существует. Поэтому время в явном виде в термодинамику не входит (термодинамика не знает времени). В этом смысле об обычной термодинамике говорят как о термостатике (термин введён в 1854 г. В.Томсоном взамен «механической теории тепла»).
Термодинамика позволяет также сделать выводы об общих закономерностях процессов, происходящих при установлении равновесия. Эти выводы касаются направления необратимых процессов и их возможностей при данных условиях. Однако все выводы классической равновесной термодинамики о неравновесных процессах или неравновесных состояниях по-прежнему не включают времени. Утверждение о направлении процесса или запрета процесса не даёт никакой информации о скорости процесса.
Классический этап развития термодинамики кроме формулировки основных начал и анализа вытекающих из них следствий оставил нам в наследство программу действий, связанную прежде всего с необходимостью описания неравновесных процессов.
Классическая термодинамика является мощным средством исследования обратимых процессов. Могущество термодинамического метода состоит в том, что он позволяет получить основные закономерности квазистатических процессов, не вскрывая их молекулярного механизма.
Вполне естественно возникает идея о необходимости создания аналогичного метода для исследования необратимых процессов. В настоящее время такой метод создан и получил своё окончательное оформление под названием термодинамики необратимых процессов.
Сегодня закончена разработка основ линейной теории неравновесных процессов, завершившейся созданием линейной неравновесной термодинамики.
Одно из направлений завтрашнего дня - создание нелинейной феноменологической теории неравновесных процессов.
Термодинамика неравновесных необратимых процессов – это физическая теория макроскопического описания неравновесных процессов.
Дата добавления: 2014-12-09; просмотров: 1883;
