Электрическая проводимость растворов электролитов
Различают две основные группы проводников электрического тока: проводники I рода, электрическая проводимость которых обусловлена электронами (металлы, графит), и проводники II рода, обладающие ионной проводимостью (расплавы и растворы электролитов). В электрохимии рассматривают проводники II рода.
Согласно теории Аррениуса, электролиты в водном растворе диссоциируют на заряженные частицы – ионы, которые и являются переносчиками электричества. При этом одни электролиты – сильные диссоциируют в растворе полностью, другие – слабые – лишь частично; доля распавшихся частиц – степень электролитической диссоциации (α) зависит от концентрации электролита и температуры.
Величина, характеризующая способность веществ проводить электрический ток под действием внешнего электрического поля, называется электрической проводимостью.
Электрическая проводимость (L) – величина, обратная электрическому сопротивлению проводника (R). Измеряется в сименсах (См): См = Ом-1.
Так как
R =  , (99)
, (99)
то
 , (100)
, (100)
где ρ – удельное сопротивление;  - удельная электрическая проводимость; S – площадь сечения проводника; l – длина проводника.
- удельная электрическая проводимость; S – площадь сечения проводника; l – длина проводника.
Электрическая проводимость в растворах электролита зависит от числа ионов в объёме раствора между электродами и скорости их движения.
Для оценки проводимости растворов и влияния на неё различных факторов применяют две величины: удельную (Χ) и молярную (λ) электрическую проводимость.
Удельной электрической проводимостью (Χ) называют электропроводность раствора, находящегося между параллельными электродами площадью 1 см2, расположенными на расстоянии 1 см.
Удельная электрическая проводимость измеряется в См·см-1 или См·м-1.Удельная электрическая проводимость раствора электролита зависит от природы электролита, концентрации раствора и температуры.
Отношение расстояния между электродами l к их площади называют постоянной электролитической (кондуктометрической) ячейки
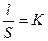 . (101)
. (101)
Подставляя (101) в уравнение (100), получаем:
Χ = К L . (102)
Величину К определяют экспериментально.
Молярная электрическая проводимость – мера электрической проводимости всех ионов, образующихся при диссоциации 1 моля электролита при данной концентрации.
Молярная электрическая проводимость равна электрической проводимости такого объёма (V,см3) раствора, в котором содержится 1 моль растворённого электролита, причём электроды расположены на расстоянии 1 см друг от друга.
Из определения удельной и молярной электрических проводимостей следует, что они связаны соотношением:
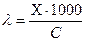 , (103)
, (103)
где С – концентрация, моль/дм3; λ – молярная электрическая проводимость, См·см2/моль; Χ – удельная электрическая проводимость, См/см.
Поскольку электрическая проводимость объёма раствора электролита определяется количеством в этом объёме ионов, переносящих электричество, и скоростью их миграции, для молярной проводимости справедливо соотношение:
λ = αF(U+ + U-), (104)
где U+ и U- – абсолютные скорости движения ионов; α – степень диссоциации электролита; F – число Фарадея, т.е. количество электричества, которое несёт 1 моль однозарядных катионов или анионов:
F = NA·e,
где NA = 6·1023 – число Авогадро, e = 1,6∙10-10 Кл – заряд электрона.
При разбавлении раствора молярная электрическая проводимость как сильных, так и слабых электролитов возрастает; для слабых электролитов – вследствие увеличения степени диссоциации (α), для сильных электролитов – в результате повышения абсолютной скорости движения ионов (U+ , U-).
Предельное значение λº, отвечающее молярной электрической проводимости гипотетического бесконечно разбавленного раствора, характеризующегося полной диссоциацией электролита и отсутствием сил электростатического взаимодействия между ионами, в соответствии с (104) можно выразить соотношением:
λº = F(U0+ + U0-). (105)
Произведения FU0+ = λ 
 и FU0- = λ
и FU0- = λ 
 называются предельными молярными проводимостями, или предельными подвижностями катионов и анионов.
называются предельными молярными проводимостями, или предельными подвижностями катионов и анионов.
Уравнение (105) можно представить в виде:
λº = λ 
 + λ
+ λ 
 . (106)
. (106)
Молярная электрическая проводимость электролита при бесконечном разбавлении (λº) равна сумме предельных подвижностей анионов и катионов.
Соотношение (106) было установлено Кольраушем и называется законом независимого движения ионов.
Предельная подвижность ионов зависит только от природы растворителя и температуры; для многих ионов эта величина определена экспериментально и приводится в справочниках.
Молярная электрическая проводимость слабых электролитов меньше, чем сильных,; так как даже при низких концентрациях степень диссоциации слабых электролитов мала (α‹1). Следовательно, несмотря на то, что в объёме раствора, заключённого между электродами, содержится 1 моль электролита, переносчиков электрического тока – ионов в данном объёме меньше, чем в растворе сильного электролита. Повышение молярной электрической проводимости слабых электролитов при разбавлении растворов связано с увеличением степени диссоциации.
Из уравнений (105) и (106) следует:
 , (107)
, (107)
где  - коэффициент электрической проводимости, характеризующийся степенью торможения ионов.
- коэффициент электрической проводимости, характеризующийся степенью торможения ионов.
Абсолютные скорости движения ионов в разбавленных растворах электролитов (U+ , U-) и в бесконечно разбавленных (U0+ , U0-) близки между собой (fλ=1), поэтому
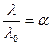 . (108)
. (108)
Для слабых электролитов отношение молярной электропроводности раствора при данном разбавлении (λ) к молярной электропроводности при бесконечно большом разбавлении (λº) характеризует истинную степень электролитической диссоциации. Степень диссоциации электролита в растворе заданной концентрации можно рассчитать, измерив молярную электрическую проводимость этого раствора и зная λº.
У слабых бинарных электролитов с разбавлением раствора увеличивается степень электролитической диссоциации и молярная электропроводность; константа же диссоциации при неизменной температуре остаётся постоянной величиной (закон разбавления Оствальда). Константа диссоциации Кдис, α, λ и концентрация (разбавление) подобных растворов связаны между собою следующими уравнениями:
Кдис = 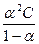 . (109)
. (109)
Учитывая уравнение (108),
Кдис = 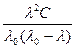 (110)
(110)
или
Кдис =  , (111)
, (111)
где V=1/C – разбавление раствора, л/г-экв.
Для сильных электролитов, диссоциирующих полностью (α=1),
 . (112)
. (112)
Уменьшение молярной электрической проводимости при переходе от бесконечно разбавленного раствора к растворам конечных концентраций у сильных электролитов связано только с уменьшением скоростей движения ионов. Сильные электролиты не подчиняются закону разбавления.
Пример 18. Для 0,01н KCl удельное сопротивление ρ = 709,22 Ом-1·см. Вычислите удельную(Χ) и молярную (λ) электрические проводимости.
Решение. Удельную электрическую проводимость вычисляем по уравнению
Χ = 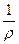 =
= 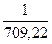 = 1,41∙10-3 Ом-1·см-1 = См·см-1.
= 1,41∙10-3 Ом-1·см-1 = См·см-1.
Молярная электрическая проводимость, согласно (103), можно выразить с помощью уравнения:
λ = 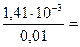 0,0141 См·см2/моль .
0,0141 См·см2/моль .
Пример 19. Вычислите молярную электрическую проводимость уксусной кислоты при бесконечно большом разбавлении при 298 К, если электрические проводимости HCl, CH3COONa, NaCl равны 0,0426; 0,0091; 0,0126 См·см2/моль соответственно.
Решение. Составляем систему уравнений согласно закону Кольрауша (106):
λHCl = λH+ + λCl- = 0,0426; (1)
λCH3COONa = 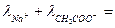 0,0091; (2)
0,0091; (2)
λNaCl =  = 0,0126. (3)
= 0,0126. (3)
Согласно (106) складываем уравнения (1) и (2), вычитаем из них уравнение (3) и получаем:
λHCl + λCH3COONa - λNaCl = λH+ +  0,0426 + 0,0091 – 0,0126 = 0,0391 См·см2/моль .
0,0426 + 0,0091 – 0,0126 = 0,0391 См·см2/моль .
Пример 20. Удельная электропроводность 0,0109 н раствора NH4OH при 18ºС 1,02·10-4 См·см-1, а 0,0219 н раствора 1,5·10-4 См·см-1. Вычислить для указанных растворов степень диссоциации NH4OH и концентрации гидроксильных ионов. Проверить, насколько точно растворы NH4OH соответствуют закону разбавления.
Решение. Вычисляем молярные электропроводности для первого и второго растворов по формуле (103):
 См·см2/моль,
См·см2/моль,
 См·см2/моль.
См·см2/моль.
По формуле (106), используя табличные данные, находим λº
λº = 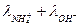 = 63,6 + 174 = 237,6 См·см2/моль.
= 63,6 + 174 = 237,6 См·см2/моль.
Значения α определяем по формуле (108):
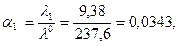

Вычисляем концентрацию ионов ОН- в растворах:

Зная α1 и α2, рассчитываем константу диссоциации NH4OH по уравнению (109) для двух растворов:
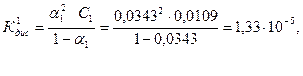 .
.
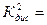
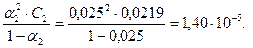
Величины 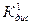 и
и 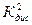 близки по значению. Следовательно, растворы NH4OH следуют закону разбавления.
близки по значению. Следовательно, растворы NH4OH следуют закону разбавления.
Вариант 1.
12. Электрическая проводимость 0,01моль/дм3 раствора хлорида калия при 25ºС равна 0,0034 См. Удельная проводимость этого раствора 1,41·10-3 См/см. Чему равна постоянная кондуктометрической ячейки?
Вариант 2.
12. Сопротивление кондуктометрической ячейки, содержащей 0,1 моль/дм3 раствора КСl, удельная электрическая проводимость которого равна 1,29∙10-2 См/см, составляет 1,16 Ом. Чему равна удельная проводимость этого раствора?
Вариант 3.
12. Постоянная кондуктометрической ячейки К = 0,41 см-1. Электрическая проводимость 0,02 моль/дм3 раствора уксусной кислоты равна 5,810-4 См. Чему равна молярная электрическая проводимость раствора?
Вариант 4.
12. Вычислите молярную электрическую проводимость 0,1 моль/дм3 раствора HCl, если удельная электрическая проводимость раствора 0,039 См·см-1.
Вариант 5.
12. Вычислите предельную молярную проводимость TlCl, если 
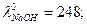

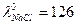 См·см2/моль.
См·см2/моль.
Вариант 6.
12. Удельная электрическая проводимость 0,1 моль/дм3 раствора этиламина при 25ºС равна 0,0015 См∙см-1. Предельная молярная проводимость 204 См·см2/моль. Найдите степень диссоциации и константу диссоциации этиламина.
Вариант 7.
12. Молярная проводимость водного раствора амида азотной кислоты H2N2O2, с=0,03 моль/дм3 равна 1,007 См·см2/моль. Предельные подвижности ионов равны: 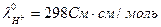 ,
, 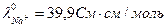 ,
, 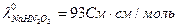 . Определите константу диссоциации по уравнению: H2N2O2 ↔ H+ + HN2O
. Определите константу диссоциации по уравнению: H2N2O2 ↔ H+ + HN2O  .
.
Вариант 8.
12. Удельная электрическая проводимость 0,001 моль/дм3 раствора уксусной кислоты равна 0,492·10-4 См/см. Чему равна константа диссоциации уксусной кислоты?
Вариант 9.
12. Произведение растворимости сульфата бария 1,3·10-10. Чему равна удельная проводимость насыщенного раствора BaSO4, если удельная проводимость воды 1,0·10-6 См/см?
Вариант 10.
12. Постоянная ячейки 0,41 см-1. Электрическая проводимость насыщенного раствора AgCl равна 8,317·10-6 См. Удельная электрическая проводимость воды 1,6·10-6 См/см. Считая молярную проводимость этого раствора равной предельной растворимости, найдите произведение растворимости AgCl.
Дата добавления: 2014-12-07; просмотров: 8397;
