Задача 19.
Процессы, протекающие на Fe c покрытиями из Sn и Zn в проводящей среде при рН=3 и доступе воздуха.
Решение.
Луженое железо Sn/Fe (пищевые емкости, консервные банки и др.)
а) Сравниваем стандартные потенциалы основного металла и покрытия:
Е0Sn2+/Sn = - 0,136 B > E0Fe2+/Fe = - 0,440 B - покрытие катодное.
б) Определяем равновесные потенциалы окислителей в заданной среде (рН=3)
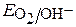 ≈ 1,23 – 0,059рН ≈ 1,05В;
≈ 1,23 – 0,059рН ≈ 1,05В; 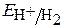 ≈ – 0,059рН ≈ -0,18 В
≈ – 0,059рН ≈ -0,18 В
в) Сравниваем значения потенциалов окислителей и металла-анода, делаем вывод о возможности данного процесса коррозии
ü Покрытие не нарушено:
- 0,136 В < 1,05 В возможна коррозия Sn с поглощением кислорода
- 0,136 В > -0,18 В невозможна коррозия Sn с выделением водорода
(A) Sn → Sn2+ + 2e
(К) O2 + 4H+ + 4 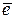 → 2H2О
→ 2H2О
ü Покрытие нарушено:
- 0,44 В < 1,05 В возможна коррозия Fe с поглощением кислорода
- 0,44 В < -0,18 В возможна коррозия Fe с выделением водорода
(A) Fe → Fe2+ + 2e
(К) 2H+ + 2 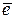 → H2
→ H2
O2 + 4H+ + 4 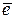 → 2H2O
→ 2H2O
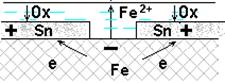
При повреждении катодного покрытия возникает коррозионный ГЭ, в котором основной материал - анод -растворяется, а материал покрытия – катод,на нем выделяется водород или поглощается кислород.
Оцинкованное железо Zn/Fe (ведра и др).
а) Сравниваем стандартные потенциалы основного металла и покрытия:
Е0Zn2+/Zn = - 0,763 B < E0Fe2+/Fe = - 0,440 B - покрытие анодное.
б) Определяем равновесные потенциалы окислителей в заданной среде (рН=3)
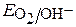 ≈ 1,23 – 0,059рН ≈ 1,05 В;
≈ 1,23 – 0,059рН ≈ 1,05 В; 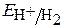 ≈ – 0,059рН ≈ -0,18 В
≈ – 0,059рН ≈ -0,18 В
в) Сравниваем значения потенциалов окислителей и металла-анода, делаем вывод о возможности данного процесса коррозии
ü Покрытие не нарушено:
- 0,763 В < 1,05 В возможна коррозия Zn с поглощением кислорода
- 0,763 В < -0,18 В возможна коррозия Zn с выделением водорода
(A) Zn → Zn2+ + 2e
(К) O2 + 4H+ + 4 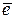 → 2Н2О
→ 2Н2О
2H+ + 2 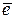 → H2
→ H2
ü Покрытие нарушено.
- 0,763 В < 1,05 В возможна коррозия Zn с поглощением кислорода
- 0,763 В < -0,18 В возможна коррозия Zn с выделением водорода
(A) Zn → Zn2+ + 2e
(К) 2H+ + 2 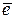 → H2
→ H2
O2 + 4H+ + 4 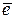 → 2H2O (процессы при нарушении анодного покрытия не меняются)
→ 2H2O (процессы при нарушении анодного покрытия не меняются)
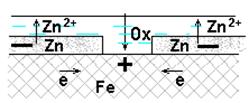
При повреждении анодного покрытия возникает коррозионный ГЭ, в котором основной материал - катодне растворяется, на нем выделяется водород или поглощается кислород, а материал покрытия – анод - разрушается.
ВЫВОД: Катодные покрытия (например, Pb, Cu, Ni) защищают М изделия в основном механически. Основное требование - сплошность, отсутствие пор, эластичность, водонепроницаемость, хим. стойкость. Анодные покрытия (например, Al, Zn, Cd) защищают изделие не только механически, но главным образом электрохимически, участвуя в анодном процессе.
Дата добавления: 2014-12-03; просмотров: 915;
