УФ-спектроскопия.
Для подтверждения подлинности исследуемого вещества использовали УФ-спектр спиртового раствора S3. Для этого готовили раствор по методике: точную навеску лекарственного вещества (0,05г) растворяли в спирте этиловом при нагревании на водяной бане в мерной колбе вместимостью 100 мл. Раствор охлаждали и доводили растворителем до метки (раствор А).
1мл раствора А переносили в мерную колбу вместимостью 5мл и доводили этанолом до метки (раствор Б).
Измеряли оптическую плотность полученного раствора на спектрофотометре марки «СФ - 101» в кварцевых кюветах толщиной 1 см, раствор сравнения – этанол, в диапазоне длин волн от 240 до 310 нм. Спектр поглощения представлен на рисунке 13.
| λ, нм |
| А |
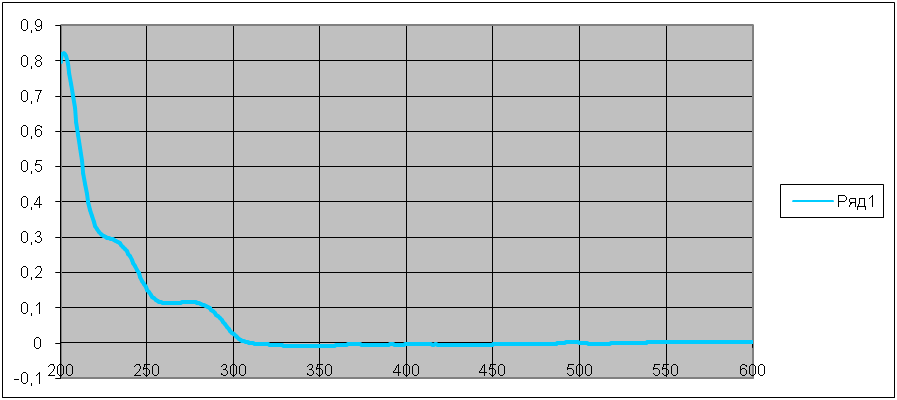
Рисунок 13 - УФ-спектр 0,001% спиртового раствора S3
Наблюдается одна полоса поглощения с максимумом в области 276 нм.
В связи с тем, что электронные спектры не дают полной качественной характеристики, следующим этапом явилось подтверждение подлинности S3 с помощью ИК- спектрофотометрии (рисунок 14 ).
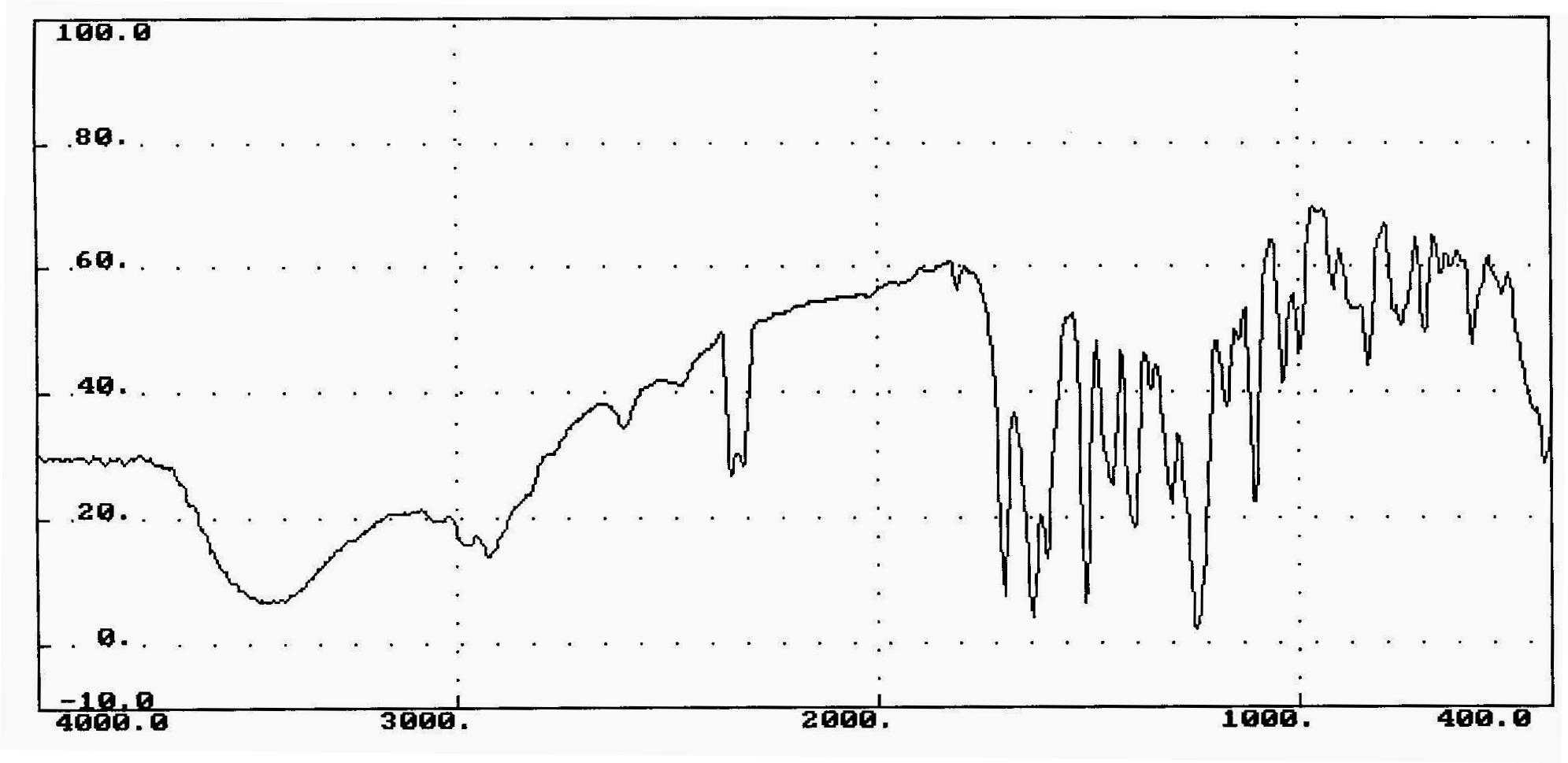
Рисунок 14 - ИК-спектр S3.
ИК-спектр, снятый в таблетках калия бромида (KBr), позволил обнаружить в молекуле S3 следующие полосы поглощения соответствующие определенным функциональным группам: 1693 см-1 (C=О связь в СООН группе), 1590 см-1 (С=О связь в >N-C=O группе).
Таким образом на основании данных спектров (ИК-, УФ-) подтверждается структура 4-[1-(4-этоксифенил)-6,7-диметокси-3-оксо-3,4-дигидро-1Н-изохино-лин-2-ил]-бензойной кислоты. В табл. 2 приведены данные физических и физико-химических свойства вещества S3.
Таблица 2 - Некоторые характеристики вещества S3
| Характеристика | Числовые показатели | |
| Описание | Белый кристаллический порошок, без запаха | |
| Растворимость | Вода | Практически нерастворим |
| Этанол | Растворим | |
| Температура плавления | 258 - 260 | |
| рН раствора (рН 5% спиртового раствора) | 5,5 | |
| Тонкослойная хроматография, этанол | Rf = 0,53 | |
| УФ-спектроскопия (этанол) | 276 нм(max); | |
Использование качественных реакций для определения подлинности вещества S3.
а) Идентификация кето-группы.
Реакции конденсации с аминами в щелочной и кислой среде с образованием оксимов и гидразонов. Методика: 0,01 г вещества S3 растворяли в 1 мл спирта этилового при нагревании на водяной бане в течение 10 минут. Добавляли 1 мл щёлочи и 1 мл раствора 2,4-динитрофенилгидразина. К такому же раствору вещества добавляли 1 мл щёлочи и 1 мл раствора гидроксиламина. Наблюдали образование оксимов и гидразонов (Схема 1).
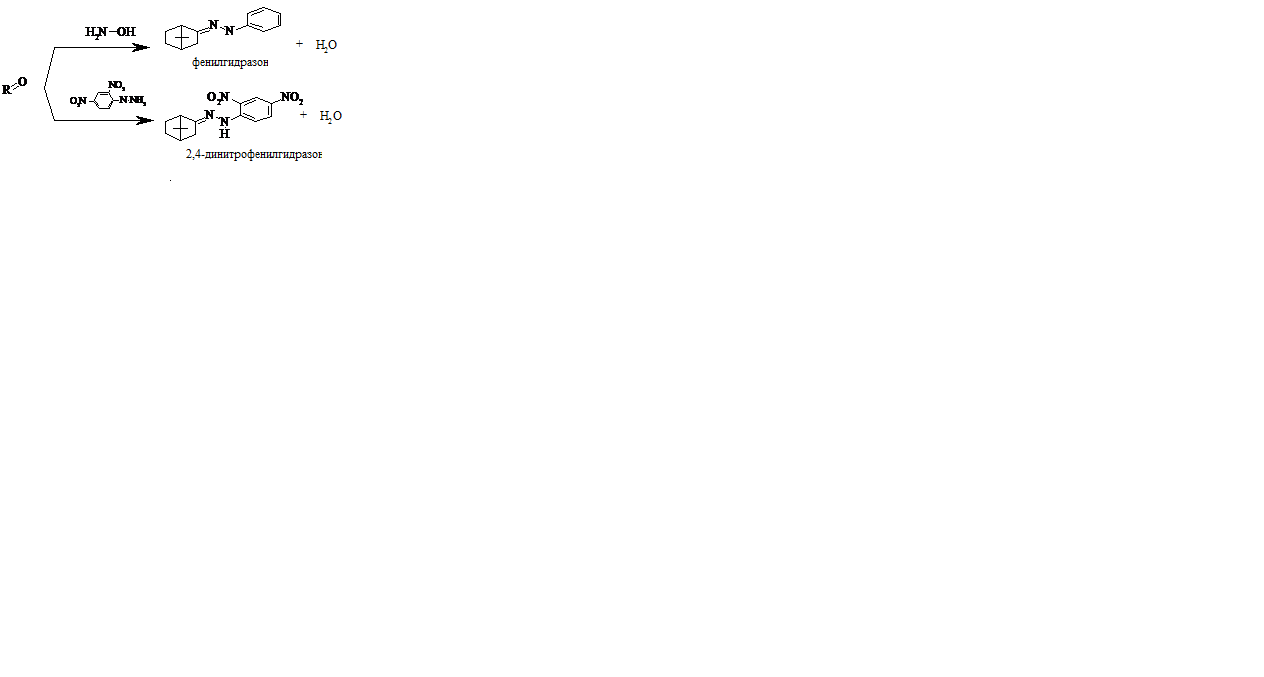
Схема 1. - Схема реакции идентификации кетогруппы
б) Идентификация третичной аминогруппы.
Реакции комплексообразования с общими и частными осадительными реактивами за счёт образования координационной связи (неподелённая пара электронов). Методика: на предметные стёкла помещали по 0,01 г исследуемого вещества. К пробам добавляли по несколько капель реактивов Драгендорфа, Майера, Мерме, Бушарда, Зонненштейна, Эрдмана, Марки, Фреде и серной кислоты концентрированной. Наблюдали появление жёлтой, розовой и фиолетовой окраски. При добавлении реактивов Майера, Марки, Зонненштейна, Бушарда и Мерме окраска не менялась. Те же реакции проводили со спиртовыми растворами вещества S3. Методика: по 0,01 г вещества растворяли при нагревании на водяной бане в течение 10 минут в этаноле в пробирках. В пробирки добавляли по несколько капель перечисленных реактивов. Наблюдали за изменением окраски растворов. При добавлении реактивов Эрдмана и Фреде окраска оставалась неизменной.
в) Идентификация этоксигруппы -
йодоформная проба. Методика: 0,01 г исследуемого вещества помещали в 1 мл воды очищенной и кипятили в пламени горелки в течение 10 минут для разрушения простой эфирной связи, фильтровали. Далее исследование проводили по известной методике идентификации спиртового гидроксила: к фильтрату добавляли 5 мл раствора натрия гидроксида, 2 мл 0,1 М раствора йода и наблюдали постепенное выпадение жёлтого осадка йодоформа, который обнаруживали также по характерному запаху.
г) Идентификация карбоксильной группы.
Реакции соле- и комплексообразования.
Реакции с растворами хлорида окисного железа, сульфата меди (ΙΙ), нитрата кобальта, нитрата свинца, сульфата бария и нитрата серебра. Методика: в пробирки помещали по 0,01 г исследуемого вещества и растворяли в 1 мл этилового спирта при нагревании на водяной бане в течение 10 минут, охлаждали, фильтровали. В каждую пробирку добавляли по 1 мл соответствующих реактивов. Наблюдали образование осадков жёлтого, голубого и белого цветов. В пробирках с растворами нитрата свинца и сульфата бария осадков не выпадало. Результаты физико-химических исследований 4-[1-(4-этоксифенил)-6,7-диметокси-3-оксо-3,4-дигидро-1Н-изохинолин-2-ил]-бензойной кислоты в таблице 3.
Таблица 3
Дата добавления: 2014-12-30; просмотров: 3653;
