НЕИЗОТЕРМИЧЕСКАЯ КИНЕТИКА
Методы термического анализа
Общим для неизотермических методов исследования является изучение изменения какого либо свойства исследуемой системы в зависимости от температуры. Основными методами термического анализа являются:
1. дифференциальный термический анализ (ДТА), регистрирующий разность между температурой образца и температурой эталона;
2. динамическая термогравиметрия, в качестве температурной функции фиксирующая либо изменение веса образца (термогравиметрический анализ – ТГА), либо скорость этого изменения (дифференциальная термогравиметрия – ДТГ);
3. дифференциальная сканирующая калориметрия (ДСК), замеряющая величину теплового потока dH/dT от образца (или к образцу);
4. газоволюмометрия, при которой определяемым параметром является объем газа, выделяющийся при нагревании образца.
Выбор того или иного метода зависит от характера изучаемого процесса. Если реакция идет со значительным изменением веса, то наиболее пригодны термогравиметрические методы (ТГА и ДТГ). Если при реакции выделяются значительные объемы газов, то естественен выбор газоволюмометрического метода. Реакции сопровождающиеся выделением или поглощением тепла, удобно исследовать при помощи методов ДТА или ДСК. Информативность методов может быть повышена если одновременно применять несколько методов. К примеру, очень распространено применение методов ДТА,ДТГ и ТГА, когда одновременно фиксируется изменение массы образца, скорость этого изменения и температура образца в зависимости от температуры окружающей среды. Изменения подобного рода проводят с помощью различных термовесов или многофункционального прибора под названием дериватограф. На получаемых графиках, так называемых дериватограммах, одновременно фиксируется температура печи (Т – кривая), изменение веса образца (ТГ), скорость изменения веса (ДТГ) и разность температур образца и эталона (ДТА). ТГ- кривая является интегральной кинетической кривой, ДТА – и ДТГ – кривые, представляют собой дифференциальные кинетические кривые.

 toC
toC
 ДТА
ДТА
 Т
Т
М ДТГ
200 Тm

 Dm,%
Dm,%
40 М
60 ТГ
t
Рисунок 42. Дериватограмма.
Точка пика дифференциальной кривой (М) соответствует температуре Tm при которой скорость реакции разложения максимальна.
Метод расчета кинетических параметров по термогравиметрическим и термографическим измерениям (метод Фримена и Кэррола).
Этот метод широко применяется для анализа термогравиметрических данных. Предполагается, что скорость реакции подчиняется уравнению
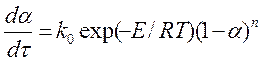 (155)
(155)
где k0 – предэкспоненциальный множитель, который характеризует вероятность реагирования и связывается с частотой колебания элементов кристаллической решетки и с величиной поверхности реагирующих веществ. При данном методе сравнивают скорости при двух температурах Т1 и Т2. Если прологарифмировать уравнение (154), то разность между прологарифмированными уравнениями для двух температур равна
 (156)
(156)
При постоянстве величины D(1/Т) - Dlg(da/dt) линейно связана с Dlg(1-a). Если эту зависимость представить графически, то отрезок , отсекаемый результирующей прямой на оси ординат, пропорционален энергии активации, а тангенс угла наклона прямой равен величине порядка реакции n. Скорости реакции и концентрации определяются по экспериментальным термогравиметрическим кривым через равные интервалы 1/Т.
 Dlg(da/dt)
Dlg(da/dt)
 0,1
0,1
 0
0
 -0,1 j
-0,1 j
 -E/2,3R
-E/2,3R
-0,3
-0,5
Dlg(1-a)
Рисунок 43. Обработка экспериментальных данных по методу Фримена и Кэррола. tgj = n.
Методом Фримена – Кэррола широко пользуются для расчета кинетических параметров, что объясняется важным преимуществом его перед другими методами: для получения кинетических данных требуется фактически один опыт (одна ТГ- либо ДТА – кривая).
Метод дифференциально-термического анализа (ДТА) может быть успешно применен для количественного определения теплот (и энтропий) фазовых переходов с последующим построением диаграмм состояния. Площадь пика на дифференциальной кривой пропорциональна величине теплового эффекта:
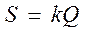 (157)
(157)
где Q – тепловой эффект, k – коэффициент пропорциональности. Для исключения k запись термограмм необходимо производить дважды: исследуемого вещества и некоторого стандартного вещества с известным тепловым эффектом при фазовом переходе. Если обе записи произведены в одинаковых условиях, то можно считать, что
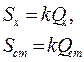 и
и 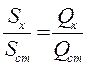 (158)
(158)
Выбор стандартного вещества определяется следующими условиями: близостью физико-химической природы исследуемого и стандартного веществ и, как следствие этого, близостью температур и энтальпий фазового перехода. Оценивать тепловые эффекты по соотношению площадей можно только при условии равенства температур фазовых переходов обоих веществ, так как площадь пика на дифференциальной кривой определяется не только тепловым эффектом, но и условиями теплопередачи (теплопроводностью и температуропроводностью образца). На практике пользуются пересчетным коэффициентом, учитывающим влияние разности температур
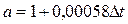 .
.
Отсюда
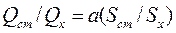 (159)
(159)
если Тст>Tx, или
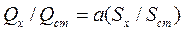 (160)
(160)
если Tx>Tст.
для стандартизации удобно производить запись обеих термограмм на одном листе. Энтальпия плавления определяется из соотношения
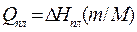 (161)
(161)
где – m – навеска вещества; М – молекулярный вес; DHпл – энтальпия фазового перехода; Qпл – экспериментально определенный тепловой эффект.
Тогда подставляя (161) в (160) и (159) получаем
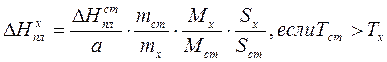 (162)
(162)
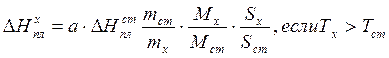 (163)
(163)
Зная энтальпию и температуру фазового превращения, легко определить энтропию этого процесса по формуле
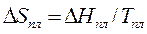 (164)
(164)
При отсутствии в системе фазового перехода, сопровождающегося тепловым эффектом, кривая Т нагрева идет монотонно. При наличие фазового перехода в результате выделения или поглощения тепла изменяется угол наклона или регистрируется горизонтальная площадка. Если тепловой эффект невелик, то вследствие низкой чувствительности прибора такая запись может его не зарегистрировать. Для увеличения чувствительности метода одновременно осуществляют так называемую дифференциальную запись. С помощью дифференциальной термопары.




 + - - +
+ - - +
 |  |
Образец Эталон
Рисунок 44. Принципиальная схема дифференциальной термопары.
Дифференциальная термопара представляет собой две включенные навстречу термопары, одинаковые по характеристикам. Одна термопара измеряет температуру исследуемого образца другая - эталона, в качестве которого выбирается вещество не претерпевающее фазовых превращений в изучаемом интервале температур. Нагрев образца и эталона ведется в одинаковых условиях.
 t oC
t oC

t
Рисунок 45. Образец термограммы.
Для регистрации фазовых превращений используют как кривые нагревания, так и кривые охлаждения. Использование кривых охлаждения как правило предпочтительнее, так как при этом система находится в состоянии, близком к равновесному (расплав легко гомогенизируется). Использование кривых нагревания всегда связано с возможностью регистрации неравновесных процессов. Однако многи системы склонны к переохлаждению, иногда значительному (до 80 –1000С), что затрудняет использование кривых охлаждения.
Дата добавления: 2014-12-26; просмотров: 1999;
